Detox 4: Grundlagenkurs ‚Halbwertzeiten‘ von Chelatoren (ALA, DMSA, DMPS) – Der wichtigste Aspekt vom Cutler-Protokoll
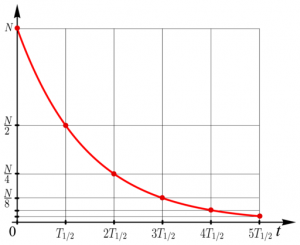
Halbwertzeit als grafisches Beispiel der Funktion. Quelle: Wikipedia. Lizenz: CC BY SA 4.0, Autor: Svjo
Halbwert(s)zeit – kennt ihr das noch von radioaktiven Stoffen wie Uran, Cäsium & Co.? Also die Zeit, ab der nur noch 50% von dem Zeug da ist – weil die andere Hälfte (in irgend etwas anderes) zerfallen ist?
Ein Beispiel: Cäsium-137 hat eine Halbwertzeit von 30 Jahren:
- nach 30 Jahren ist noch die Hälfte (50%) da,
- nach 60 Jahren 1/4 (25%),
- nach 90 Jahren 1/8 (12,5%)
- und nach 120 Jahren noch 1/16 (6,25%).
Das ganze gilt auch für pharmakologische Substanzen im Körper, u.a. auch so genannte Schwermetall-Chelatoren (u.a. DMPS, DMSA, ALA). Auch diese zerfallen bzw. werden im Körper metabolisiert und ausgeschieden. Dies geschieht bei den Chelatoren im Stundenbereich. Dabei wird ggf. mobilisiertes und gebundenes Quecksilber & Co. im Körper wieder freigesetzt -> bevor es ausgepinkelt oder ausge’stuhlt‘ wurde.
Ich hoffe, das Prinzip, wie eingangs auch abgebildet, ist klar. In der Wikipedia steht dann noch mal zu Halbwertzeit:
„ist die Zeitspanne, nach der eine mit der Zeit abnehmende Größe die Hälfte des anfänglichen Werts (oder, in Medizin und Pharmakologie, die Hälfte des Höchstwertes) erreicht.“
Insofern möchte ich dieses wichtige Prinzip auf Basis der Überlegungen von Andrew Hall Cutler [6], im Artikel vorstellen. Themen sind u.a.:
- Was hat das alles mit der Quecksilber-Mobilisierung & Ausleitung zu tun?
- Nur Andrew Hall Cutler berücksichtigte die pharmakologische Kinetik & Halbwertzeit der Chelatoren
- Was ist nun der ‚Deal‘ bei ALA in Vergleich zu DMPS & DMPS?
- Pharmakokinetik der Halbwertzeit in der Praxis
- Was hat Cutler anders gemacht?
- Noch was wichtiges zur Alpha-Liponsäure
- Gibt es auch Kritik an Cutler in Bezug auf seine Halbwert-Zeiten?
Am Ende folgt mein übliches Fazit.
Hinweis: Mehr Interesse am Thema? Dann empfehle ich die Themenseite hier im Blog zur Schwermetall- & Quecksilber (Amalgam) Ausleitung, Cutler & Co.
Inhaltsverzeichnis für den Schnellzugriff
Was hat das alles mit der Quecksilber-Mobilisierung & Ausleitung zu tun?
Ganz viel! Im Textbook of Clinical Neurology, 2nd ed., Goetz et al., Elsevier, 2003 [11] steht denn auch auf Seite 1177 steht denn auch zur pharmakologischen Halbwertzeit, welche sich auf die Dosierung bzw. zeitliche Zufuhr von Medikamenten auswirkt (übersetzt mit deepl.com) [12]:
„Die Halbwertszeit (t1/2) ist die Zeit, die benötigt wird, bis die Serumkonzentration eines eines Medikaments, nach der vollständigen Absorption und Verteilung einer Einzeldosis um 50 Prozent abnimmt. Die Halbwertszeit eines Arzneimittels bestimmt die Dosierungshäufigkeit und in der Regel sollte das Dosierungsintervall eine Halbwertszeit nicht überschreiten. Medikamente mit kurzen Halbwertszeiten sollten mehrmals am Tag verabreicht werden, um um große Schwankungen in der Serumkonzentration zu vermeiden, die zu unerwünschte Wirkungen oder hervorrufen können. Medikamente mit längeren Halbwertszeiten können einmal täglich verabreicht werden, was im Allgemeinen die Compliance verbessert.“
Was bedeutet das?
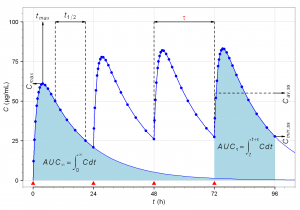
Pharmakologische Halbwertzeit als grafisches Beispiel: Plasmaspiegel über 96 Stunden nach oraler Verabreichung alle 24 Stunden (τ). Absorptionshalbswertzeit 1 h, Eliminationshalbswertzeit 12 h. Quelle: Wikipedia. Lizenz: CC BY 3.0, Autor: Alfie66
Dass alle Arzneistoffe – also DMSA, DMPS, aber auch die Alpha-Liponsäure (ALA)– von Abbauprozessen im Metabolismus (-> Biotransformation, Ausscheidung, etc.) betroffen sind. Oft kann man im Kontext der körpereigenen Entgiftung etwas über Phase I, II und III der Entgiftung lesen [3]. Diese Prozesse, welche für das Verarbeiten von Giften und Stoffwechsel-Metaboliten und das Verbessern der Ausscheidung von Toxinen aus dem Körper notwendig sind, haben auch Auswirkung auf die so-genannten Schwermetall-Chelatoren.
Die ungefähren – (sehr) vereinfachten – Halbwertzeiten der klassischen Chelatoren liegen (bei oralen Aufnahme der Chelatoren), je nach Quelle [4][5][6], auch abhängig von der Dosis, was vorher im Magen war, dem Alter & anderem, zwischen:
- DMSA: 3-4 h
- DMPS: 6-10 h
- RS-ALA: Nach Cutler Einnahme alle 2-3 h, wobei die Halbwertszeit grob um die 60 Minuten liegt.
Warum soll nun ALA alle 2-3 h eingenommen, wenn die Halbwertszeit 60 Minuten ist? Das ist so, weil der ALA-Metabolit Dihydroliponsäure (DHLA) der eigentliche Chelator ist. Nach Studien soll (orales) ALA seinen Höhepunkt nach ca. 60-90 Minuten erreichen und hat eine Halbwertzeit von ca. 2 bis knapp 3 Stunden – je nach Dosis, Nüchtern oder nicht, etc.
So finden sich zur Anflutung der einzelnen Stoffe im Serum (Blut) bis zum Maximum (Tmax), je nach Quelle, verschieden Angaben. Zu berücksichtigen ist hier auch: Je schneller die Phase-1 des Leber-Metabolismus, desto schneller werden einige Chelatoren (u.a. DMPS) abgebaut. Auch einige Supplemente können die Phase 1 (aber auch 2) beschleunigen (z.B. T3, Niacin, Lakritze, Ginseng) bzw. Bremsen (z.B. Nicotinamid, Eisenmangel). Insofern sind die Halbwertzeiten nicht ’statisch‘ sondern durchaus (in maßen) variabel.
Das bedeutet: Nach dem die Chelatoren eingenommen werden – verbinden sich diese (hoffentlich) mit einem Quecksilber (Hg)-Ion, wobei diese Verbindung wieder zerfallen kann – irgendwo im Körper – also auch bevor sie über Stuhl und Urin ausgeschieden werden können. Bei ALA ist das aber nochmals komplexer, denn ALA selber ist kein Chelator – sondern nur das DHLA. Das ALA diffundiert in die Zellen, in die Mitochondrien, wird dort in DHLA umgewandelt, bindet da hoffentlich an ein Hg-Ion, etc. Auf den detaillierten Prozess mag ich hier nicht eingehen.
Nur Andrew Hall Cutler berücksichtigte die pharmakologische Kinetik & Halbwertzeit der Chelatoren
DMPS. Quelle: Wikipedia
Cutler war Chemiker – und diesem war im Gegensatz zu vielen Ärzten – auch die Pharmakokinetik der als Chelatoren eingesetzten Verbindungen wie DMPS und DMSA klar. Diese binden sich mit ihren Thiol- (SH-) Gruppen an ein Quecksilber-Atom bzw. Ion das irgendwo rumschwimmt -> Mobilisierung von Hg. Wenn die Verbindung wieder zerfällt, wird jedoch das Hg-Ion wieder ‚frei gelassen‘. Und wenn das an einem ungünstigen Ort passiert – dann kann das ganze Projekt Schwermetall-Ausleitung ‚Netto‘ schlimmer, also mit einer (ungünstigen) Verschiebung des Hg und einer ‚Re-Vermüllung‘ der Organe enden. Denn die Ausscheidung über Urin und Stuhl benötigt einiges an Zeit.
Cutler behauptete nun (in etwa), dass es bei einem Chelatbildner zwei Dinge zu beachten gibt:
- Erstens die Stärke der Bindung zwischen dem Chelatbildner und dem Schwermetall-Atom und
- die Häufigkeit, mit der der Chelatbildner das Schwermetall absetzt und wieder aufnimmt (genannt Kinetik)
Schaut man nun auf die verfügbaren Daten zu den Halbwertzeiten von RS-ALA, hier speziell der R-Komponente, dann werden verschiedenste Halbwertzeiten angegeben [u.a. 7]. Dabei ist jedoch der Verlauf der Kurve der Halbwertzeit(en) oft weit weg vom idealen Verlauf. Wer sich allerdings mehr mit ALA beschäftigt, der wird feststellen, das, wie weiter oben schon angeführt, nicht RS-ALA ist der ‚eigentliche‘ Chelator, sondern DHLA, also die reduzierte Version der Alpha-Liponsäure [8]. Letztendlich geht es also um die Halbwertzeit von DHLA-Hg-Komplexen im Organismus – was jedoch stark von ALA abhängig ist (-> Redox-Paar). Aus den verfügbaren Daten und aus Praxis-Erfahrungen ist dann der Einnahme-Intervall von (2 bis) 3 Stunden entstanden.
Was ist nun der ‚Deal‘ bei ALA in Vergleich zu DMPS & DMPS?
Alpha-Liponsäure (ALA) ist im Unterschied zu DSMA und DMPS auch Zell-Gängig und überwindet die Blut-Gehirn-Schranke [4][5][6]. Zwar ist in diesem Aspekt DMPS ggf. etwas besser als DMSA – aber nicht in der Weise von ALA [8]. Insofern ist eine unregelmäßige Einnahme, aus meiner Interpretation von Cutler, bei ALA auch schlimmer: Denn dies mobilisiert (als DHLA) das Hg auch intrazellulär und im Gehirn, so das Hg dort umverteilt und auch aus eher unkritischen Bindegeweben tief in Organe und insbesondere in das Gehirn verschleppt werden kann. Viele dieser Effekte merkt man dann erst Monate (oder Jahre) später. Deswegen ist aus Cutlers Sicht die pauschale Verwendung von Alpha-Liponsäure in NEM keine gute Idee für viele Menschen.
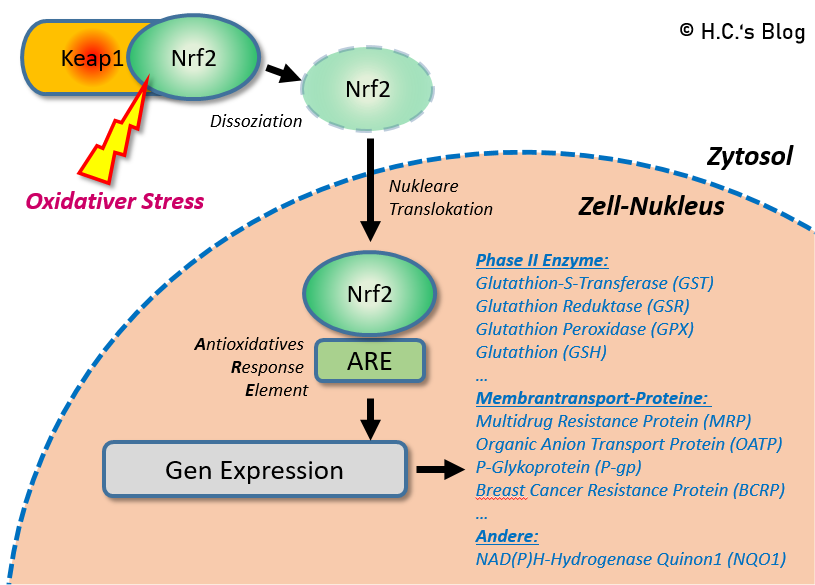
ALA hat jedoch noch andere Funktionen auf die Entgiftungssysteme u.a. als potenter Nrf2-Aktivator, welcher die Gluthation und Phase II & III Entgiftungs-Systeme hochregelt. Das war Cutler damals so wohl noch nicht bewusst und wird noch mal Thema eines anderes Beitrags. So argumentieren dann auch einige, u.a. Chris Shade, dass der ‚Entgiftungseffekt‘ über die Nrf2-Induktion seitens ALA größer sei, als der potentielle Chelator-Effekt von dem Cutler ausgeht. Aus Shade seiner Sicht existiert denn der direkte Chelator-Effekt von ALA, den Cutler auf Basis von Gregus et al. [10] und anderen herleitete, gar nicht. Für mich spiele beide Effekte eine Rolle – weswegen aus meiner Sicht einiges im Cutler-Protokoll optimiert werden sollte – speziell in Anbetracht des 2019er Buches, welches für mich in einigen Aspekten hinter dem 1999er zurückbleibt.
Pharmakokinetik der Halbwertzeit in der Praxis
In einer eigenen Grafik habe ich mal versucht die Unterschiede der regelmäßigen und niederdosierten Einnahme von Chelatoren nach dem Cutler-Protokoll auf Basis einer vereinfachten Pharmakokinetik zu visualisieren. Ich gebe zu bedenken, dass diese Grafik sehr idealisiert ist. Sie soll nur das grundsätzliche Prinzip verdeutlichen. In der Praxis beeinflussen dann viele Parameter die intestinale Absorption – z.B. ob die Chelatoren nüchtern – oder (direkt) nach Mahlzeiten eingenommen werden.
Das Problem: Je stärker der Spiegel an den Chelatoren im Blut schwankt, desto mehr mobilisierte Hg-Ionen verlieren (der Theorie nach) auch wieder Ihre Bindung an den Chelator und werden irgendwo freigesetzt und machen dort neuen Schaden – ggf. bevor sie über den Urin oder Stuhl ausgeschieden werden. Hier bedarf es dann genug anderem, noch im Blut kreisendem Chelator um das Spiel der ‚heißen Kartoffel‘ zu spielen – so das die Hg-Ionen wieder, (der Theorie nach) durch die Bindungsaffinität zu den SH-Gruppen des ALA (oder DMPS bzw. DMSA) bedingt, mit diesem einen Komplex formen.
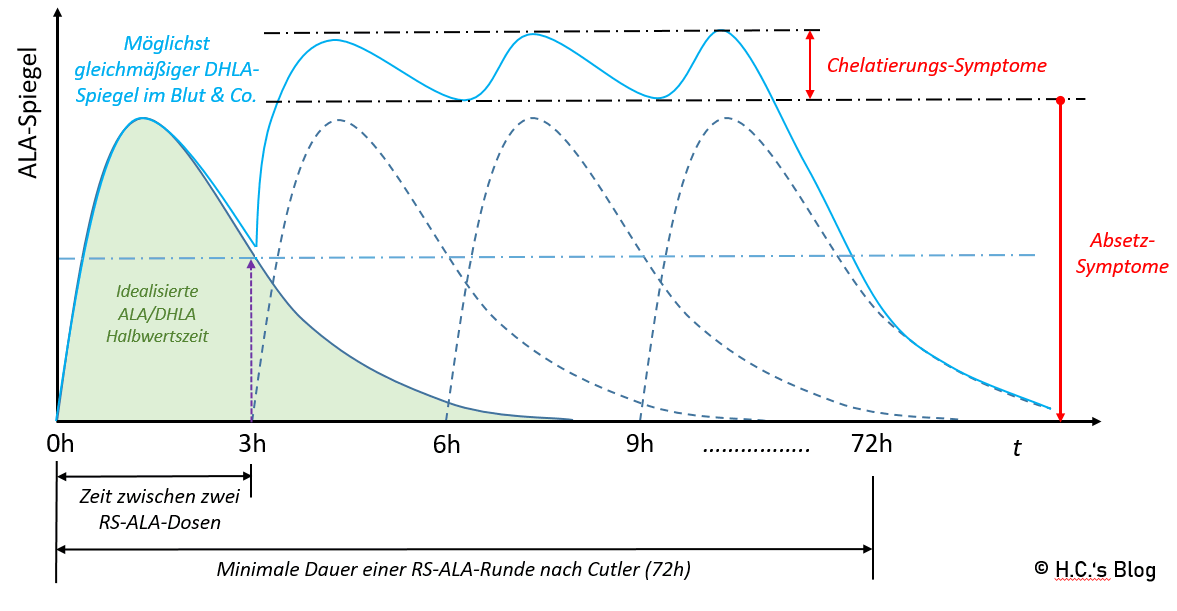
Ein abstrakt-reales Beispiel warum Cutler auf den 2-3h Intervall bei RS-Alpha-Liponsäure besteht und warum es zu ‚Entgiftungs-‚ und Absetz-Symptomen kommen kann.
Was hat Cutler anders gemacht?
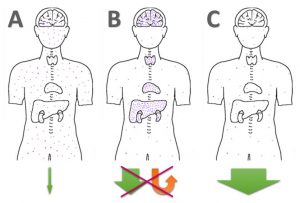
Die verschiedenen Formen der Quecksilber (Amalgam) und Schwermetall-Ausleitung: A) Gar nichts machen, B) Staub aufwirbeln und schön in Gehirn + Organe verteilen, C) effektiv binden & ausleiten. Bild: H.C. Fricke, basierend auf R. Rust Lee und der Bildquelle Pixabay, Torso
Cutlers Grundprinzip war nun die regelmäßige (orale) Einnahme der Chelatoren im Abstand deren jeweiliger Halbwertzeit über mindestens 3 und bis zu ggf. 14 Tagen.
Den Zeitraum von 3-14 Tagen hatte Cutler gewählt, weil am Ende einer Ausleitungs-‚Runde‘, der (Blut-) Serum-Spiegel von DMSA, DMPS und / oder ALA unweigerlich sinkt und es zur ‚Re-Distribution‘ des mobilisierten aber nun nicht mehr effektiv gebundenen Hg und damit den Absetz-Symptomen kommen kann. Insofern sollte eine Runde eine Minimalzeit haben. Die vorgeschlagene Maximal-Zeit ergibt sich aus einem weiteren Kompromiss, denn es können sich bei der dauerhaften Anwendung von ALA u.a. Methyl-Hg, Kupfer, Zink und andere in der Leber anreichern bzw. konzentrieren – und diese Schwermetalle kann die Leber nur in der ALA-Pause effektiv ausscheiden [6, Seite 203]. Cutler im Original zu lesen ist also durchaus sinnvoll für ein umfassendes Verständnis.
So ist dann Cutlers Methode (aus meiner Sicht) auch deutlichst besser als die Chelatoren nur unregelmäßig, bzw. 1-3 mal am Tag, einzunehmen und jedes mal eine ggf. starke Umverteilung des Hg und oft auch starke Absetz-Symptome zu riskieren (-> siehe für letzteres Vorgeben auch nebenstehendes Bild unter Buchstabe B).
Nach jeder Runde ist eine Pause von mindestens 4 Tagen sinnvoll, damit sich die Leber und andere Systeme im Körper regenerieren können und Methyl-Quecksilber, Kupfer und Cadmium aus der Leber ausgeschieden werden kann. Im Körper ist eben nichts ohne Interaktionen und Wechselwirkungen. Je besser man diese kennt bzw. abschätzen kann, desto optimaler kann eine Intervention gestaltet werden.
Noch was wichtiges zur Alpha-Liponsäure
Es gibt mehrere Varianten Alpha-Liponsäure, wobei die Halbwertzeiten der R-Varianten wohl bei (oder unter) einer Stunde liegt. Zudem ist wohl auch die Anflutung (die Kurve bis zum Maximalwert) schneller und der erreichte Spitzen-Serumswert im Blut höher. Cutler rät deswegen dringendst von R-ALA im Rahmen des Cutler-Protokolls ab. nach Cutler sollte so nur die (deutlich günstigere) RS-Alpha Liponsäure verwendet werden.
Hier zur Orientierung eine Übersicht über die am Markt verfügbaren Varianten:
- RS-Alpha Liponsäure
- R-Alpha Liponsäure
- Natrium R-Alpha Liponsäure
Anmerkung: Cutler riet auch deswegen zur Nutzung von RS-ALA, weil er und viele andere, damit (positive) Erfahrungen gesammelt hatten. So könnten R-ALA & Co. funktionieren – oder auch nicht – wobei die Halbwertzeiten jedoch angepasst werden müssten – ein Experiment, was keiner ohne Not wagt. RS/DL-Varianten (Eantiomere) verhalten sich eben biochemisch deutlich anders als die R/L Versionen.
Hinweis: In diesem Artikel – Alpha-Liponsäure Teil 2 – gehe ich weiter auf die Halbwertszeit-Thematik, Interaktionen und Problematiken ein.
Gibt es auch Kritik an Cutler in Bezug auf seine Halbwert-Zeiten?
Ja, klar.
Klar scheint zu sein, welche Metabolisierungs-Halbwertzeit die ‚ungebundenen‘ Chelatoren haben – aber anscheinend ist nicht ‚ganz‘ klar was die Halbwertzeit der ‚gebundenen‘ Chelatoren-Komplexe ist, also denen, welche eine Verbindung mit eine Hg-Ion eingegangen sind. So konnte ich in einer sehr intensiven Suche zu diesem Aspekt der Pharmakokinetik von ALA, DHLA, DMSA und DMPS nichts finden. In späteren Artikeln werde ich dann noch mal im Detail auf alle relevanten Chelatoren eingehen – zu viel für diesen Artikel. Wichtig jedoch: Die Kritiker haben keinen besseren Vorschlag, keine Daten und infusieren oft einfach weiter…
Insofern halte ich mich selber, also bei diesem Aspekt, vorerst an Cutler – denn ich sehe nicht, wo das Schadenspotential einer ‚frequent low dose chelation‘ sein sollte. Zudem ’stehe‘ ich selber nicht auf eine sehr hoch dosierte ‚Einmal-Einnahme‘ von Supplementen und / oder anderen pharmazeutischen Substanzen – wenn es dafür nicht überzeugende Gründe gibt. Einer dieser Gründe kann die gezielte Nrf2-Aktivierung sein, was im Rahmen dieses Artikels jedoch zu weit führt.
Mein Fazit
Eigentlich gibt es für mich nur nur ein Fazit, was ich hier schon ausgeführt hatte:
- a) ‚Finger weg‘ von (hoch dosierten) Infusionen mit ALA, DMPS, DMSA bei noch bestehender Belastung mit Quecksilber.
- b) ‚Finger weg‘ von sehr hoch dosierten oralen Gaben mit ALA, DMPS, DMSA bei noch bestehender Belastung mit Quecksilber.
- c) ‚Finger weg‘ von oralem oder infusiertem EDTA und Glutathion bei noch bestehender Belastung mit Quecksilber.
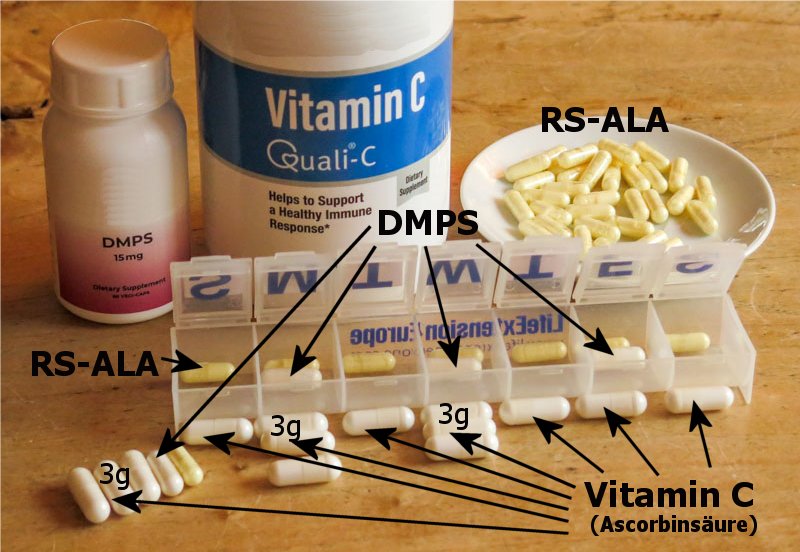
So sollten die Chelatoren dann, aus Cutlers und meiner Sicht eher niedrig dosiert, oral und im Kontext ihrer ‚Halbwertzeit‘ eingenommen werden: Optimal im regelmäßigen Takt über mehrere Tage am Stück – ohne in irgend einer Weise vom Einnahmeschema abzuweichen. Das bedeutet:
- Wecker stellen.
- Chelatoren immer dabei haben!
- Den Tag und die Mahlzeiten entsprechend planen – gleich mehr dazu!
Wird einmal die Einnahme vergessen – dann sollte (nach Cutler) besser abgebrochen werden. Zudem sollten die jeweilig gewählten Einnahme-Intervalle in einem sehr engen Zeit-Korridor eingehalten werden (max. +/- 15 Minuten, besser +/- 5 Minuten) [6]. Am optimalsten werden die Einnahme-Zeiten so gelegt, das der Chelator immer auf nüchternen Magen (vor dem Essen) eingenommen wird. Der Hintergrund: Der Chelator flutet dann immer in einer ähnlichen Zeit im Blut an – zumindest ist das mein persönlicher Schluss aus den Studien die ich dazu gelesen habe.
Wer das alles nicht glaubt – der schaut ggf. mal bei What NOT to do! – CutlerSuccessStories.com [9] – vorbei. Da gibt es einiges erschreckendes zu lesen – zu IV-Therapie mit DMSA und DMPS, Chelations-Mobilisations-Tests und den Ergebnissen anderer Protokolle, welche die Vorbereitung, Organfunktionen & Unterstützung sowie Halbwertzeiten und Pharmakokinetik nicht beachten. Gerade die Unterstützung der Leber (aber auch der Niere) und der Phase III der Entgiftung halte ich dabei für fundamental. Wer das übersieht – der tut sich keinen Gefallen und verschlimmert eventuell seinen Zustand.
Wie nun aus meiner Sicht, ganz konkret und im Detail vorgegangen werden sollte, werden ich Stück für Stück in dieser Artikelserie beschreiben – über die nächsten Monate & Jahre, je nachdem wie es meine Zeit erlaubt. Ganz wichtig vorab: Wer massive Probleme bei der anfänglichen Einnahme von Chelatoren und / oder ALA verspürt – der macht meist etwas falsch oder übersieht etwas. Oft sind dann Leber, Niere und speziell die Phase III der Entgiftung nicht richtig unterstützt. Oft fehlt es dann an Magnesium, Vitamin C, Vitamin E, Zink, Phosphatidylcholin, Mariendistel, Molybdän und anderen.
Links / Quellen
- [1] Überarbeitetes Glossar zu Begriffen der Pharmazeutik., Peter Langguth, Joachim Seydel, Angewandte Chemie. Bd. 123, Nr. 15, 2011, S. 3635–3651, doi:10.1002/ange.201100728
- [2] Biologische Halbwertszeit, Wikipedia.de, Abruf am 21.12.2019
- [3] Pharmakokinetik, Wikipedia.de, Abruf am 21.12.2019
- [4] Handbuch der Amalgamvergiftung: Diagnostik – Therapie – Recht., Max Daunderer, 1995
- [5] Durchführung, Referenzbereiche und Interpretation des DMPS-TestesEine kritische Datenanalyse, Dr. Wolfgang Bayer, Laboratorium für spektralanalytische und biologische Untersuchungen Dr. Bayer GmbH
- [6] Amalgam Illness: Diagnosis & Treatment: What You Can Do to Get Better, How Your Doctor Can Help You, Andrew Hall, Ph.D. Cutler , 1999
- [7] Comparison of R(+)-α-lipoic acid exposure after R(+)-α-lipoic acid 200 mg and 300 mg and thioctic acid 600 mg in healthy Korean male subjects, Jangsoo Yoon et al., Transl Clin Pharmacol, 2016, doi: 10.12793/tcp.2016.24.3.137
- [8] Mercury toxicity and antioxidants: Part 1: role of glutathione and alpha-lipoic acid in the treatment of mercury toxicity., Patrick L., Altern Med Rev. 2002 Dec;7(6):456-71.
- [9] What NOT to do!, CutlerSuccessStories.com, 12.12.2017
- [10] Effect of lipoic acid on biliary excretion of glutathione and metals., Gregus Z, Stein AF, Varga F, Klaassen CD, Toxicol Appl Pharmacol 1992 May;114(1):88-96, doi: 10.1016/0041-008x(92)90100-7.
- [11] Textbook of Clinical Neurology, 2nd ed., Goetz et al., Elsevier, 2003
- [12] Doctors should study their textbooks carefully. , AndyCutler, Wed, 15 Dec 2004






Neuste Kommentare