Eisen-Update Teil 5: Eisenmangel-Anämie (IDA, ACD) & Überschuss Diagnoseleitfaden + Infos zu Eisen-Supplementen & Infusionen

Der Navigationsleitfaden für Eisen-Blutwerte. Foto: H.C.
Im 5ten und letzten Teil dieses Eisen-Update soll es noch einmal praktisch werden: Ich möchte die Essenz der vorhergehenden 4 Teile zusammenfassen und einen kleinen Leitfaden für die Diagnose des Eisenstatus erstellen. Zudem möchte ich noch etwas zu Eisen-Supplementen & Infusionen schreiben, u.a. wann was in welcher Form angemessen sein könnte.
- Rekapitulation: Welche Fälle von Eisenmangel und Überschuss sind zu Unterscheiden?
- Mein Eisenmangel-Diagnoseleitfaden in der Übersicht
- Grundlagen 101: Was ist bei der Interpretation der Eisenwerte zu beachten?
- (Akut-Phase) Entzündungen
- Die Anämie aufgrund von (funktionalem) Eisen-Mangel
- Die brauchts auch: Vitamin B6, B12 und Folat
- Die Retinol und / oder Kupfer-Mangel Anämie
- Ferritin (Serum)
- Ein Coaching-Fall „aus der Praxis“
- Eisenspeicher leer – was tun?
- Die Relation von Serum-Ferritin Wert zu gespeichertem Eisen
- Zur Bioverfügbarkeit und Menge oraler Ergänzungen mit Eisen
- Orales Eisen-Ergänzung – eine gute Variante? Und wenn ja, für wen?
- Anmerkungen zur intravenösen Eisentherapie
- Potentielle Nebenwirkungen & Seiteneffekte der Eisenergänzungen: Viele
- Eisenspeicher übervoll – was tun?
Am Ende des Artikels folgt dann mein übliches Fazit.
Hinweis: Hier geht es zum Eisen-Übersichtsartikel
Inhaltsverzeichnis für den Schnellzugriff
Rekapitulation: Welche Fälle von Eisenmangel und Überschuss sind zu Unterscheiden?
Zu viel & zu wenig Eisen und beides mal Eisemangel-Anämie als Resultat: Es ist wichtig IDA und ACD zu unterscheiden! Bild generiert mit: DALL-E durch Anfrage von H.C.
Wenn es um den Eisenstatus geht, muss klar sein welche Fälle es zu unterscheiden gibt. Die Klassiker sind Eisen-Überschuss, „alles o.k.“ und Eisen-Mangel (IDA). Allerdings können bei reduzierter Eisenverfügbarkeit, egal ob eine Vorstufe von IDA oder ACD, bei noch normalen Hb-Werten, schon andere Mangelsymptome auftreten. Dieses nennt man dann Eisenmangel ohne Anämie (EoA).
Ein „funktionaler“ Mangel an Eisen (ACD) , u.a. durch chronische Entzündungen mit hohem Hepcidin, kann bei genug oder zu viel Eisen im Körper auftreten, letztere wenn es (u.a. Entzündungsbedingt) „weggesperrt“ ist. Deswegen unterscheidet man die „richtige“ Eisenmangel-Anämie (IDA) mit leeren Eisenspeichern von der Anämie chronischer Krankheiten (ACD), bei der das Eisen im Körper ausreichend bzw. sehr Üppig vorhanden ist, aber eben nicht bioverfügbar..
Der Teil 4 endete im Fazit deswegen mit folgender Auflistung der verschiedenen Fälle die aus meiner Sicht unterschieden werden sollten:
- „Alles gut“ –> Hb im gutem Bereich, Funktionseisen o.k., nicht zu wenig, nicht zu viel Speichereisen.
- Wenig Speichereisen, jedoch noch genug Funktionseisen für alle Prozesse, inkl. Häm/Hb -> Hb & Co. o.k.
- Anm.: Hier würde ich nichts machen, ggf. die Ernährung verbessern & auf Risikofaktoren schauen.
- Zu viel Speichereisen, Funktionseisen für alle Prozesse o.k. -> Hb & Co. o.k.
- Anm.: Oft zu viel Häm-Eisen (u.a. rotes Fleisch), teils genetische Defekte -> Förderung des oxidativen Stresse, Alzheimer, etc.
- (Speicher-) Eisenmangel ohne Anämie (EoA) , aber ggf. schon Auswirkungen auf einige eisenabhängige Prozesse.
- Anm.: Noch genug Funktionseisen für Häm/Hb > 12/13 g/dl. Ggf. Mangel von 500-1000 mg Eisen [1].
- Eisenmangelanämie (IDA), zu wenig Speichereisen, zu wenig Funktionseisen -> mit niedrigem Hb, MCH, MCHC, (sehr) niedrigem Serum-Ferritin.
- Anm.: Eisen abhängige Prozesse laufen eventuell suboptimal.
- Anämie chronischer Krankheiten (ACD), zu wenig Funktionseisen -> wie IDA, zudem oft chronische Entzündungen (u.a. IL-6 hoch) mit Subformen:
- a) Speichereisen (noch) o.k. -> Aber dieses Eisen ist „weggeschlossen“
- b) Zu viel Speichereisen -> zusätzlich zu a) ox-Stress durch viel (ggf. ungebundenes) Eisen.
Neu in dieser Auflistung ist der Eisenmangel ohne Anämie (EoA). Dies ist aus meiner Sicht ein diffuses Symptombild, wo von Eisen abhängige Prozesse nicht mehr optimal laufen können (z.B. Eisenmangel bedingter Haar-Ausfall), jedoch der Hb-Wert noch deutlich über 12/13 g/dl liegt. Nur mittels des (sTfR-log-) Ferritin-Indexes lässt sich aus meiner Sicht dieser Fall eindeutig von einer ausreichenden Versorgung bei Serum-Ferritin (< ~ 30-40 ng/ml) unterscheiden, da in vielen Fällen, das Serum-Ferritin durch ein niederschwelliges Entzündungsgeschehen leicht erhöht sein könnte und so z.B. Werte < 18 ng/ml als 30-40 ng/ml auf dem Laborzettel erscheinen.
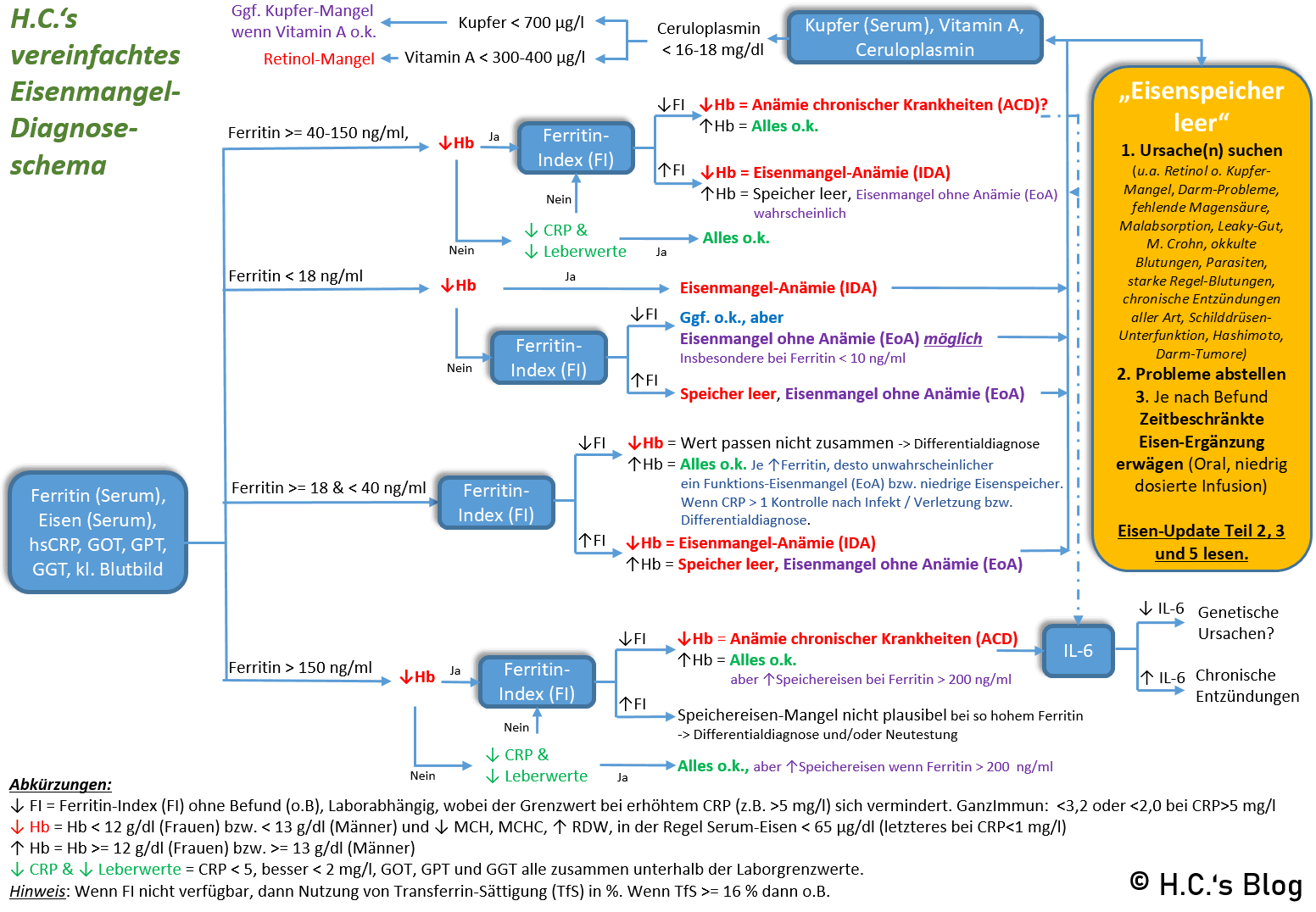
Mein Eisenmangel-Diagnoseleitfaden in der Übersicht
Für das nachfolgende Bild habe ich lange überlegt, wo der Anfang bei einer Eisenstatus-Untersuchung in Bezug auf einen Mangel (bzw. Ausschuss dessen) sein könnte. Letztendlich habe mich mich für das Serum-Ferritin entschieden, auch wenn dieses einen sehr großen (u.a. entzündungsbedingten) Graubereich hat. Man muss eben nehmen was man bekommt.
Im zweiten Schritt schaue ich auf das kleine Blutbild (u.a. Hb, MCH, MCHC, RDW) sowie das Eisen im Serum. Je nach Ferritin-Werte wird mittels CRP-Wert sowie den Leberwerten (GOT, GTP, GGT) unterschieden bzw. plausibilisiert. Ist das Eisen im Serum sehr niedrig, dann spricht das für einen (funktions-) Eisenmangel, wobei es auch entzündungsbedingt hoch sein kann, obwohl es einen Eisenmangel und ein niedriges Hb gibt. Deswegen darf Eisen nur herangezogen werden, wenn CRP < 1 mg/l ist. Sind die Leberwerte hoch, spricht das auf für etwas ungutes, wobei hier wiederum mehr Ferritin(e) in das Serum „lecken“ können, u.a. durch Zellzerstörung. Diese Werte sollte man grundsätzlich immer „mit messen“ und sie sind auch nicht teuer.
Der (sTfR-log-) Ferritin-Index liefert, falls nötig, wohl die besten Informationen zu den Eisenspeichern, also ob diese nun wirklich leer sind oder nicht. In Teil 4 dieser Artikel-Serie habe ich den Wert sowie einige Studien dazu ja im Detail vorgestellt und betrachtet. Allerdings hat diesen Wert noch nicht jedes Labor im Programm, weswegen des Backup die Transferrin-Sättigung ist, welche aber nicht zwischen (funktions-) Eisenmangel bei vollen oder leeren Speichern unterscheidet. Dann sollte man etwas Vorsichtig mit der Interpretation der Ergebnisse sein.
Je nach Status muss im Nachgang nach den Gründen für den Eisenmangel geschaut werden, wobei dies insbesondere Thema von Teil 2 und Teil 3 dieser Serie ist. Für mich ist eine Schau auf Vitamin A und Kupfer (Serum) angebracht. Stimmt da irgendwas nicht, dann auch Ceruloplasmin – oder gleich alle drei. Das geht natürlich auf den Geldbeutel, also würde ich es nicht unbedingt in der ersten Runde machen, wobei ein Check von Vitamin A bei jeder Art von Nachtblindheit, Problemen mit den Augen oder dem Immunsystem aus meiner Sicht schon angebracht ist. Kupfer (im Serum) ist dann recht günstig. In Teil 4 stehen noch ein paar weitere Infos, was Warnsignale für einen Kupfer-Mangel sein könnten, wobei das alles recht vage ist und keine qualitativen und erst erst keine quantitativen Aussagen zulässt. Also besser richtig nachschauen, wenn en Eisenmangel vermutet wird.
Wichtig: Ich gebe zu bedenken, das auch dieser Leitfaden nicht alle (Grenz-) Fälle abdeckt! B6, B12 und Folat-Mangel sind hier u.a. unberücksichtigt, wie auch genetische Ursachen, welche teils zu sehr hohen Serum-Ferritin Werten führen.
Grundlagen 101: Was ist bei der Interpretation der Eisenwerte zu beachten?
Nachfolgend noch ein paar kurze Erklärungen und Zusammenfassungen in Bezug auf die Blutwerte und das obenstehende Diagramm. Aus meiner Sicht für es 3 Stufen des „Eisenmangels“, welche unterschieden werden sollten:
- Stufe 0: Alles o.k.
- Stufe 1: Niedriges Speichereisen bzw. wenig(er) bioverfügbares Eisen durch chronische Entzündungen, (okkulte) Blutungen, verminderte Aufnahme und / oder (selten/er) Parasiten.
- Stufe 2: Eisenmangel ohne Anämie (EoA), also das Fortschreiten der Entwicklung der Stufe 1 mit Auswirkungen auf einige eisenabhängige Prozesse
- Stufe 3: Eisenmangelanämie (IDA) bzw. Anämie chronischer Entzündungen (ACD) mit niedrigen Hb-Wert (Anämie)
Gerade um 0, 1 und 2 gegeneinander abzugrenzen, erfordert den Einsatz von spezifischen Laborwerten bzw. Parametern. So berichtet Martius [1] über die nicht hämatologische Effekte des Eisenmangels (-> EoA), in Bezug auf verminderte körperliche Leistungsfähigkeit, kognitive Störungen, gestörte Thermoregulation und Fatigue – wobei gerade diese unspezifischen Symptome viele Ursachen haben können, speziell auch eine Schilddrüsen-Unterfunktion.
Ganz wichtig ist: Es muss immer der Grund für den Mangel identifiziert werden! Eisen mangelt faktisch nie „einfach so an sich“. Irgendetwas „brodelt“ im Hinter- oder Untergrund. Und es muss klar sein, was das ist, damit das Üben an der Wurzel behandelt werden kann
Hinweis: Auf eine Vielzahl von genetischen Störungen des Eisen-Metabolismus, die allerdings eher zu hohen Speichereisenwerten führen, gehe ich in diesem Artikel jedoch bis auf die Hereditäre Hämochromatose (weiter unten) nicht ein.
Grundlagen 101: (Akut-Phase) Entzündungen
Akut-Phase Entzündungen (u.a. CRP hoch), aber auch andere Entzündungen & Infekte, beeinflussen faktisch alle eisenrelevanten Werte bzw. können dies tun. Deswegen sollte immer Leberwerte und CRP gemessen werden, wenn eine initiale Eisenstatus-Diagnose erstellt werden soll.
Dies passiert deswegen, weil der Körper das Eisen in solchen Fällen als Schutzmechanismus „einsperrt“, weil Pathogene Eisen „lieben“. Dadurch sinkt das Eisen im Serum und das Ferritin (Serum) steigt. Beides repräsentiert aber nicht den Normalfall und kann in die Irre führen, wenn nicht auf solche Umstände geachtet wird.
Welche eisenrelevanten Werte bei Entzündungen „runter“ oder „hoch“ gehen, habe ich in Teil 4 dieser Serie in der Übersicht angemerkt. Grundsätzlich sind Eisen (Serum), Ferritin (Serum), Transferrin-Sättigung (TfS), Zinkprotoporphyrin (ZnPP), Retikulozyten-Hämoglobin (Ret-Hb), Hepcidin, Kupfer (Serum) und Ceruloplasmin betroffen.
Grundlagen 101: Die Anämie aufgrund von (funktionalem) Eisen-Mangel
Eine Anämie (egal ob IDA oder ACD) wegen zu wenig verfügbarem Eisen zeigt sich u.a. durch das kleine Blutbild, was eigentlich immer vorliegen sollte:
- Abfall des Hämoglobingehaltes unter < 12 (Frauen) bzw. 13 g/dl (Männer),
- MCH, MCHC unterhalb der Referenzwerte,
- in der Regel hohe RDW (Erythrozyten-Verteilungsbreite) und
- ggf. dem Absinken des Eisens (im Serum) unter 65 µg/dl, speziell bei hohem CRP.
- Zudem können auch Hämatokrit, Erythrozyten wie auch MCV noch niedrig sein.
Eine IDA oder ACD ist jedoch die 2te Stufe der Eisenmangelsymptomatik. Vorher, also in Stufe 1, kommt der Eisenmangel ohne Anämie (EoA). Liegt der Hb-Wert jedoch bei 10 g/dl oder weniger, dann sollte unbedingt korrekt diagnostiziert werden ob eine IDA oder ACD vor liegt und was die ursächlichen Ursachen dafür sind, denn wenn Eisen fehlt oder nicht verfügbar ist, hat das Gründe.
Ein niedriger Hb-Wert kann jedoch auch andere Ursachen haben, wie z.B. eine Nierenfunktionsstörung bzw. CKD (Chronic Kidney Disease), wobei dann auch meist die Erythrozyten niedrig sind. Hier ist dann meist wenig EPO da, was für die Steuerung der Hämoglobinbildung im Knochenmark wichtig ist. Deswegen war EPO auch als Dopingmittel beliebt, weil durch das „Extra“ mehr Erythrozyten -> in Folge mehr Hämoglobin gebildet wurde, was dann den (extra) Sauerstoff-Transport befördert.
Grundlagen 101: Die Retinol und / oder Kupfer-Mangel Anämie
Es „kann“ auch sein, das eine Anämie, die wie eine Eisen-Mangel Anämie „aussieht“, durch zu wenig Kupfer bedingt ist, ggf. auch durch zu wenig Vitamin A. Beide sind wichtig für das Ferroxidase-Enzym (FOX) und ohne dies kein Eisentransport, was sich u.a. an einem niedrigen Ceruloplasmin. zeigen sollte. Da kein anderer Eisenwert auf zu wenig Retinol bzw. Kupfer hinweist, messe ich bei Verdacht immer:
- Vitamin A (als Retinol) im Serum
- Kupfer (im Serum) sowie optional, aber speziell wenn Kupfer und/oder Vitamin A niedrig sin auch
- Ceruloplasmin
Muss nicht sein, ist in der Regel wohl auch nicht oder nur selten so – aber es „kann“ sein und ansonsten sucht man sich „irre“ nach dem Grund für den Mangel an bioverfügbaren Eisen und findet nix. Also bei Verdacht und speziell bei Veganern, (strikten) Vegetariern ohne genug Gemüse, Mangelernährung, Untergewicht und Augenproblemen unbedingt testen!
Grundlagen 101: Die brauchts auch: Vitamin B6, B12 und Folat
Irreguläre Werte bei MCH, MCHC, MCV und Hb können auch von einem Mangel an B6, B12 und / oder Folat stammen. Die einfachste Variante dies zu prüfen ist Homocystein zu messen. Dieses sollte optimalerweise <8 sein, maximal 10 µmol/l. Sinnvoller Weise wird auch noch das B12 im Serum gemessen. Werte sollten hier mindestens 400, eher 600 pg/ml sein um einen deutlichen B12-Mangel als Ursache auszuschließen. Ich selber strebe bei B12 als Minimum >> 800 an. Folat und B6 zu messen ist aus meiner Sicht nicht sinnvoll, da hier oft nicht zwischen den verschiedenen Stoffwechsel-aktiven (u.a. P5P) und nicht aktiven Varianten unterschieden wird.
Grundlagen 101: Ferritin (Serum)
Wie in den vorhergehenden Artikeln ist Ferritin (im Serum) ein ganz guter Marker für den Eisen-Speicherstatus, leider mit einem großen Graubereich, der noch größer wird, wenn (Akut-Phase) Entzündungen vorliegen!
Werte unter 15-18 ng/ml werden klar mit einem sehr wahrscheinlichen Mangel an Speichereisen bzw. EoA assoziiert. Messwerte zwischen 18-30 ng/ml sind in einem Graubereich, aber es kann auch ein Eisenmangel ohne Anämie (EoA) bzw. ein realer Eisenmangel (IDA) vorliegen – speziell wenn (niederschwellige) Entzündungen das Serum-Ferritin erhöhen. Zwar sollen diffuse EoA-Symptome wie Haarausfall nach Angaben des Labors GanzImmun auch bis 70 ng/ml auftreten, hier vermute ich jedoch eher Probleme in Richtung ACD, wo das Eisen weggesperrt ist, oder Ferritin-Werte, welche wegen Entzündungen (deutlich) erhöht sind.
Martius [1] schreibt in einer aus meiner Sicht brauchbaren Zusammenfassung zu Serum-Ferritin-Werten (ohne Entzündungen) folgendes:
- <15 ng/ml: Hohe Spezifität entleerter Eisenspeicher, aber kein Beweis für einen Mangel an Funktionseisen (also das der aktuelle Bedarf nicht gedeckt werden kann).
- 15–30 ng/ml: Korrespondiert mit leeren oder knappen Speichern.
- 30–50 ng/ml: Grauzone. In der Regel o.k., wobei es bis 50 ng/ml, meist bei leicht erhöhten CRP-Werten, auch mal, im Einzelfall, zu wenig sein kann.
- >50-100 ng/ml: Genügende Eisenreserve.
- >100 ng/ml: Zu viel Eisen (bei CRP < 0,5), wobei es bei > 150 ng/ml wirklich zu viel ist.
Diese Angaben korrelieren mit den von mir betrachteten Studien zu Ferritin (im Serum) sehr gut.
Grundlagen 101: Ein Coaching-Fall „aus der Praxis“
Just als ich diesen 5ten Teil schrieb konnte ich meine nun erweiterten Erkenntnisse an einem praktischen Beispiel anwenden. Ich bekam die Bitte, über einige Blutwerte einer 52 jährigen Frau zu schauen. Dazu gab es dann 4 Blutwertanalyen von verschiedenen Labors mit wiederum verschiedenen Blutwerten, die alle in einem 4-Wochen Zeitraum lagen. Nicht optimal, aber eben die Realität. Und das was ich hier schreibe soll ja Realitätstauglich sein.
Damit alles nachvollzogen werden kann, präsentiere ich in diesem Abschnitt auch die Scans der wichtigsten eisenrelevanten Ausschnitte aus den Blutwerten, welche ich freundlicher Weise hier verwenden darf.
Den Anfang macht das große Blutbild, leider ohne Serum-Ferritin, ohne CRP – dafür jedoch mit Schilddrüsen und Leberwerten. Was war auffällig?
- Hb genau 12 g/dl, also die „Kippe“ zur Anämie, obwohl es der Klientin noch nach eigenen Aussagen gut ging.
- MCH niedrig, MCHC stark erniedrig, RDW stark erhöht – die klassische Eisenmangel-Konstellation
- Erythrozyten niedrig was zur Anämie passt.
- Monozyten erhöht, was erst einmal gegen Kupfer-Mangel aber ggf. auch für ein Infekt-geschehen spricht
- MCV, Hk noch o.k., also wohl noch „keine Katastrophe“. Immerhin ist Hb „noch“ 12 g/dl.
Die klinische Chemie zeigt:
- Eisen ist mit 63 µg/dl grenzwertig niedrig. Allerdings ist die Entzündungs-Situation (insbesondere CRP) nicht bekannt, welche Ferritin (deutlich) senken kann. Insofern ist dieser Wert mit Vorsicht zu interpretieren.
- Anm: Das Labor gibt zwar 50 µg/dl als Grenzwert an, dieser Wert ist jedoch „irre“ niedrig. Die Studienlage und auch GanzImmun geben 65 µg/dl als unteren Grenzwert an.
- Die Leberwerte scheinen gut zu sein.
Die Endokrinologie zeigt ganz klar, das eine Schilddrüsen-Unterfunktion vorliegt, egal, was die viel zu niedrigen Referenzwerte angeben. fT3 mit 2,77 pg/ml und fT4 mit 0,81 nd/dl sind nicht gut. Hohes Cholesterin und Triglyceride bestätigen dies. Die Schilddrüse (bzw. T3/4) braucht jedoch auch Eisen und ohne Schilddrüse funktioniert die Eisenaufnahme (u.a. Magensäure-Produktion) und ggf. auch die Ceruloplasmin-Bildung nicht richtig. In jedem Fall ist die Schilddrüsen-Situation eine extra Baustelle, wobei es eine Eisenmangel-Situation, soweit diese vorliegen sollte, nicht besser macht.
Anhand dieser Werte ist allerdings keine Diagnose außer ‚an der Grenze zur Anämie‘ möglich, da CRP und Ferritin nicht gemessen wurden. Es mangelt scheinbar an (Funktions-) Eisen, es ist jedoch nicht klar, ob wirklich zu wenig in den Speichern ist, oder ob es entzündungsbedingt in den (vollen) Speichern zurückgehalten wird.
Dann wurde zwei mal in Bezug auf den Eisen-Status und die Schilddrüse nachgeliefert. Folgendes ist zu sehen:
- Ferritin 8 ng/ml also „nichts“ bei CRP von 3 mg/l, was ja tendenziell Ferritin sogar erhöht.
- Transferrin bei 341 mg/dl, ohne Angabe der Sättigung. Die Sättigung (TfS) könnte bei einem angenommenem Eisen von 70-80 µg/dl irgendwo bei ca. 15-17, ggf. 18% liegen. Das wäre in der Nähe des GanzImmun Grenzwertes von 16%.
- Ein anderes mal Ferritin bei 13 ng/dl und TfS bei 17%, wobei Eisen (im Serum) 78 µg/dl ist. Ein hohes CRP supprimiert den Eisen-Wert und erhöht den Ferritin-Wert und dennoch bleiben die Werte schwach.
Egal wie man diese Werte dreht: Aus meiner Sicht ganz klar ein (fortgeschrittener) Speichereisenmangel, aber noch keine ausgeprägte Eisenmangelanämie (IDA). Aber warum?
Es scheint sich abzuzeichnen, das die Situation der Schilddrüse ggf. kritischer ist: die MAK-Antikörper sind erhöht. TSH ist nur leicht erhöht, was mir zeigt, dass das System „mehr will“, aber a) nicht bekommt und b) ggf. die Hypophyse sich zurückhält, weil irgendwo ein Entzündungsgeschehen im Körper stattfindet, worauf auch CRP und MAK hinweisen. Ein Ultraschall der Schilddrüse wäre der nächste Schritt um die Größe festzustellen und zu checken, ob das Organ bzw. das Gewebe o.k. ist. Vorher sollte in keinem Fall mit Jod herumgespielt werden. Die Schilddrüsenthematik würde ich hier in jedem Fall zeitnah abklären, Hashimoto liegt für mich nahe und besser wird es nicht werden…
Bei dem Warum steht immer die Frage von Retinol (Vitamin A) und Kupfer im Raum. Diese Werte sind aber eher „Satt“ im Gutem mit eher sehr üppigem Vitamin A. Auffällig ist jedoch:
- Vitamin D (25-OH) ist mit fast 90 ng/dl sehr hoch und wird wohl etwas üppig ergänzt. Das aktive 1,25-OH D3 ist jedoch im normwertig und klar im gemäßigten Bereich. Da die Eisen-Speicher leer sind, kann das Immun-Suppressive D3 in diesen Dosen über Senkung von Hepcidin und Förderung von Ferroportin keinen weiteren Nutzen im Kontext Eisen-Stoffwechsel mehr generieren.
- B12, Magnesium und Selen sind (eher) niedrig, wobei die Werte für Menschen ohne Ergänzung nicht unnormal sind. Ein Serum-B12 mit 339 pg/ml spricht jedoch klar für einen Mangel.
- Homocystein ist noch o.k., so das es noch keinen akuten B12/B6/Folat-Mangel zu geben scheint.
- Zink ist sehr gut und wird ggf. ergänzt.
- Gesamteiweiß bei 7,0 g dl, was für mich im o.k.-Bereich ist.
Auf Basis der Daten würde ich nicht davon ausgehen, das der Eisenmangel auf Basis einer Malabsorption durch zu wenig Magensäure vorliegt. Da Progesteron sehr niedrig war müsste man die Klientin fragen, wie es mit der Intensität der Regel-Blutung aussieht, soweit diese noch besteht. Progesteron könnte sinnvollerweise auch bioidentisch ergänzt werden.
Wenn keine „offensichtlichen“ Darmproblematiken vorliegen und parallel die Schilddrüsen-Situation geklärt wird, sollten ggf. orale Eisen-Supplemente erwogen werden um die Speicher zu füllen, z.B. 15 mg Eisen-Bisglycinat / Tag zusammen mit Betain HCL oder Ascorbinsäure min. 1h vor der Mahlzeit. In jedem Fall ist es wichtig die Schilddrüsenwerte zu verbessern, weil auch dies mit dem Eisen-Metabolismus und der Blutbildung interagiert.
Wenn die Eisenverluste nicht auf die Schilddrüse und Regelblutung zurückzuführen sind würde ich noch folgendes Messen:
- Ggf. den (sTfR-log-) Ferritin-Index um einen Überblick über die Speicher-Situtation (Füllstand) zu bekommen.
- Ceruloplasmin -> check ob das Kupfer auch „ankommt“ -> Ferroixdase (FOX)-Akitivität
- IL-6 -> Check ob irgendwelche chronische / systemische Entzündungen vorliegen, u.a. da auch CRP erhöht war.
- Falls sich später nichts bessert, ggf. Zonulin, Alpha-1-Antitrypsin in Bezug auf Leaky Gut und sCD14 in Bezug auf LPS -> Details im Eisen-Update Teil 3.
Ist IL-6 erhöht, dann beginnt die Suche erst richtig, wobei nie ausgeschlossen werden kann, das es auch Parasiten + okkulte Blutverluste gibt. Für mich am plausibelsten wäre auf Basis der Schilddrüsen-Werte jedoch eine beginnende Hashimoto-Erkrankung. Hier könnten Entzündungsschübe über Hepcidin die Eisenaufnahme „abgewürgt haben“, bis es zur aktuellen Mangelproblematik kam, welche sich ggf. über große Ab- oder Regelblutungen verschärft. Um diesen Vermutungen nachzugehen braucht es jedoch gute Anamnese zusammen mit dem Klienten, was in diesem Fall nicht „mein Part“ war.
Eisenspeicher leer – was tun?
Was bei niedrigen funktionalem bzw. bioverfügbarem Eisen bei noch vollen Speichern (ACD) zu tun ist bzw. getan werden könnte habe ich bereits in Teil 2 dieser Serie beschrieben. Dem kann ich nichts weiter hinzufügen.
Der Frage was bei einem realem Speicher-Eisenmangel getan werden kann, also insbesondere orale Ergänzungen sowie Infusionen, und welche Dosierungen angemessen sein könnten habe ich bereit in allgemeinen Eisen-Artikel beleuchtet. Hier möchte ich die Thema der Dosierung, der Nebenwirkungen und die Fälle anspreche bei denen ich sehr vorsichtig mit oralen Ergänzungen sein würde.
Die Relation von Serum-Ferritin Wert zu gespeichertem Eisen
Wenn von „Speicher“ Auffüllen gesprochen wird, ist interessant zu wissen wie viel Speichereisen 1 ng/ml Serum-Ferritin repräsentiert, wobei diese Korrelation sicherlich nur ungefähr und vor allem auch nicht linear sein dürfte. Das Labor GanzImmun [2] schreibt ohne direkten Verweis auf eine Quelle:
„1 ng/ml Ferritin entspricht ca. 8 -10 mg Speichereisen“
Dieses geht jedoch mit anderen Angaben überein [4], wobei Martius 10 mg pro 1 ng/ml Ferritin angibt [1].
Wenn ich nun annehme das bei einem Serum-Ferritin von 20 ng/ml die Eisenspeicher ziemlich leer sind, 60 ng/ml jedoch ein sicher Wert ist, weil bereits mehr als 100 ng/ml nach Studienlage auch nicht erstrebenswert erscheinen, dann ergeben sich daraus bei einen Ferritin-Wert von 10 ng/ml: (70 ng/ml – 10 ng/ml) * (10 mg / 1 ng/ml) = ca. 500 mg die an „Netto-Eisen“ fehlen.
Diese 500 mg sind bei Eisen-Infusionen schnell erreicht, weil hier das Eisen zu 100% zur Verfügung steht. Deswegen würde ich auch bei nachgewiesenem Speichereisen-Mangel nicht mehr als 5 * 100 mg Eisen in zügiger Folge nacheinander (also ca. 1 mal pro Woche) verabreichen lassen. Danach sollte nach einer Verweildauer die Eise-Werte überprüft werden. Sind diese nicht viel Besser, liegt (wahrscheinlich auch) ein anderweitiges Problem vor.
Hinweis: Beachtet werden sollte für Blutwertbestimmungen, das 100 ml Blut mit einem Hk von 0,35 L/L ca. 35 mg Eisen enthalten.
Zur Bioverfügbarkeit und Menge oraler Ergänzungen mit Eisen
Martius [1] schreibt, das bei realem Eisenmangel (ohne Begleiterkrankung) die intestinale Eisenresorption maximal stimuliert ist und anstelle der üblichen 10% nun 20% bis 40% des oral zugeführten Eisens aufgenommen werden.
Wenn zusätzlich eine gut bioverfügbare Form genutzt wird, wie Eisen-Bisglycinat, dann sollte die 10, 20 ggf. 40% auch real erreichbar sein. Dies speziell, wenn das Eisen-Supplement 1-2 Stunden vor der Mahlzeit mit zusätzlicher Ascorbinsäure (oder alternativ Betain HCL) eingenommen wird, was den PH-Wert im Magen senkt und die Aufnahme noch einmal verbessert, da gleichzeitig keine anderen Mineralien oder Spurenelement mit den Transportern (u.a. DMT-1) konkurrieren.
Das bedeutet für mich, das von einem 15 mg Supplement 1,5-6 mg „Netto-Eisen“ im Körper ankommen könnten, wenn z.B. ein hohes Hepcidin bzw. chronische Entzündungen oder Parasiten im Darm dieses nicht verhindern. Zu wenig Magensäure sollte durch die Ascorbinsäure bzw. Betain HCL kompensiert werden, soweit Magensäureblocker und Protonenpumpen-Inhibitoren abgesetzt werden. Diese Medikamente haben sowieso kaum eine sinnvolle Funktion, lösen kein Problem und behandeln nur Symptome.
Gleichzeitig gibt es pro Tag einen Eisenverlust bzw. Verbrauch von 1-2 mg und natürlich Umstandsbedingt (u.a. Schwangerschaft, Stillzeit) mehr. Bei meiner Berechnung gehe ich davon aus, dass das über die Nahrung zugeführte Eisen ungefähr diesen Verlust (bzw. 50-75% davon) deckt, aber nicht für den Aufbau von neuen Reserven reicht. Zudem gehe ich bei höheren Dosierungen pro Tag von einem geringeren Grenznutzen aus (-> ala 40/30/20%).
Das ergibt folgende Beispielrechnungen:
- 1 * 15 mg/Tag = 1,5-6 mg Netto – 0,5 „Verbrauch“ = 1-5,5 mg Überschuss
- 2 * 15 mg/Tag = 3-9 mg Netto – 0,5 „Verbrauch“ = 2,5-8,5 mg Überschuss
- 3* 15 mg/Tag = 4,5-9 mg Netto – 0,5 „Verbrauch“ = 4-8,5 mg Überschuss
Meint: Es kann durchaus 100 Tage (3 Monate) dauern um die Eisenspeicher relevant anzuheben, wobei mit einer 15 mg Kapsel am Tag bei einem wirklichen Mangel an Eisen nicht so viel zu erwarten ist, da die Stimulation der Eisenresorption sukzessive nachlassen dürfte.
Orales Eisen-Ergänzung – eine gute Variante? Und wenn ja, für wen?
Aus meiner Sicht Ja, wenn das Eisen wirklich, wirklich fehlt. Zudem ist orales Eisen günstig und lässt sich gut dosieren. In keinem Fall jedoch würde ich eine chronische, also Langzeit, Eisentherapie ohne Kontrollen unterstützen und auch keine bei komplett normalen Eisenwerten >= 50 ng/ml. Martius [1] schreibt dazu:
„Für Eisengaben bei Ferritinwerten >50 mg/l gibt es keine rationale Evidenz.“
sowie
„Eine Langzeittherapie bei normalen oder hochnormalen Ferritinwerten ohne funktionelle Eiseneinbaustörung hat keine rationale Basis und ist langfristig potentiell gefährlich.“
Diesen Aussagen stimme ich zu. Weiterhin sollte ausgeschlossen sein (-> Kontraindikation), das eine chronische Darmentzündung (u.a. Morbus Crohn, Colitis Ulcera) oder anderweitige kritische Darmerkrankungen (u.a. Darm-Tumore, Parasiten) vorliegen. In diesen Fällen kann ggf. eine niedrig dosierte Infusion hilfreicher sein. Ansonsten sollten bei Nebenwirkungen bzw. Unverträglichkeiten im Zusammenhang mit der Eisen-Ergänzung alternative erwogen werden bzw. wenn diese auch nach 4-8 Wochen Nicht „anschlägt“.
Martius [1] schlägt eine einschleichende Dosierung mit 80–100 mg in der ersten Woche, dann erst Erhöhung auf die „volle Dosis“ von 200 mg (pro Woche) vor. Das wäre 1 * 15 mg pro Tag in der ersten Woche und 2 * 15 mg pro Tag ab Woche zwei. Gibt es in der ersten Woche Probleme, sollte geprüft werden, ob dies ggf. an der Ascorbinsäure (z.B. 1 g pro 1 Kapsel Eisen) oder Betain HCL liegt. Ist das orale Eisen der Auslöser, sollte geschaut werden ob auch Eisen-Bisglycinat verwendet wird, wenn ja, dann ggf. auch eine andere Form oder Marke wechseln.
Bei oraler Substitution würde ich dies nach 4 Wochen tun. Steigt das Serum-Ferritin, insb. auch das Hb nicht an, muss dies eine Reevaluation auslösen: Sind z.B. die persistierenden Verluste unterschätzt? Gibt es [1]:
- eisenbindende oder die Eisenaufnahme unterdrückende Nahrungsbestandteile -> Milch, Calciumhaltiges?
- Medikamentöse Interferenzen, ggf. auch andere Supplemente (z.B. Hochdosis-Zink) die interferieren?
- Tropische Sprue -> Malabsorption?
- H. pylori Besiedelung?
- Autoimmungastritis? Morbus Crohn, Colitis Ulcera, Darm-Tumore?
- „Compliance“ -> Also wirklich alles eingenommen, wie geplant?
- Parasiten mit starkem Eisenverlust?
- (Okkulte) Blutungen, insb. starke Regelblutungen?
Ansonsten bitte ich im Teil 3 dieser Serie nachzulesen, dort habe ich noch zusätzliches zum Thema geschrieben.
Anmerkungen zur intravenösen Eisentherapie
Eiseninfusionen haben bis heute einen schlechten ruf, da es schwere Zwischenfälle nach parenteraler Gabe von hochmolekularem Eisendextran gab. Das hat die ältere Ärztegeneration wohl sehr geprägt. Heutige Präparate sind da deutlich besser, wobei es auch hier zu differenzieren gilt. In meinem allgemeinen Eisen-Artikel hatte ich Eisen-Sucrose (Eisen-Saccharat) als aktuell gängigste Form ausgemacht hatte, welche u.a. auch häufig bei Patienten mit chronischer Nierenerkrankung verwendet wird.
Da nur Therapeuten Eisen-Infusionen verabreichen dürfen sollte zwingend eine klare Indikation bestehen. Bei eier EoA ist eine Indikation z.B. die dokumentierte Unverträglichkeit oder die Malabsorption. Die Leitlinien der European Crohn’s and Colitis Organization empfehlen u.a. die intravenöse Eisenzufuhr als Hauptbehandlung für CED-Patienten und als Erstbehandlung bei Hämoglobinwerten (Hb) < 10 g/dL. Eine weitere Indikation für intravenöses Eisen ist die aktive Phase einer Erkrankung, da systemische bzw. chronische Entzündungen die Eisenaufnahme im Darm beeinträchtigen. [5]
Ich selber würde Infusionen nur im Bereich von 100 mg pro Einzelgabe / Termin geben wollen, sowie im Nachgang noch Vitamin C mit 7,5 g. Mehr habe ich in meinem allgemeinen Eisen-Artikel dazu geschrieben.
Eine Kontrolle des Ferritinspiegels bei bzw. nach Infusionen ist nach Martius [1] erst nach 8–12 Wochen sinnvoll, da in den ersten Wochen nach Infusion ein vorübergehender starker Anstieg des Ferritin im Serum erfolgt, der in diesem Fall nicht mit der Menge des Speichereisens korreliert. Allei Einschränkungen zum Ferritin-Sert im Serum gelten dabei natürlich weiter.
Potentielle Nebenwirkungen & Seiteneffekte der Eisenergänzungen: Viele
Je nach Dosis und Art können insbesondere orale Gaben von Eisen mit zusätzlichem oxidativer Stress, systemischen und lokal-intestinalen Entzündungen, Dysbiosen, karzinogenen Prozessen und gastrointestinalen Nebenwirkungen verbunden sein. Ungebundenes Eisen führt dabei zu einer Überlastung des Gewebes und zu weiteren Schäden durch die Bildung reaktiver Sauerstoffspezies (ROS) über die Fenton- oder Haber-Weiss-Reaktion. In der Folge kommt es zu Lipid- und Aminosäureperoxidation und DNA-Schäden, die zum Zelltod führen. [5]
Die Eisentoxizität tritt auf, weil die Kapazität der eisenbindenden Proteine eingeschränkt ist. Deswegen unterstütze ich nur nur geringe Einzeldosierungen bei den oralen Supplementen bzw. max. 100 mg als Fe3+ Eisen bei Infusionen. Die Toxizität von Eisen ist auf zwei unterschiedliche Eigenschaften des Metalls zurückzuführen:
- a) die Fähigkeit, freie Radikale zu erzeugen, und
- b) seine Funktion als wesentlicher Wachstumsfaktor für fast alle pathogenen Bakterien, Pilze und Protozoen sowie für alle neoplastischen Zellen.
Es ist auch erwähnenswert, dass ein Überschuss an Eisen in der Nahrung (bzw. durch Supplemente) die Aufnahme anderer zweiwertiger Metalle beeinträchtigen kann. Bei Mäusen und Ratten beispielsweise trug eine hohe Eisenaufnahme mit der Nahrung zu Kupfermangel bei. Das hört sich jetzt alles dramatisch an, sollte in Bezug auf 15 mg Eisen-Bisglycinat aber nicht zu stark erschrecken. Genau deswegen soll das Eisen auch im Abstand zu den Mahlzeiten eingenommen werden!
Eine Eisenüberladung erhöht das nicht an Transferrin gebundene Eisen. Ungebundenes Eisen ist besonders gefährlich, da es beim Wechsel zwischen den beiden Formen Fe2+ und Fe3+ leicht Elektronen aufnimmt und abgibt, was zur Bildung freier Radikale (ROS) führt. Da der Dünndarm der wichtigste Ort für die Eisenaufnahme und -regulierung ist, betreffen die ROS-erzeugenden Reaktionen in erster Linie diesen Teil des Gastrointestinaltrakts. Das ist der Grund, warum ich auch nicht jeden Tag rotes Fleisch essen würde und Ideen wie einer Carnivore-Ernährung nicht folge nkann.
Eine (hohe bzw. unnötige) Eisenergänzung kann nachteilige Auswirkungen auf den Magen-Darm-Trakt haben, vor allem auf die intestinale Mikrobiota. Die Menge an verfügbarem „freiem Eisen“ im Darm ist in der Regel deutlich niedriger als der optimale Wert, der für das ordnungsgemäße Funktionieren und die Replikation von Bakterienzellen erforderlich ist. Einige pathogene Bakterien wie Salmonellen oder der pathogene Stamm von Escherichia coli sind mit Siderophoren ausgestattet, extrazellulären Eisenchelatoren, die es den Bakterien ermöglichen, dreiwertiges Eisen (Fe3+) aus Ferritin und Transferrin zu binden. Interessanter weise benötigen positiv wirkende Bakterien wie die Gattungen Lactobacillus und Bifidobacterium keinen hohen Anteil an Eisen, um zu wachsen und sich auszubreiten, wobei Lactobacillus plantarum die Eisenabsorption im Darm von Frauen mit Eisenmangel erhöhte. [5]
Grundsätzlich lässt sich auf Basis der Studienlage wohl sagen, das nach oder während einer oralen Eisensupplementierung die Menge an nützlichen Mikroben abnimmt und gleichzeitig die Menge an schädlichen Mikroben zunimmt [5].
Zu bedenken ist, das etwa 90% des Eisen im Darm nicht absorbiert wird und dort verbleibt und Nebenwirkungen wie Gastroduodenitis, Übelkeit, Blähungen, Erbrechen, Dyspepsie, Verstopfung, Durchfall, Unterleibsschmerzen oder Dunkelfärbung des Stuhls verursachen kann, wobei dies bis ggf. 20% der Nutzer treffen kann, wobei diese Zahlen eher bei höheren Dosierungen als 15 mg/Einzeldosis und ungünstigen Formen wie Eisen-Sulfat auftreten. Gerade bei bestehender Colitis oder anderen entzündlichen Darmerkrankungen kann eine Infusion auch Vorteile haben. Ich würde hier mit Vitamin E und C ergänzen, ggf, auch Papain und Bromelain um Seiteneffekte zu minimieren. Butyrate (Buttersäure) kann zudem helfen die Darmbarriere zu verbessern, damit LPS nicht in das Blut gelangen können. In Teil 2 habe ich eine entsprechende Liste an Nahrungsergänzungen für den Darm verlinkt. Alternativ sind diese im Magen- und Darm-Artikel Teil 1 angegeben.
Festzuhalten ist also: Die orale Eisenergänzung aktiviert die ROS-Produktion gleichzeitig im Darmlumen und in den Enterozyten. Dies kann (auf die Dauer) die Integrität der Darmwand schädigen und selber das Leaky-Gut-Syndrom zur Folge haben. Deswegen ist Mäßigung angesagt – also aus meiner Sicht – oder eben auch, bei Indikation, eine niedrig dosierte Infusion. Denn die erhöhte Permeabilität der Darmwand führt zum Übergang von Metaboliten und bakteriellen Toxinen in das Blut, was zu einer Endotoxämie führt und zu einer systemischen Entzündung beiträgt. Dies kann schlussendlich viele klinischen Symptome verschlimmern. Eisen im Darmlumen aktiviert zudem direkt den NF-κB-Signalweg und stimuliert die Expression von proinflammatorischen Zytokinen und der iNOS. Dies ist der Grund, warum die orale Verabreichung von Eisen bei entzündlichen Darmerkrankungen (IBD) nicht empfohlen wird. Das überschüssige Eisen wird hier im Dickdarm zu einem wesentlichen Wachstumsfaktor für fast alle pathogenen Bakterien, Pilze und Protozoen sowie für alle neoplastischen Zellen, was zudem noch die Zahl der nützlichen Mikroben reduziert. [5] Das braucht keiner.
Eisenspeicher übervoll – was tun?
Für mich sind Serum-Ferritin Werte > 100 ng/ml bei normalem CRP (< 0,5) nicht erstrebenswert. Spätestens ab Werten von >= 150 ng/ml (CRP <0,5) würde ich (regelmäßig) Blutspenden oder einen Aderlass beim Arzt durchführen.
Zuerst kann jedoch Fleisch (Häm-Eisen) reduziert bzw. mal 8 Wochen ausgesetzt werden. Zudem können die Hinweise in meinem Eisen-Artikel beachtet werden, wie z.B. Curcumin einnehmen und zudem z.B. Quercetin bei eisenreichen Mahlzeiten zuführen.
Bei einer Transferrin-Sättigung von >= 40-45% und einem dreistelligem Serum-Ferritin, ggf. auch hohen Hb-Werten kann auch eine Hereditäre Hämochromatose, eine Mutation in den HFE-Genen, vorkommen, die zu einer Eisenakkumulation führt. Allerdings gibt es hier eine größere Anzahl von Problem-Konstellationen sowie verschiedene Ausprägungen.
Mein Fazit
Wow! Das war eine lange Reise durch die Eisen-Thematik bis zu diesem Fazit. Ich hoffe das jemand mir folgen konnte und einen Gesundheits-Gewinn aus dieser Serie ziehen kann. In jedem Fall bin ich bisher in keinen Mikronährstoff so tief eingestiegen wie in Eisen, wobei ich viele Dinge und auch die Erbkrankheiten „außen vor“ gelassen habe. Mehr habe ich nach diesem Marathon erst einmal nicht über Eisen zu sagen 🙂
Anmerken möchte ich noch, das Ihr euch von der Sektion der Nebenwirkungen nicht abschrecken lasst. Sie ist natürlich ein starkes Argument für Infusionen, wenn diese Angezeigt sind. Allerdings kann ich auch sagen, das 15 mg Eisen-Bisglycinat, u.a. Ferrochel, zusammen mit Ascorbinsäure, in der Regel sehr gut vertragen werden und bisher keine mir bekannten Probleme gemacht haben. Im Eisen-Artikel habe ich einige potenzielle Produkte verlinkt, wobei ch iselber Albion Ferrochel-Eisen (Eisen-Bisglycinat) beorzugen würde und das von:
- Bluebonnet (18 mg, 90 pflanzliche Kapseln) – ohne für mich bedenkliche Zusatzstoffe
Relevant ist am Ende jedoch die Verträglichkeit, wobei ich das Produkt von Bluebonnet zusammen mit 1 g Ascorbinsäure, also ungepuffertem Vitamin C, einnehmen würde.
- Lake Avenue Nutrition 1000 mg, 360 Kapseln in der Dose mit Marken-Ascorbinsäure (Quali-C), was in Schottland produziert wird. – ohne jegliche Zusatzstoffe
- Hinweis: Im Zweifelsfall verwende ich dieses Vitamin C – aus Fermentation von Mais. Besser geht aus meiner Sicht kaum. Kein China-Krams!
- Cal. Gold Nutrition 1000 mg 240 Kapseln in der Dose, nach Herstellerangaben mit Ascorbinsäure pharmazeutischer Qualität – ohne Siliziumdioxid
- Hinweis: Bisher keine Probleme bekannt, sehr gutes Preis-Leistungsverhältniss.
Das Eisen + das Vitamin C müssen vor bzw. zwischen den Mahlzeiten eingenommen werden. Optimalerweise 1-2 h Abstand zu den Mahlzeiten. Bei sensitiven bzw. Menschen mit Leake-Gut würde ich es eher zwischen Frühstück und Mittag bzw. Mittag und Abendessen versuchen, jedoch nicht vor dem Frühstück. Ich selber würde nie mehr als eine Kapsel Eisen pro Einnahme nutzen und maximal 2 pro Tag. Die Dosierung sollte von den Blutwerten, Symptomen und Ursachen abhängig gemacht werden. In jedem Fall ist das Bisglycinat auch bei Problemen it dem Darm deutlich verträglicher als z.B. Eisen-Sulfat. Bei Problemen mit der Ascorbinsäure, in der Regel (über-) empfindliche Mägen bei Menschen mit Leaky-Gut & Co., diese einfach weglassen.
Wenn zu viel Eisen vorliegt, dann empfiehlt sich ggf. Curcumin und Quercetin:
- Curcumin
- Life Extension (Curcumin Elite CGM-Mischung, 500 mg, 60 vegetarische Kapseln) – der Klassiker, leider mit Siliciumdioxid
- Info: Nutzt anscheinend die CurQuofen Technologie mit reduzierter Partikelgröße
- Doctor’s Best (Curcumin Phytosome Meriva, 500 mg, 180 pflanzliche Kapseln) – ähnlich LEF, leider mit Siliciumdioxid
- Info: Meriva ist auch eine wohl sehr gute Formulierung mit Phospholipiden aus Soja
- Gaia Herbs (CO2-Extrakt,60 Vegane flüssige Phyto-Kapseln) – in jedem Fall nicht so potent wie die vorgenannten, ohne Siliciumdioxid, mit Soja-Lecithin.
- Life Extension (Curcumin Elite CGM-Mischung, 500 mg, 60 vegetarische Kapseln) – der Klassiker, leider mit Siliciumdioxid
- Quercetin
- 50 mg enzymatisch modifiziertes Iso-Quercetin (Natural Factors, EMIQ) für angeblich bis zu 40-fach bessere Bioverfügbarkeit, ohne Siliciumdioxid
- 250 mg liposomal (Natural Factors, Quercetin LipoMicel Matrix) für angeblich bis zu 10 * besserer Resorption
- 500 mg / 60 Kapseln (MRM, QU995™ Quercetin) – ohne weitere Zusätze
Und die Curcumin-Kapseln von LEF senken klar das Ferritin. Sowas sagt nur keiner den Menschen mit geringem Eisen-Speichern.
Ach ja: Wenn Ihr bei iHerb etwas bestellen solltet, dann gebt bitte den 5% Rabatt-Code “HER2060“ an – und tut mir damit einen kleinen Gefallen.
Links / Quellen
- [1] Eisenmangel ohne Anämie – ein heißes Eisen? Nicht hämatologische Auswirkungen des Eisenmangels: Welche sind belegt, wann kommen sie zum Tragen?, Ferdinand Martius, Medizinische Universitätsklinik, Kantonsspital Bruderholz, Schweiz Med Forum 2009;9(15–16):294–299
- [2] Labordiagnostik bei Störungen des Eisenstoff wechsels, Fachinformation 0109, GanzImmun AG
- [3] Serum or plasma ferritin concentration as an index of iron deficiency and overload, Maria Nieves Garcia-Casal et al., Cochrane Database Syst Rev, 2021 May 24;5(5):CD011817. doi: 10.1002/14651858.CD011817.pub2.
- [4] Serum Ferritin and Estimate of Body Iron Stores, Medal, Abruf: 8.1.2024
- [5] The Dark Side of Iron: The Relationship between Iron, Inflammation and Gut Microbiota in Selected Diseases Associated with Iron Deficiency Anaemia—A Narrative Review, Ida J. Malesza et al., Nutrients. 2022 Sep; 14(17): 3478., Published online 2022 Aug 24. doi: 10.3390/nu14173478
Der Rest dieses Beitrages ist nur für eingeloggte Freunde des Blogs einsehbar. Bitte logge Dich ein, oder schaue unter dem Menüpunkt 'Freunde des Blogs' für weitere Informationen wenn ein ernsthaftes Interesse besteht hier weiter zu lesen.












Neuste Kommentare