Schwermetall-Chelatoren & Mobilisatoren: Eine Übersicht (DMPS, DMSA, EDTA, Zn-DTPA, Irminix, ALA, NAC, Glutathion) & Bindemittel

Flüssiges Quecksilber. Lizenz: CC BY SA 4.0. Autor: 2×910
Wer in das Thema Schwermetalle, Quecksilber, Blei & Co. eintaucht hat schnell die Frage: „Wie bekomme ich den Kram wieder aus meinem Körper raus“.
Gerade am Anfang sieht man oft den Wald vor lauter Bäumen nicht mehr – da es so viele verschiedene Varianten zu geben scheint, die alle mal mehr oder weniger kompliziert scheinen. Auch Therapeuten sind bei expliziter Nachfrage mit den nachfolgend diskutierten Fragen und Aspekten oft überfordert. Das ist aus meiner Sicht jedoch problematisch bzw. hoch-kritisch, denn in diesem Gebiet können leicht viele Fehler gemacht werden, welche dann nicht oder nur sehr schwer zu korrigieren sind.
Doch zurück zum Thema: Im Kern geht es bei den meisten ‚Schwermetall-Entgiftungs-Ansätzen‘ Ansätzen darum, über sogenannte Chelatoren die Schwermetalle und ggf. radioaktiven Substanzen aus dem Körper herauszuholen. Ein Chelator ist im ‚einfach-Sprech‘ eine Substanz, die mit einem Metall-Ion (z.B. einem Quecksilber-Ion) ein stabile Verbindung eingehen kann, die hoffentlich so lange Stabil ist bis Chelator+Schwermetall „aus dem Körper heraus sind“.
Optimal macht der Chelator das nicht nur im Blut, sondern mobilisiert (+bindet) auch Schwermetalle in Zellen, Organen sowie dem Gehirn – wozu der dieser jedoch die Blut-Hirn-Schranke (BHS) überwinden muss. Genau das, also die Überwindung der BHS, bzw. die Bindung ‚tief in den Organen‘, leistet nicht jeder Chelator. Aus meiner Sicht ist das auch gut so – allerdings nur dann, wenn auch ein mehrstufiger Plan da ist, was, wie und wann, zu welcher Zeit, in welcher Dosis und in welcher Abfolge getan werden ’sollte‘. Leider ist solch ein mehrstufiges Vorgehen nicht der „Standard“, u.a. da es ein tiefes auseinandersetzen mit der Detox-Materie bedingt.
So ist die Affinität (-> Bindungsfreude) eines jeden Chelators zu bestimmten Schwermetallen wie Quecksilber (Hg), Blei (Pb), Arsen (As) oder Gadolinium (Ga) verschieden & der richtige Chelator für die jeweilige Aufgabe sollte mit bedacht gewählt werden:
- Je nach dem wo der Schuh drückt (ggf. Mehrfachbelastungen, z.B. mit Hg und Pb),
- wie hoch die Belastung ist, wie schnell ggf. gehandelt werden muss (u.a. akut oder chronisch),
- welche Nebenwirkungen akzeptabel sind (u.a. Beförderung von Candida, Belastung der Leber oder eher der Niere) und
- nachdem, wie es um die finanziellen Möglichkeiten steht.
Entsprechende Verabreichungsform (u.a. oral per Kapsel, Infusion, Liposomal), Dosis, ein Einnahme-Schema (z.B. Cutler) und begleitende Supplemente, Vorbereitungen und ggf. zusätzliche Behandlungen von Therapeuten müssen ebenfalls sinnvoll festgelegt werden – wer hier ’schludert‘ der macht ggf. mehr Schaden als heile. Worum geht es mir nun in diesem Artikel?
- Was ist ein Chelator (bzw. Komplexbildner)?
- Der Unterschied zwischen Chelatierung, Mobilisierung und Bindemitteln
- Chelatoren für Quecksilber und die Thiol-Gruppen: DMPS, DMSA, Irminix, ALA, Glutathion
- Übersicht über die gängigsten Chelatoren bzw. Komplexbildner
- Übersicht über Glutathion-Beförderer und Bindemittel (Darm)
Am Ende des Artikels folgt wie immer mein übliches Fazit.
Hinweis: Mehr Interesse am Thema? Dann empfehle ich die Themenseite hier im Blog zur Schwermetall- & Quecksilber (Amalgam) Ausleitung, Cutler & Co.
Inhaltsverzeichnis für den Schnellzugriff
Was ist ein Chelator (bzw. Komplexbildner)?
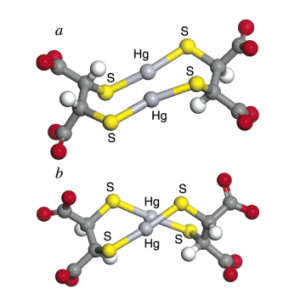
Berechnete Strukturen der beiden Diastereomere des kleinstmöglichen DMSA Hg 2+ Komplexes. Die Kohlenstoffatome werden als dunkelgrau, Sauerstoffatome als rot, Wasserstoffatome als weiß, Quecksilber-Atome als hellgrau und Schwefelatome als gelb dargestellt.. Quelle: [4]
„Als Chelatoren bezeichnet man organische oder selten anorganische Verbindungen, die zwei oder mehr freie Elektronenpaare aufweisen und damit mehr als eine koordinative Bindung mit einem zentralen (Metall-)Ion eingehen können. Damit haben sie die Fähigkeit, zwei- oder mehrwertige Kationen in stabilen, ringförmigen Komplexen (sogenannte Chelate) zu fixieren.“
Alternativ gefällt mir auch die Definition von Flora [29] (übersetzt mit Deepl.com):
„Chelatbildner sind chemische Verbindungen, deren Struktur es erlaubt, dass sich ihre zwei oder mehr Donoratome (oder -stellen) gleichzeitig an dasselbe Metallion anlagern und einen oder mehrere Ringe bilden.“
Übliche Chelatoren für Schwermetalle sind DMPS, DMSA, EDTA und für Gadolinium auch noch Zn-DTPA. Ganz exquisit mag auch noch Irminix von Boyd Haley sein – wobei dieser Chelator so gut sein soll, das er wohl niemals zugelassen wird. Schließlich ist Quecksilber (Hg) als Amalgam (was ca. 50% Hg enthält) aus schulmedizinischer Sicht kein Problem „und im Menschen als Amalgamfüllung ungiftig“ – denn es wird ja immer noch als Kassenleistung (in Deutschland) in die Zähne eingebaut. Man hält uns offen für Dumm und lügt uns ohne Scham in das Gesicht.
Da Quecksilber nun nicht gleichzeitig giftig und ungiftig sein kann, ist es (als Amalgam) per Definition per „offizieller Definition“ ungiftig, Hg-Dämpfe aus den Amalgam-Füllungen gibt es nicht und Bakterien wandeln metallisches Amalgam (u.a. als Abrieb) im Magen auch nicht zu Methyl-Quecksilber um. Wissenschaftliche Studien die so etwas in renommierten Magazinen beschreiben gilt es bitte zu ignorieren. Die Patienten mit angeblicher Hg-Belastung alle nur leicht verwirrt – und aus schulmedizinischer Sicht ist das Problem gelöst. Die Symptome zu behandeln ist ertragreicher als das ursächliche Problem anzugehen – soweit die Problemkaskade vom Arzt überhaupt realisiert und akzeptiert wird.
Würde man nun, einen im Vergleich zu DMPS & Co., wirklich potenten und ggf. sogar idealen Hg-Chelator zulassen – dann müsste man ja auch die Probleme durch Amalgam & Co. eingestehen, was dann zu vielen (haftungsrelevanten) Fragen führen würde. Wer einen gewissen Sarkasmus aus den letzten Sätzen bemerkt hat – hat richtig gelesen.
Der Unterschied zwischen Chelatierung, Mobilisierung und Bindemitteln
Aus meiner Sicht müssen bei der Ausleitung von Schwermetallen vorab noch drei Dinge unterschieden werden. So gibt es
- Chelatoren von Schwermetallen, also das, was das Hg & Co. bindet,
- wobei nicht alle Chelatoren alles gleich gut ‚binden‘.
- Mobilisatoren von Schwermetallen, also Stoffe welche das Hg & Co. aus den Zellen mobilisieren – aber nicht binden
- wobei es in einigen Fällen Überschneidungen zwischen Chelatoren & Mobilisatoren gibt.
- Bindemittel für den Darm, welche dort verschiedenste Toxine und teils auch Schwermetalle neutralisieren bzw. an sich binden können,
- wobei sie in Bezug auf die Bindung von Hg & Co. den Chelatoren in der Regel deutlichst unterlegen sind.
Chelatoren binden an Schwermetalle und ermöglichen (hoffentlich) deren (effiziente) Ausscheidung aus dem Körper entweder über die Nieren oder die Leber oder beides. Mobilisatoren neigen dazu, die Ausscheidung von Schwermetallen aus dem inneren der Zellen, den Knochen und dem Gehirn (über die Blut-Hirn-Schranke) anzuregen, also Körperteile, zu denen die meisten Chelatbildner keinen Zugang haben.
Das Problem: Mobilisatoren sind meist nicht besonders effektiv wenn es darum geht, die Bindung mit den Schwermetallen (bis zur Ausscheidung) aufrechtzuerhalten und können so auch (meist Dosisabhängig) Schwermetalle im Körper ‚umverteilen‘ – wenn sie alleine eingesetzt werden. Mobilisierende Mittel verlassen sich oft auf das Glutathion– (GSH-) System im Körper, um die Schwermetalle zu binden und sie über die Leber und den Verdauungstrakt aus dem Körper zu transportieren. Zwar kann so ein Teil der mobilisierten Schwermetalle aus dem Körper ausgeschieden werden, jedoch ist die Ausscheidungsrate im Vergleich zu tatsächlich wirksamen Chelatbildnern viel geringer.
Ein zusätzliches Problem, auf das auch Cutler hinweist ist, dass Mobilisatoren, welche die Blut-Hirn-Schranke überwinden (z.B. Alpha-Liponsäure, ALA), dazu neigen, Schwermetalle aus dem Gehirn zu entfernen, aber nur, wenn dort die Schwermetallkonzentration höher ist als im restlichen Körper. Ist dies nicht der Fall, können zusätzliche Schwermetalle in das Gehirn gelangen (-> osmotisches Gefälle).
Deshalb ist es wichtig, also zu Beginn eines Entgiftungsprogramms, keine mobilisierenden Mittel einzunehmen und sich zunächst auf die Chelatbildner zu konzentrieren, die das Körperinventar an Schwermetallen senken. Zudem ist es sinnvoll, bei der Verwendung eines mobilisierenden Mittels (z.B. ALA) gleichzeitig auch ein chelatbildendes Mittel zu verwenden (z.B. DMPS), so dass die durch das mobilisierende Mittel freigesetzten Metalle wirksam chelatiert werden.
Die Bindemittel für den Darm sind in dem ganzen Konzept eine weiteres ‚Netz‘, da diese u.a. verhindern sollen, dass z.B. an Glutathion, oder andere schwache Chelatoren bzw. Mobilisatoren gebundene Schwermetalle dort re-absorbiert werden.
Chelatoren für Quecksilber und die Thiol-Gruppen: DMPS, DMSA, Irminix, ALA, Glutathion
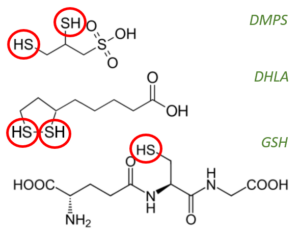
DHLA, DMPS und GSH im Vergleich.
Das relevante an den pharmakologischen Chelatoren (u.a. DMPS, DMSA), wie auch an dem wichtigsten physiologischen Chelator & Mobilisator Glutathion (GSH) sind die SH- bzw. Thiol-Gruppen. Denn letztendlich ist es dieser schwefelhaltige Ligand, über den die Bindung an das Hg-Ion geschieht, da Hg eine hohe Affinität zu SH-Gruppen hat. [4]
Ein idealer Quecksilber-Chelator würde nun ein Hg-Ion zwischen seinen beiden SH-Liganden fest binden – bis er aus dem Körper über den Stuhl oder Urin ausgeschieden wird. Allerdings ist dies nach neueren Erkenntnissen der Stereo-Chemie bei DMPS und auch DMSA zweifelhaft bzw. nicht gegeben [4][20]. Genau aus diesem Grund hatte Boyd Haley mit Irminix (vormals OSR2/NBMI) auch einen idealen Hg-Chelator mitentwickelt, der diese Limitation nicht hat [21]. Allerdings wurde dieser Chelator, vormals unter dem Namen OSR2 in den USA als Nahrungsergänzungsmittel verkauft, jedoch seitens der FDA als Arzneimittel eingestuft – und dann, wegen fehlender klinischer Tests, der Vertrieb und Verkauf verboten.
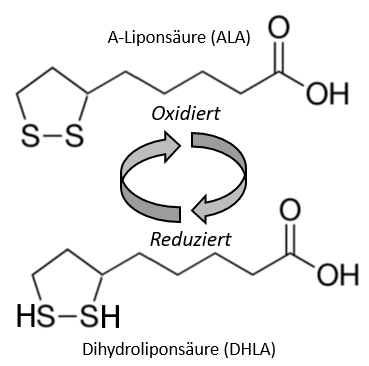
Als weiterer ’natürlicher‘ Chelator (& Mobilisator) wird die Alpha-Liponsäure (ALA) gehandelt. Diese hat (in der reduzierten Form als DHLA) ebenfalls zwei SH-Gruppen, unterliegt jedoch der Problematik von DMPS und DMSA in Bezug auf die Bindungskapazität seiner SH-Liganden [4]. So bezweifelt Christopher Shade von Quicksilver Scientific [22], dass DHLA auch in der Praxis als Chelator agiert. Allerdings spricht nach meiner Lesart der Studien alles dafür, das DHLA als Hg-Chelator fungiert [25][26][und andere] – wie es auch Cutler 1999 beschrieben hat [24]. Wie stabil und effizient ein Hg-DHLA-Komplex ist, ist allerdings noch eine andere Frage. Jedoch funktioniert die Cutler-Methode (mit ALA) aus meiner Sicht gut und verwendet meist günstige und lange erprobte Substanzen.
Auch gibt es noch einen physiologischen „Chelator“: (intrazelluläres) Glutathion (GSH). In Phase II der biochemischen Entgiftung konjugiert (-> bastelt, verbindet) die Zelle (-> mittels Gluthation-S-Transferasen, GST) ein Quecksilber-Ion (und anderes böses Zeug) an ein GSH-Tripeptid. Durch diesen Mechanismus macht die Zelle (bzw. der Körper) auf seine ’natürliche‘ Art Schadstoffe wie Quecksilber (und andere Toxine) transportfähig, damit diese in Folge aus der Zelle ausgeschieden werden kann. Dieser Prozess passiert primär in der Leber um das Hg-Ion in die Galle zu befördern und damit auszuscheiden. In wie weit und welcher Menge es in jeder Zelle geschieht im ein Hg-Ion aus der Zelle über das Blut in die Leber zu transportieren habe ich nicht recherchiert. GSH ist jedoch kein „Quecksilber-Chelator“, sondern ist, neben seinen zahlreichen anderen Funktionen, dazu da Toxine transportfähig zu machen.
Der Nachteil bei Glutathion ist jedoch, dass dieses intrazellulär gebildet werden sollte. Bei oraler Gabe wird GSH im Magen metabolisiert [17] und bei Infusion kann es spontan an Quecksilber binden und dieses Quecksilber im Körper ungünstig neu verteilen [24]. Der einzige mir bekannte Weg, GSH sicher von außen zuzuführen sind effektive (Nano-) Liposome [22]. Die sind jedoch teuer, müssen dauerhaft gekühlt werden, so das durchaus 95% der Glutathion-Produkte am Markt eher ‚lausig‘ sein dürften und bei Verzehr eine Hg-Problematiken schlimmer machen können.
In die Leber-Zelle wird der vorgenannte GSH-Hg-Komplex, wie auch DMSA, DMPS und ALA hoffentlich über einen Phase-III Membran-Transporter wie MRP2 [27] zusammen mit der Galle in die Gallenkanälchen ausgeschieden, gelangt in die Gallenblase (-> wo die Galle eingedickt wird), landet dann im Dünndarm, wo das Gift hoffentlich nicht re-absorbiert wird (-> Hg2+ wird fast nicht re-absorbiert, MeHg, primär aus Fisch, leider bis zu 95%) und gelangt schlussendlich möglichst schnell in der Toilette. Alternativ kann die Ausscheidung auch über die Niere geschehen, wobei auch hier Phase-III Membran-Transporter wie MRP2 involviert sind, um die Komplexe aus der Nierenzelle in die Harnblase zu befördern [15][28].
Ein weiterer wichtiger Aspekt eines idealen Chelators ist, dass dieser auch über die Blut-Hirn-Schranke (BHS) gelangen sollte und die Schwermetalle nicht nur aus dem Blut, sondern auch aus den Zellen und Organen mobilisieren ‚können sollte‘. DMSA und DMPS machen dies nicht (BHS) [3][22] und bezüglich der Zellen nur eingeschränkt, ALA macht wohl beides und befördert nebenbei noch die GSH-Produktion, wobei die Bindung an das Hg-Ion recht schwach sein könnte. Nur Irminix scheint beides so sicher zu machen, das der Komplex es, ohne relevante Re-Absorption im Darm, auch die Toilette erreicht [21] – also wenn die Phase III-Entgiftung sauber läuft. Allerdings muss eine Gehirngängigkeit nicht nur Positiv sein – speziell nicht zu Anfang einer Hg-Ausleitung.
Übersicht über die gängigsten Chelatoren bzw. Komplexbildner
Die nachfolgende Tabelle, die im Ursprung auf Assheuer [5] basiert, habe ich um einige Chelatoren, zusätzliche Informationen von Daunderer [1][7], Blaurock-Busch [3], Retzek [6], Mutter [23] und Cutler [24] erweitert. So habe ich zu der ursprünglichen Tabelle noch drei Spalten hinzugefügt:
- Bindet: Ungefähre Reihenfolge der Bindungsqualitäten, wobei die in Fett geschriebenen Elemente (im Vergleich bzw. in Relation) wohl sehr gut gebunden werden.
- Hws (Oral): Die ungefähre, geschätzte bzw. vermutete (pharmakologische) Halbwertzeit des Chelators im Blut bei oraler Zufuhr.
- BHS: Ob der Chelator in der Lage ist, die Blut-Hirn-Schranke zu überwinden.
- Anmerkung: Weiterführende Informationen zur Anwendung, Nebenwirkungen, Alternativen und den primären Ausscheidungswegen (Niere oder Leber)
| Chelator | Bindet [5] | Hws (Oral) | BHS | Anmerkung |
|---|---|---|---|---|
| DMPS (Dimaval®, Unithiol) | Hg, As, Sb [1][3], Cu [3], Ni [23], Pb, Zn, Cr [1] | 6-10h [11] | Nein | Gut für Hg, Bioverfügbarkeit <= 40% orale Aufnahme [2], wohl optimal bei RHg+/MeHg [7], aber auch gut bei Hg++ [4], Entg. über Niere [6][9]. Nach [2] sehr gut für Hg++/MeHg, As. |
| DMSA | Pb, Hg, As [7], Ni [nicht nach 1], Zn, Cd [4], Ba [10] | 2(,4)-3h [12][14] | Nein | Gut für Blei (FDA zugelassen), Bioverfügbarkeit <= 20% orale Aufnahme [2], Nach Daunderer besser bei Hg++, As und für die Senkung von Hg im Gehirn als DMPS [7], wobei der Effekt wohl indirekt ist [4]. Entg. über die Niere, fördert nach Cutler Candida & Co. [24] Fett erh. Bioverfügbarkeit [3]. Günstiger als DMPS, aber mehr Nebenwirkungen. |
| (Na, Ca, CaNa2, Mg) EDTA | Pb, Ca (Na/Mg-EDTA) [3], Cd [3], Zn [3], Fe, Cu, Ni | 1,4-3h [13] | Günstig, ggf. per i.v. effektiver. Nicht bei Hg-Belastung, Verschlimmerung nach Cutler [24][AC2], Boyd Haley [AC3] und Dr. Mutter [23]. Bei Blei besser DMSA nutzen. | |
| (Zn-) DTPA | Pb, Zn, Fe, Mn, Cr, (Zn), Radionukleide wie Pl, Bk, Am, Cm, Cf, bestes Mittel für Gadolinium | Nur als Infusion, wohl optimal bei Gadolinium (MRT-Kontrastmittel), Zn-DTPA zu bevorzugen, nicht mit Zn-Chelatoren mischen [23], Teuer. | ||
| Irminix, OSR2, NBMI (N,N′bis-(2-mercaptoethyl)-isophthalamide) | Hg, unklare Reihenfolge anderer Metalle, wohl auch effektiv bei ungebundenem Kupfer und Eisen [31] | ca. 6h | Ja | Inaktiviert Hg wohl eher als es dieses ausleitet. In der klinischen Erprobung (Phase II) [23], recht teuer bei „Drittanbietern“. |
| Desferroxamin (Desferal®) | Fe, Al | Bei Fe kann eine Alternative der Aderlass bzw. die Blutspende sein. Nach Mutter [23] gut verträglich (niedrige Dosen) | ||
| Deferipone (Ferriprox®) | Fe | Leitet Fe wohl mehr intrazellulär aus, Aussch. ü. Niere [23] | ||
| Eisen(III)-Hexacyanoferrat(II) (Radiogardase-Cs®) | Cäsium, Thallium | Auch als Preußisch Blau (Prussian Blue) bekannt. | ||
| Tiopronin (Captimer®) | Hg, Cu, Fe, Zn, Po, Cd | Wohl mehr Nebenwirkungen als D-Penicillamin, insb. (R)Hg+, weniger effizient als DMPS, Aussch. ü. Niere [23] | ||
| D-Penicillamin (Metalcaptase®) | Cu, Pb, Hg, Cd, Zn [23] | Ja [23] | Wohl starke Nebenwirkungen [23]. Bei Cu kann eine Alternative hoch dosiertes (Thio-)Molybdän + Zink sein [24] | |
| (RS-, R-, Na-R-) Alpha-Liponsäure (ALA)** | Hg (ggf. auch Pb, Cd, Mn, Zn, Ni) | 2-3h (RS-ALA) | Ja | Effizienz als effektiver Hg-Chelator umstritten, potenter Nrf2-Inducer. [22] Sehr günstig, Entgiftung über die Leber, nach Cutler effizient [24] Nahrungsergänzungsmittel bei Hg-Belastung mit ALA vermeiden. Potenter Mobilisator. |
** Mobilisator
Grundsätzlich ist das Ermitteln, welcher Chelator nun ‚im Detail‘ für welches Element besser ist, schwierig, da hier, speziell bei strukturell ähnlichen Chelatoren wie DMPS und DMSA, sehr viele Parameter relevant sind:
- Verabreichungsform (oral, intravenös), Dosis, mit oder ohne Fett, nüchtern oder nicht.
- Das Vorkommen des Elements im Organismus, da was mehr ‚vorkommt‘ auch mehr und schneller gebunden werden kann.
- Die Stabilitätskonstante zwischen Chelator und Element.
- Die Bindungsstärke des Schwermetalls an Biomoleküle – also wie ‚fest‘ die Schwermetalle an / in den Zellen hängen.
Es mag noch andere Chelatoren geben, u.a. BAL, jedoch sind diese nicht sehr gängig bzw. auf Grund ihrer Nebenwirkungen nicht mehr zeitgemäß. Ein Grenzfall in der Tabelle mag die Alpha-Liponsäure sein, welche neben der potentiellen Chelatoren-Fähigkeit auch noch über die Induktion von Nrf2 die Expression der antioxidativen Systeme und damit die Bildung von Gluthation fördert – also auch ein potenter Mobilisator ist.
Bei EDTA sollte beachtet werden, dass dieses wirklich nicht bei einer noch bestehenden Belastung mit Hg verwendet wird. DTPA sollte vorwiegend in der Zn-Form verwendet werden, um den Körperbestand an Zink zu schonen. Grundsätzlich sollten die Chelatoren dann auch nicht gemischt werden, um ungewollte Interaktionen zu vermeiden – z.B. würde DMPS das Zink aus dem Zn-DTPA binden, wie Mutter anmerkt [23].
Bei DMPS und DMSA gehen die Aussagen in der Literatur und von Praktikern auseinander, welches nun besser für organisches (R)Hg+ bzw. anorganisches Hg++ ist oder auch nicht. Hier kann aus meiner Sicht auch der Preis und die Verträglichkeit eine Rolle spielen, insbesondere jedoch die oft anzutreffende parallel-Belastung mit Blei (Pb).
Übersicht über Glutathion-Beförderer, weitere Mobilisatoren und Bindemittel (Darm)
Ein Thema das ich im Rahmen der Diskussion um Chelatoren bzw. Komplexbildner wichtig finde, sind Glutathion und Bindemittel. Ohne Glutathion (GSH) in den Zellen gibt es keine natürliche Entgiftung, keine Komplexierung von Toxinen & Schwermetallen an GSH mittels der Glutathion-S-Transferasen (GST). Oft haben Vergiftete, u.a. mit EHS, MCS und CFS, niedrige GSH-Werte. Fehlt ausreichend GSH – dann stockt die Toxinausscheidung aus dem Zellen: Ein Teufelskreislauf.
Cystein, optimal als N-Acetyl-Cystein (NAC) zugeführt, ist die ‚rate limiting‘ Aminosäure für die Körpereigene GSH-Synthese [3] und kann helfen, dass der Körper Glutathion (GSH) endogen, also selber, in den Zellen bilden kann [17]. Ein weiterer Aspekt sind pflanzliche Nrf2-Inducer, welche den Körper dazu anregen können mehr GSH zu produzieren (-> über die Induktion/Aktivierung bestimmter Gene). Allerdings wird eine äußere Zufuhr von GSH nicht nur kontrovers diskutiert[17], sondern diese ist (bei existierender Belastung mit Hg) auch teils mit starken Nebenwirkungen verbunden.
Das Problem: Exogen (-> Oral, IV) zugeführtes GSH kann, bei vorliegender Belastung mit Quecksilber, das Hg extrazellulär aufsammeln und in die Zellen bzw. das Gehirn verschleppen – was der Betroffene dann auch an unmittelbaren Verschlechterungen bemerken kann. Auch zu viel NAC oder Cystein kann nach Cutler sehr schleichend ähnliches befördern – so das hier, wenn man eher Vorsichtig ist (nach Cutler) ist ein Kompromiss auf Basis der Blutwerte (-> Aminogram) abzuwägen ist. Wenn NAC zugeführt wird, sollte jedoch an Glutamin und Glycin, zwei anderen Co-Faktoren für die GSH-Bildung, nicht gespart werden. Der Trick mit NAC zur Erhöhung des Glutathion funktioniert jedoch nicht bei den Menschen, bei denen die GSH-Synthese, u.a. (Epi-) Genetisch bedingt, nicht mehr funktioniert. Aber auch dafür gibt es ggf. teils Mittel und Wege, die jedoch den Rahmen dieses Beitrages sprengen.
Ein weiterer Aspekt sind Bindemittel für den Darm, so dass die von der Leber mittels Galle in den Dünndarm entlassenen (komplexierten) Schwermetalle nicht wieder über die Darmschleimhaut resorbiert werden. Ein effektiver Mix an den passenden Bindemitteln kann die Wiederaufnahme von toxischen Metaboliten, aber auch Schwermetallen reduzieren. Allerdings mag ich hier einschränken, das keine genau weis wie viel Schwermetalle & Co. diese Bindemittel im Darm nun konkret binden können. Für mich stellen Sie ein Netz mit doppeltem Boden dar: Jedes Nano-Gram Quecksilber & Co. das ausgeschieden und nicht mehr resorbiert wird, ist aus meiner eigenen Sicht den Aufwand wert.
| Substanz | Bindet | BHS | Anmerkung |
|---|---|---|---|
| N-Acetyl-Cystein (NAC)** | Verbessert die Ausscheidung von MeHg [12] um Faktor 5-10 in Tierstudien und auch in Kombination mit DMPS / DMSA (ca. 130-160%) | Ja | Unterstützt Glutathion-Bildung [3]. H.C.: Bei Hg-Belastung würde ich nur dann NAC zuführen wenn Cystein im Aminogram niedrig ist. |
| Glutathion (GSH)** | Natürlicher Komplexbildner in den Zellen (u.a. Hg) | Ja | Konjugierung von Toxinen & Metallen via Glutathion-S-Transferase(n) an GSH. H.C.: Nie Intravenös oder Oral bei Hg-Belastung zuführen. Liposomal nur mit entspr. Know-How. |
| Aktivkohle, Zeolithe, Bentonit, Chitosan, Pektine, Ballaststoffe, etc. | Verschiedenste (Schwer-) Metalle, Endotoxine, Chemikalien, Gifte, Toxinen, etc. | Nein | Primär gegen Pilze, Endotoxine, Chemikalien und (komplexierte) Metalle im Magen- und Darmtrakt. Binden eher wenig Schwermetalle im Vergleich zu den Chelatoren. H.C.: Ballaststoffe, L-Glutamin und Aloe-Vera ggf. auch für Darmaufbau. |
** Mobilisator
Weitere potentielle Substanzen die auch als Mobilisatoren agieren können (inkl. schon genannter), auf die ich hier jedoch nicht weiter eingehe sind:
- Alpha-Liponsäure (ALA, RS-ALA, R-ALA, Na-R-ALA), u.a. nach Christopher Shade sehr potente Nrf2-Inducer [22]
- Huminsäure, Fulvinsäure – neben Ihrer Fähigkeit Toxine zu Binden sind diese auch Mobilisieren (-> Nrf2-Inducer), ggf. sind einige Varianten (dosisabhängig) aber auch Zytotoxisch. Letzteres muss ich noch weiter recherchieren.
- Koriander (Extrakte bzw. Tinktur) – Unklarer Wirkungsmechanismus, soll BHS öffnen, viele ‚Horror-Geschichten‘ [30]
- Bärlauch (Extrakte bzw. Tinktur) – Schwefelhaltig, mobilisiert, bindet aus meiner Sicht nicht gut.
- Chlorella – Schwefelhaltig, mobilisiert, bindet aus meiner Sicht nicht gut, bzw. nur bei sehr hohen Mengen (> 30-50 g).
- Weißdornblatt und -beeren – sollen ggf. auch mobilisieren, wobei ich die Aussage nicht überprüft habe.
Aminosäuren und Derivate, die schwach mit Quecksilber und Blei binden, also suboptimale Mobilisatoren sind; welche aber auch von der Leber genutzt oder produziert werden bzw. in der Nahrung vorkommen:
- Methyl-Sulfonyl-Methan (MSM) – Cutler rät von einer Verwendung ab [24][30]
- H.C.: Ich sehe es weniger kritisch, würde bei Hg-Belastung jedoch Dosen um 1-2 g pro Tag nicht überschreiten.
- N-Acetyl-Cystein (NAC) – Ist die wichtigste Aminosäure für die GSH-Synthese im Körper. Cutler befürwortete seine Verwendung [24], aber nicht pauschal, sondern nur bei nachgewiesenen niedrigen Thiolen im Blut (-> niedriges Cystein, Methionin -> Aminogram) [AC1].
- H.C.: Die Dosis macht das Gift. Optimal sicherlich eingesetzt wenn auch Chelatoren zugeführt werden. Würde 600 mg / Tag nicht pauschal überschreiten
- Glutathion (GSH) – Macht die Zelle selber, nach Cutler niemals oral oder per Infusion zuführen [24][30], wobei es Shade [22] in liposomaler Form nutzt.
- H.C.: Eine exogene Zufuhr sehe ich sehr diffizil… wie Cutler. Einzig ein einziges spezielles nano-liposomales GSH-Produkt würde ich in Betracht ziehen.
Dann gibt es noch andere Mittel, die nicht unbedingt direkt mobilisieren, wo jedoch, aus meiner Sicht, Vorsicht geboten ist:
- Homöopathisches Quecksilber (und andere Homöopathische Entgiftungsmittel) – können ganz doll nach ‚hinten‘ los gehen.
- H.C.: Weil diese u.a. die Lymphzirkulation und Abbau von Ablagerungen im Lymphsystem mobilisieren können. Wer meint Homöopathie wirkt nicht, wird hier eines maximal besseren belehrt: minimalste Mengen homöopathisches Quecksilber können starke Um-Vergiftungsschübe auslösen.
- Elektromagnetisch stimulierende Behandlungen (PEMF, IR-Sauna, etc.) – kann nach vielen Berichten die Toxinausscheidung aus Zellen erhöhen [6].
- H.C.: Ich Tippe auch auf zusätzliche Induktion von Nrf2, wobei z.B.. PEMF auch auf die Zellmembranen wirkt.
- Phosphatidylcholin – zwar kein Mobilisator – jedoch kann es die Ausscheidung von Toxinen über die Galle verbessern (-> in der Regel sehr positiv).
- H.C.: Wichtig ist hier jedoch die Frequenz des Stuhlgangs sowie Bindemittel – um eine Re-Absorption der Toxine zu minimieren.
Gerade der letzte Punkt sollte noch einmal transparent machen, dass Bindemittel für den Darm mitunter einer der ersten Schritte beim (Schwermetall-) Detox sein sollten. Allerdings ist vielen ‚Praktikern‘ nicht so recht klar was gegen oder für was wirkt und wie ein Kombinations-Bindemittel konzipiert sein sollte.
Ein paar Anmerkungen zu Dosierungen & Co.
Als allgemeine Regeln, welche für fast jedes Nahrungsergänzungsmittel, jedoch insbesondere Chelatbildner und, ganz wichtig, für Mobilisatoren gelten – empfehle ich die folgenden Dinge:
- Immer mit einer sehr niedrigen Dosierung beginnen (u.a. DMPS, DMPS, ALA, Irminix)
- In der Regel nur Oral – fast nie per Infusion (bis z.B. auf Zn-DTPA, wobei wenn eine zusätzliche Hg-Belastung vorliegt in der Regel ein paar Extras zu beachten sind)
- Die Chelatoren, soweit möglich, immer im Abstand Ihrer Halbwertszeit zuzuführen bzw. einzunehmen
- U.a. in Verweis auf das Cutler-Protokoll
- Die Dosierung nur langsam, über einen Zeitraum von Wochen oder sogar Monaten, steigern und dabei etwaige (negativ) Symptome beachten
- Viele ‚Standard-Dosierungen‘ für Chelatoren sind aus meiner Sicht deutlich zu hoch angegeben -> Siehe auch das Cutler-Protokoll.
Ach ja: Wenn sich der Stuhlgang zu sehr verlangsamt, aber auch zu wenig ‚gepinkelt‘ wird, nimmt zudem die Rückvergiftung durch Wiederaufnahme von Giftstoffen durch die Darmwand bzw. in der Blase stark zu. Hier sollte dann keine ‚Entgiftung‘ begonnen werden.
Die Ausscheidung der Giftstoffe erfolgt schrittweise, und im Allgemeinen gilt: Je niedriger die Werte im Körper sind, desto höher kann die problemlose Dosierung des Chelatbildners geschehen. Leider kennt aber kaum jemand den Körperbestand. So ist aus meiner Sicht eine ’sanfte‘ Steigerung der Dosis einer aggressiven Variante vorzuziehen. Das eigene Wohlbefinden, die Härte & Frequenz des Stuhls, die Haut (u.a. Pickel), die Gesundheit der Leber und Niere (u.a. Blutwerte) können einem dabei helfen das individuell-richtige Maß in Zusammenarbeit mit einem kompetenten Therapeuten zu finden.
Auf jeden Fall: Nie einen Chelator oder Mobilisator einnehmen wenn noch Quecksilber im Mund, also den Zähnen bzw. dem Kiefer oder Weichteilen (u.a. als Splitter) steckt!
Mein Fazit
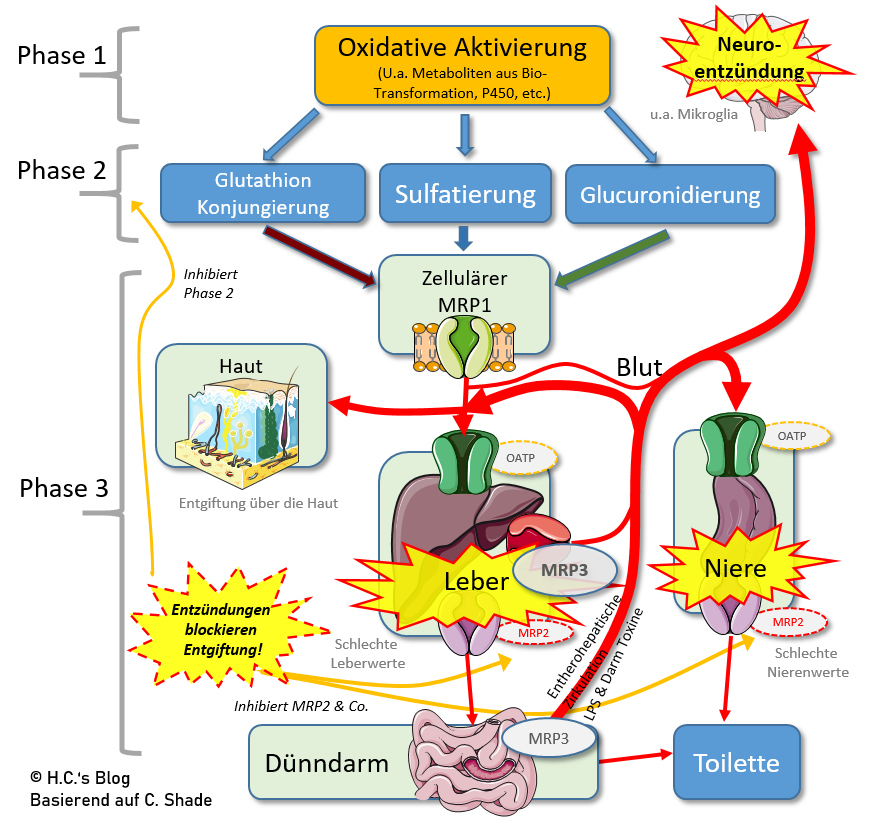
Das primäre Problem, das ich bei der Verwendung von Chelatoren sehe – also warum so viele ‚Ausleitungen‘ so unterschiedlich ausfallen (bzw. schief gehen) – ist, dass die Phasen II & III der biochemischen Entgiftung sowie die Ausscheidungsorgane Niere und Leber nicht ‚ordentlich‘ unterstützt werden. Egal wie gut chelatiert, komplexiert und gebunden wird – am Ende müssen die Schwermetall-Komplexe aus der Zelle, in das Blut, in die Leber- oder Nierenzellen und aus diesen Zellen wieder raus in Urin (Blase) oder den Dünndarm (zusammen mit der Galle), wo sie dann hoffentlich, alsbald möglich, in die Toilette entlassen werden.
Aus meiner Sicht klappt es mit
- DMSA & DMPS nur bei funktionierender Niere –> Detox-Schwächen der Niere führen ggf. zur Unverträglichkeit.
- Warum? Da die primäre Ausscheidung von Hg über die Niere erfolgt – wobei die Leber auch o.k. sein sollte. Allerdings könnte DMPS auch Hg aus der Niere „mitnehmen“ und die Lage dort potentiell verbessern. Dieses bedingt aus meiner Sicht jedoch unbedingt die Einhaltung des Cutler-Protokolls!
- ALA geht nur bei funktionierender Leber –> Detox-Schwächen der Leber führen zur Unverträglichkeit.
- Warum? Da die primäre Ausscheidung, speziell von anorganischem Quecksilber (Hg2+) über die Galle in den Dünndarm erfolgt [25].
- Irminix / NBMI könnte bei Nierenproblemen o.k. sein – leider sind Erfahrungsberichte und Daten dazu weniger umfassend als bei DMSA und DMPS. Meine Erfahrungen damit sind jedoch sehr positiv gewesen.
- Problem: Die Verfügbarkeit von „sauberem“ NBMI.
Zusammengefasst: Stockt irgend etwas im Prozess der Ausscheidung, gibt es (irgendwo) einen Stau (von toxischen Metaboliten) und dann kommt es zu Beschwerden. In Folgebeiträgen zur biochemischen Entgiftung werde ich auf diese Problematiken noch näher eingehen. Zur Einführung kann ich jedoch schon mal diesen Beitrag empfehlen sowie diesen zu den Bindemittel. Bei den „Sulfa“-Chelatoren (mit SH-Ligand) wird jedoch Molybdän gerne übersehen. Ohne (sehr) guten Molybdän-Status würde ich keine Chelat-Therapie beginnen!
Links / Quellen:
- [1] Handbuch der Amalgamvergiftung: Diagnostik – Therapie – Recht., Max Daunderer, 1995
- [2] Durchführung, Referenzbereiche und Interpretation des DMPS-Testes – Eine kritische Datenanalyse, Dr. Wolfgang Bayer, Laboratorium für spektralanalytische und biologische Untersuchungen Dr. Bayer Gmbh
- [3] Comparison of chelating agents DMPS, DMSA and EDTA for the diagnosis and treatment of chronic metal exposure. Blaurock-Busch, E.. (2014)., British Journal of Medicine and Medical Research. Doi: 10.9734/BJMMR/2014/6875.
- [4] A Review on Coordination Properties of Thiol-Containing Chelating Agents Towards Mercury, Cadmium, and Lead, Geir Bjørklund et al., Molekules, Molecules. 2019 Sep; 24(18): 3247., Published online 2019 Sep 6. doi: 10.3390/molecules24183247
- [5] Chronische Metallintoxikationen – Diagnosestellung und Therapie mit und ohne Chelatoren, Dr. Patrick Assheuer, Berlin, 18.11.2017
- [6] Metall-Detox in der Krebstherapie, Von Dr.med. Helmut B Retzek, August 17, 2018
- [7] Entgiftungscheckliste von Daunderer, Toxcenter
- [8] Risikoreduktion bei onkologischen Patienten durch Metallausleitung als Intervalltherapie., Fr. Professor Eleonore Blaurock-Bush, AZN 1/10
- [9] Fachinformationen DMPS (Dimaval) 100 mg Oral, Heyl
- [10] DMSA – die sanfte und effektive orale Entgiftung, Dr. rer. nat. Eleonore Blaurock-Busch, OM & Ernährung, 2011, Nr. 134
- [11] Medical Countermeasures—Chelation Therapy, Govinder Flora et al, Handbook of Arsenic Toxicology, 2015, Pages 589-626, doi: 10.1016/B978-0-12-418688-0.00026-5
- [12] Clinical Environmental Medicine – Identification and Natural Treatment of Diseases Caused by Common Pollutants, Walter J. Crinnion und Joseph E. Pizzorno, Elsevier; Auflage: 1 (26. April 2018)
- [13] Chelation in Metal Intoxication, Swaran J.S. Flora* and Vidhu Pachauri, Int J Environ Res Public Health. 2010 Jul; 7(7): 2745–2788., Published online 2010 Jun 28. doi: 10.3390/ijerph7072745
- [14] Pharmacokinetics of meso-2,3-dimercaptosuccinic acid in patients with lead poisoning and in healthy adults., Dart RC1, Hurlbut KM, Maiorino RM, Mayersohn M, Aposhian HV, Hassen LV., J Pediatr. 1994 Aug;125(2):309-16., doi: 10.1016/s0022-3476(94)70217-9
- [15] Impact of Organic Anion Transporter 3 (OAT3) on renal transport of the metal chelator 2,3-Dimercapto-1-propane-sulfonate (DMPS), Matthias Rödiger et al., Can J Physiol Pharmacol. 2010 Feb; 88(2): 141–146., doi: 10.1139/Y09-123
- [16] Interaction of 2,3-Dimercapto-1-propane Sulfonate with the Human Organic Anion Transporter hOAT1, Florian Islinger, and
- [17] Chelation: Harnessing and Enhancing Heavy Metal Detoxification—A Review, Margaret E. Sears, ScientificWorldJournal. 2013; 2013: 219840., Published online 2013 Apr 18. doi: 10.1155/2013/219840
- [18] Mercury binding to the chelation therapy agents DMSA and DMPS and the rational design of custom chelators for mercury, G.N. George, R.C. Prince, J. Gailer, G.A. Buttigieg, M. Bonner Denton, H.H. Harris, I.J. Pickering, Chem Res Toxicol, 2004 Aug;17(8):999-1006. doi: 10.1021/tx049904e.
- [19] Insights on alpha lipoic and dihydrolipoic acids as promising scavengers of oxidative stress and possible chelators in mercury toxicology, Geir Bjørklunda et al., Volume 195, June 2019, Pages 111-119, Journal of Inorganic Biochemistry, doi: 10.1016/j.jinorgbio.2019.03.019
- [20] G.N. George, R.C. Prince, J. Gailer, G.A. Buttigieg, M. Bonner Denton, H.H. Harris, I.J. Pickering, Mercury binding to the chelation therapy agents DMSA and DMPS
and the rational design of custom chelators for mercury, Chem. Res. Toxicol. 17 (2004) 999–1006. - [21] Amelioration of Acute Mercury Toxicity by a Novel, Non-Toxic Lipid Soluble Chelator N,N′bis-(2-mercaptoethyl)isophthalamide: Effect on Animal Survival, Health, Mercury Excretion and Organ Accumulation, David Clarke, Roger Buchanan, Niladri Gupta and Boyd Haley, Toxicol Environ Chem. 2012; 94(3): 616–640., doi: 10.1080/02772248.2012.657199
- [22] Dr Shade’s Lecture at ACIM 2017, Quicksilver Scientific, Dec 8, 2017
- [23] Entgiftung: Effektiv bei vielen Krankheiten, Joachim Mutter, OM – Zs. f. Orthomol. Med. 2016; 4: 5–15
- [24] Amalgam Illness: Diagnosis & Treatment: What You Can Do to Get Better, How Your Doctor Can Help You, Andrew Hall, Ph.D. Cutler , 1. Juni 1999
- [25] Effect of lipoic acid on biliary excretion of glutathione and metals., Gregus Z, Stein AF, Varga F, Klaassen CD, Toxicol Appl Pharmacol 1992 May;114(1):88-96, doi: 10.1016/0041-008x(92)90100-7.
- [26] Zashchitnyi effekt amida lipoevoi kisloty pri eksperimental’nom merkurializme. [Protective effect of lipoic acid amide in experimental mercurialism], Leskova GE, Gig Tr Prof Zabol 1979 Jun;(6):27-30 (Teiltext)
- [27] MRP2 and the DMPS- and DMSA-Mediated Elimination of Mercury in TR− and Control Rats Exposed to Thiol S-Conjugates of Inorganic Mercury, Christy C. Bridges et al., Toxicol Sci. 2008 Sep; 105(1): 211–220., Published online 2008 May 28. doi: 10.1093/toxsci/kfn107
- [28] MRP2 involvement in renal proximal tubular elimination of methylmercury mediated by DMPS or DMSA, Rudolfs K Zalups, Christy C Bridges, Toxicol Appl Pharmacol, 2009 Feb 15;235(1):10-7.,doi: 10.1016/j.taap.2008.11.003. Epub 2008 Nov 19.
- [29] Handbook of Arsenic Toxicology Chapter 26 – Medical Countermeasures—Chelation Therapy, Govinder Flora et al., Handbook of Arsenic Toxicology, 2015, Pages 589-626, DOI: 10.1016/B978-0-12-418688-0.00026-5
- [30] What NOT to do!, CutlerSuccessStories.com, 12.12.2017
- [31] Boyd Haley, Delingpod’s Podcast, 19.11.2022 (Backup)
Cutlers Kommentare:
Der Rest dieses Beitrages ist nur für eingeloggte Freunde des Blogs einsehbar. Bitte logge Dich ein, oder schaue unter dem Menüpunkt 'Freunde des Blogs' für weitere Informationen wenn ein ernsthaftes Interesse besteht hier weiter zu lesen.







Neuste Kommentare