Detox 5: DMPS & DMSA – Die Standard-Chelatoren für Quecksilber (Hg) und Blei (Pb): Zu Halbwertszeiten, (Neben-) Wirkungen, Dosen & Co.
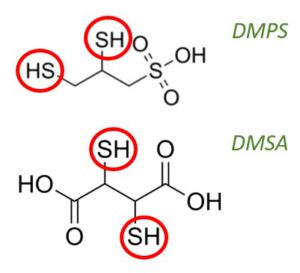
Struktur von DMPS und DMSA.
Die wohl verbreitetsten Chelatoren für Quecksilber (Hg) und andere Schwermetalle sind wohl Dimercaptopropansulfonsäure (DMPS) und Dimercaptobernsteinsäure (DMSA). Beide Chelatoren wurden in den 50er Jahren in der ehemaligen UDSSR entwickelt & Synthetisiert: DMPS von V. E. Petrunkin, 1956 und DMSA von V. Nirenburg im Urals Polytechnic Institute (ebenfalls in den 50’ern). Heute wird DMPS in Deutschland als Dimaval® von der Heyl GmbH & Co. KG produziert und ist „das“ Mittel bei Hg-Belastungen, wofür es in Deutschland sogar offiziell zugelassen ist.
Auch das Cutler-Protokoll nutzt diese beiden gut verfügbaren Chelatoren, wobei DMSA eher bei einer Co-Belastung mit recht viel Blei eingesetzt wird und aus meiner Sicht DMPS das Mittel der Wahl bei Hg–Belastungen ist. Allerdings, und darauf weißt nach meiner Kenntnis nur Cutler hin, gibt es bei der Einnahme der Chelatoren etwas zu beachten: Die zeitliche Abfolge, Regelmäßigkeit und Dauer der Einnahme, die sich nach Cutler an der pharmakologischen Halbwertzeit (t1/2) der oral zugeführten Chelatoren im Blutplasma orientieren sollte. Egal wie man zum Cutler-Protokoll steht, dieser Aspekt ist real, relevant und wird u.a. von „Opponenten“, wie C. Shade, PhD (Firma Quicksilver Scientific) bestätigt. Bestimmte pharmakologische Grundlagen gelten eben unabhängig persönlicher Ansichten.
Die Punkte die ich in diesem Artikel besprechen möchte sind dann folgende:
- Welche Schwermetalle werden durch DMPS & DMSA Cheliert?
- Vorweg: DMPS & DMSA sind keine optimalen Chelatoren
- Details zu DMSA
- Details zu DMPS
- Zu Anflutung (tmax) und Halbwertszeiten (t1/2) von DMSA und DMPS
- Zur Dosierung und Anwendung von DMPS und DMSA – und etwas zu Infusionen
- Nebenwirkungen & Kritiken zu DMPS und DMSA
Am Ende des Artikels folgt dann mein übliches Fazit.
Tipp: Hier geht es zu meiner Schwermetall- und ‚Entgiftungs‘-Übersichtsseite
Inhaltsverzeichnis für den Schnellzugriff
Welche Schwermetalle werden durch DMPS & DMSA Cheliert?
In meinem Übersichtsartikel zu den Chelatoren hatte ich schon versucht die teils unterschiedlichen Angaben zu plausibilisieren. Da ich dem nichts mehr hinzuzufügen habe, hier noch einmal der Tabellenausschnitt und die Erklärung der Spalten:
- Bindet: Ungefähre Reihenfolge der Bindungsqualitäten, wobei die in Fett geschriebenen Elemente (im Vergleich bzw. in Relation) wohl sehr gut gebunden werden.
- Halbwertzeit (Hwz, Oral): Die ungefähre, geschätzte bzw. vermutete (pharmakologische) Halbwertzeit des Chelators im Blut bei oraler Zufuhr.
- BHS: Ob der Chelator in der Lage ist die Blut-Hirn-Schranke zu überwinden.
- Anmerkung: Weiterführende Informationen zur Anwendung, Nebenwirkungen, Alternativen und den primären Ausscheidungswegen (Niere oder Leber)
| CHELATOR | BINDET [5] | Hwz (Oral) | BHS | ANMERKUNG |
|---|---|---|---|---|
| DMPS (Dimaval®, Unithiol) | Hg, As, Sb [1][3], Cu [3], Ni [23], Pb, Zn, Cr [1] | 6-10h [11] | Nein | Teurer als DMSA, <= 40% orale Aufnahme [2], wohl optimal bei RHg+/MeHg [7], aber auch gut bei Hg++ [4], Entg. über Niere [6][9]. Nach [2] sehr gut für Hg++/MeHg, As. |
| DMSA | Pb, Hg, As [7], Ni [nicht nach 1], Zn, Cd [4], Ba [10] | 2-4h [12][14] | Nein | Günstig, <= 20% orale Aufnahme [2], Nach Daunderer besser bei Hg++, As und für die Senkung von Hg im Gehirn als DMPS [7], wobei der Effekt wohl indirekt [4] und unwesentlich [40][51] ist. Entg. über Leber [6], fördert nach Cutler Candida & Co. [24] Fett erh. Bioverfügbarkeit [3]. |
Das Labor Beyer [2] weißt hin, das Aposhian et al. (2003) [34] zeigten, dass weder DMPS noch DMSA allein noch in Kombination mit Vitamin C, Alpha-Liponsäure oder Glutathion den Quecksilbergehalt im Gehirn bei belasteten Ratten reduzierten – was zu der Angabe passt, das beide Chelatoren die BHS nicht überwinden sollen. Allerdings lief die Studie nur über 7 Tage und hat viele systemische Schwächen im Design, was jedoch für diesen Aspekt nicht relevant war.
Grundsätzlich haben sich sowohl DMSA als auch DMPS in Humanen Studien zur Quecksilbertoxizität als klinisch wirksame Schwermetallchelatoren erwiesen, welche beide anorganisches und organisches Quecksilber binden/ausleiten. DMSA wirkt dabei nur als extrazellulärer Chelator, während DMPS in Hepatozyten und Nierenzellen eindringen soll, obwohl es immer noch als primär extrazellulärer Chelator angesehen wird. [34][38]
Das DMPS das Mittel der Wahl für anorganisches Quecksilber ist – scheint mir jedoch unbestritten: Bei Daunderer [1], Beyer [2] und anderen [3][4][21][27][28] ist das eindeutig. Teils [36], u.a. auch bei Daunderer [7], wird angegeben, das DMSA für Methyl-Hg bzw. das Gehirn ‚besser‘ sei als DMPS, wobei dieser Effekt auch indirekt sein kann [4] (deepl.com):
„Es (Anm: DMSA) passiert nicht die Blut-Hirn-Schranke, scheint aber indirekt die MeHg-Belastung des Gehirns zu reduzieren, indem es das Gleichgewicht zwischen Gehirn und Blut verändert“
Cutler [40] beschreibt das dies zwar der Fall ist, die ‚Beschleunigung‘ durch DMSA jedoch, in Verweis auf Buchet et al. [41], maximal 20% gegenüber der natürlichen Halbwertzeit des Hg im Gehirn (25 Jahre) hätte – was klinisch gesehen irrelevant wäre. So kann auch Dr. Retzek [27] Daunderer in diesem Punkt nicht folgen und führt verschiedene Studien an, die belegen sollen, das zumindest DMPS effektiv die Hg-Last im Gehirn reduziert, u.a. bei einem Goldschmied mit schweren neurologischen Symptomen, der durch DMPS beschwerdefrei wurde [26] oder bei einer massiven Quecksilberbelastung mit neurologischen Symptomen von 95 Philippinischen Goldminen-Arbeitern [27]. In Bezug auf Alkyl-Hg (u.a. MeHg) soll nach anderen Studien [13][29] dann DMPS ‚auch the drug of choice‘ sein. Ich denke jedoch, das die Interpretation dieser Studien durch Retzek in Bezug auf Hg im Gehirn zu positiv ist: Ggf. hat sich eine Symptomatik verändert – dies kann aber viele Ursachen haben.
Dr. J. Mutter ergänzt zwar auch noch, das DMPS u.a. eine gute Wirkung bei vielen neurologischen Krankheiten hat [21] – was jedoch viele Ursachen haben kann, u.a. auch die indirekten Auswirkungen der Senkung von Hg auf das Gehirn bzw. neurologische Prozesse – hier z.-B. im Darmtrakt (-> Gehirn-Darm-Achse), der Leber und Niere. Zu DMSA schreibt Mutter u.a.:
„… ist aber zur Quecksilberausleitung schwächer wirksam als DMPS und für Arsen gar nicht.“
Im folgenden Text sollte dann auch noch klar werden, das DMPS bzw. intestinaler Resorption und potentiellen Nebenwirkungen besser abschneidet als DMSA – so zumindest meine Lesart und (auch) meine Erfahrung.
Vorweg: DMPS & DMSA sind keine optimalen Chelatoren
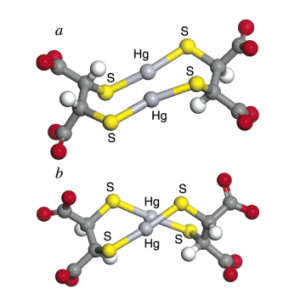
Berechnete Strukturen der beiden Diastereomere des kleinstmöglichen DMSA Hg 2+ Komplexes. Die Kohlenstoffatome werden als dunkelgrau, Sauerstoffatome als rot, Wasserstoffatome als weiß, Quecksilberatome als hellgrau und Schwefelatome als gelb dargestellt.. Quelle: [4]
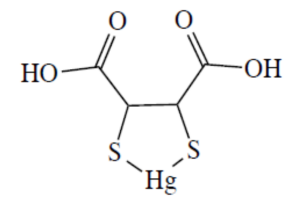
So wohl nicht: Die von Rivera et al. vorgeschlagene Molekülformel des DMSA-Hg-Komplexes. Quelle: [4]
„Chelatbildner sind chemische Verbindungen, deren Struktur es erlaubt, dass sich ihre zwei oder mehr Donoratome (oder -stellen) gleichzeitig an dasselbe Metallion anlagern und einen oder mehrere Ringe bilden.“
Zudem sollte ein idealer Chelator a) Fettlöslich sein, damit er die Blut-Hirn-Schranke (BHS) überwindet, b) Zellgängig sein und die Schwermetalle c) möglichst unlösbar und damit sicher an sich binden können, meint: Der Chelator-Hg-Komplex sollt zumindest bis zur potentiellen Ausscheidung über Urin bzw. Stuhl nicht zerfallen bzw. Re-Absorbiert werden.
Nach Haley [31][33], Bjørklund et al. [4] und George et al. [18] ist das Problem bei DMPS, DMSA (und auch ALA) jedoch, das ein Hg-Ion nicht zwischen die beiden SH-Liganden (Thiol-Gruppen) passt (-> 3D-Stereochemie). So braucht es in der Regel wohl 2 Moleküle DMPS, DMSA und auch ALA um ein Hg-Ion zu komplexieren bzw. zu binden. Dadurch ist jedoch der gesamte Komplex, wie nebenan abgebildet, nicht so stabil wie ursprünglich angenommen. Dies könnte dann auch einen Teil der vielen unterschiedlichen bzw. widersprüchlichen Erfahrungen mit DMPS und DMSA erklären. George et al. [18] schreiben so (deepl.com):
„Wir zeigen, dass weder DMSA noch DMPS einen echten Chelatkomplex mit Quecksilberionen bilden und dass diese Medikamente für ihre klinische Aufgabe, Quecksilberionen zu binden, als suboptimal angesehen werden sollten.“
Mercola schreibt zusammenfassend in Bezug auf ein Interview mit Boyd Haley [31] (Deepl.com):
„Laut Haley sind sie in der Tat keine echten Chelatbildner. Vielmehr bilden sie einen ‚Sandwich-Komplex‘, bei dem an jedes Quecksilbermolekül zwei DMSA-Moleküle gebunden sind, im Gegensatz zu nur einem.“
Ein weiteres Problem ist, das DMPS und DMSA nicht die BHS überwinden und nicht sehr Zellgängig sein sollen (-> beide sind negativ geladen, was eine effektive Zellpenetration verhindert und die Mittel hauptsächlich im Blut hält [30]). Bei DMSA binden sich dann wohl etwa 95 % an Plasmaproteine (-> Albumin), so das nur noch eine SH-Gruppe frei ist, um Metalle zu binden [4]. Angesichts der in der Regel nicht verfügbarer Alternativen (-> Irminix, NBMI) gibt es in der Praxis für die meisten Menschen keine Alternative zu DMPS bzw. kombinierten Ansätzen mit Alpha-Liponsäure (ALA) zusammen mit DMPS (u.a. das Cutler-Protokol).
Details zu DMSA
Das grundsätzliche Problem bei den Chelatoren ist, das sich viele und teils widersprüchliche Informationen zu diesen finden lassen. Der deutsche Schwermetall-Pionier Daunderer, primär tätig im letzten Jahrhundert, schrieb damals zu DMSA [1, Seite 824]: a) Weniger toxisch als DMPS, aber: nicht nach Labor Beyer [2], wenn man die nötigen Dosen auf Basis der Bioverfügbarkeit & Wirkung angleicht. b) drei mal mehr Arsenausscheidung als DMPS, aber: nicht nach J. Mutter [21]), c) Kupferausscheidung wie bei DMPS, aber: nicht nach [3][10], wo DMPS deutlich besser abschneidet) und d) wirkungslos bei Eisen, Al, Barium, Berillyum, Chrom, Mg, Mangan, Selen, Zinnoxid, Strontium, aber: Nach [10] wird zumindest auch Selen & Barium gebunden. Was bleibt ist wohl:
- Relativ viel Bindung von Zink
- Auch gut geeignet für Kobalt, Platin, Silber, Nickel
Mein kurzes Anfangsfazit: So einfach ist das mit an Angaben von Daunderer wohl nicht – einiges scheint falsch bzw. strittig. Schauen wir mal auf die einzelnen Punkte die mir plausibler scheinen:
- Toxizität: Nach [2] LD50 bei parenteraler Gabe (i.p., Maus) bei zirka 2500 mg/kg Körpergewicht, bei Katze und Hund jedoch nur ca. 150 mg/kg.
- Meint: Die Übertragung auf den Mensch ist zweifelhaft, da es große Speziesunterschiede gibt.
- Bioverfügbarkeit (Oral): Hier gibt es verschiedenste Werte, wobei orales DMSA wohl nicht gut aufgenommen wird:
- Einnahme auf nüchternen Magen bei 15-20% [2],
- 20% [4] bzw. 25% [3], wobei
- die Gleichzeitige Verabreichung von Fett die orale Bioverfügbarkeit um bis zu 40% erhöht [3].
- Ausscheidung: Wohl über Urin, jedoch vorwiegend Stuhl [17]
- Wobei wohl nur 10-25% über den Urin ausgeschieden werden und
- die Hauptlast auf der Leber liegt [6] und dann mittels des Stuhl ausgeschieden wird. (-> DMSA-Cystein-Disulfide Konjugate) [3]
- Cutler merkt jedoch an, das sich das Hg bei DMSA wohl vorwiegend im Urin, jedoch nicht dem Stuhl finden lässt [35, Seite 150]. Zudem gibt er in seinem Standardwerk [35] dann auch auf auf Seite 206 & 207 Hinweise bzw. Formeln zur Pharmakokinetik von DMPS, DMSA und ALA – aus denen hervorgeht, das DMSA-Konjugate wohl primär über den Urin ausgeschieden werden.
Ein Problem kann wohl noch sein, das die Nieren-‚clearance‘ von DMSA bei Patienten mit Bleivergiftung, insbesondere bei Kindern, reduziert sein kann. Bei Patienten mit Anzeichen einer signifikanten Nierenfunktionsstörung, sei es durch Blei oder andere Ursachen, könnte die Verwendung hoher DMSA-Dosen so zu einer Akkumulation von Toxinen und der Entwicklung von zuvor nicht erkannten toxischen Wirkungen führen [14], was Cutlers Sicht unterstützt. Auch C. Shade (Quicksilver Scientific) weißt auf die Nieren-Problematik (-> Hg-Akkumulation) in verschiedenen Webinars hin. Gerade wenn die Phase III der Entgiftung, also die Membrantransporter wie insbesondere MRP2 in der Niere nicht funktionieren kann es hier zu Problemen bei der Ausscheidung der DMSA & DMPS-Komplexe kommen [42].
Daunderer [7] merkt aber noch an, das DMSA stärker fettlöslich sein, was nach [3] stimmen mag, und deswegen besser auf das Gehirn wirke (‚achtfach‘ mehr als DMPS), bei fettleibigen Menschen aber wiederum schlechter wirke – da es sich hier auch in den Fettgeweben akkumuliert. Allerdings passen Daunderers Angaben bzw. Hg-Gehirn-Detox nicht zu dem, was Aposhian et al. (2003) [34] und andere berichten.
Details zu DMPS
Einige Schwermetalle, darunter Blei, Cadmium und Quecksilber (speziell Hg++ [15]), werden bei der Urinausscheidung in den proximalen Tubuluszellen der Niere akkumuliert und verursachen chronische Nierenerkrankungen. Ein gängiger Weg hier die Belastung zu senken ist die Gabe von DMPS, was primär über die Nieren ausgeschieden wird [15][16]. Allerdings weist Mutter [21] darauf hin, das die Bindungskonstante von DMPS um so höher ist, je alkalischer das Milieu ist. Ein zu saurer Urin ist also im Kontext einer DMPS basierenden Ausleitung nicht optimal, da hier sogar Schwermetalle (aus dem Körper) an das Gewebe angegeben werden könnten.
So viel zur Einführung, doch schauen wir mal auf die einzelnen Punkte wo es mehr Übereinstimmung zu geben scheint:
- Toxizität: Nach [2] LD50 bei parenteraler Gabe (i.p., Maus) in einem Bereich von 1100 bis 1500 mg/kg Körpergewicht.
- Die Übertragung auf den Mensch ist allerdings wie auch bei DMSA zweifelhaft.
- Bioverfügbarkeit (Oral): Hier gibt es verschiedenste Werte, wobei orales DMPS wohl recht gut aufgenommen wird:
- Nach Beyer [2] ca. 50% (Maiorino et al., 1991; Waelti, 1992),
- nach [4] < 40% und
- nach [12] 39% Absorption.
- Ausscheidung: Primär über die Niere / den Urin [6]
- So werden beim Menschen ca. 50 % des oral verabreichten DMPS im Urin nachgewiesen [9].
- Optimal für
- Anorganisches Hg++ [4]
- Kombibelastungen aus „Sb, As und Hg.“ [3]
- Belastungen der Nieren (besser als DMSA) [4][34], wobei die Membrantransporter (u.a. MRP2) funktionieren müssen [42].
Hinweis: Der nachfolgende Abschnitt ist nur für Unterstützer sichtbar.
Da auch mehr Kupfer, Zink, Selen, Magnesium ausgeschieden werden, ist auf eine Ergänzung zu achten [12]. Aus einer Studie zu DMPS-Infusionen [43] mit ca. 250 mg DMPS errechnete ich nachfolgend ca. 1,7 µg Zn pro Liter Urin (was wenig wäre), sowie ca. 0,5 mg Kupfer pro L Urin, was schon sehr viel wäre. So könnten pro 100 mg DMPS durchaus 0,5-1 mg Gesamtkupfer ausgeschieden werden. Insofern würde ich bei längerer Therapie auch die Kupfer-Spiegel überwachen.
Mutter [21] beschreibt noch eine gute Wirkung bei bei vielen neurologischen Krankheiten, Autoimmunerkrankungen, Durchblutungsstörungen, Autismus, Neurodermitis, Psoriasis, Allergien, chronische Müdigkeit, Schmerzsyndrome, etc.
Zu Anflutung (tmax) und Halbwertszeiten (t1/2) von DMSA und DMPS
Hinweis: Der nachfolgende Abschnitt ist nur für Unterstützer sichtbar.
Da die Messwerte die in der Literatur finden, noch abhängig von Dosis, Nüchternheit, Körpergewicht, Zustand des Magen-Darmtraktes und mehr sind – finden sich dann auch die unterschiedlichsten Angaben. Für DMPS habe ich folgende Angeben ermitteln können:
| Dosis | t bis cmax | t1/2 | Anmerkung | Quelle |
|---|---|---|---|---|
| 5-50 mg | ? | 6-8 h | DMPS alle 6 h in der Praxis besser | Cutler [35] |
| 300 mg | 3,4 h | 9,9 h | Plasma, 10 Probanden | [1, Seite 786] |
| 300 mg | 3,7 h | 9,1 h | Blut, 10 Probanden | [1, Seite 786] |
| ? | 4 h | 10 h | ? | [2] |
| ? | 3 h | Nach 5-6 h 80% Ausscheidung über den Urin | [3] | |
| ? | 3,5 h | 10 h | [11] |
Für DMSA habe ich folgende Werte ermitteln können:
| Dosis | t bis cmax | t1/2 | Anmerkung | Quelle |
|---|---|---|---|---|
| 5-50 mg | ? | 3-4 h | DMSA alle 3 h in der Praxis besser | Cutler [35] |
| ? | 2 h | 2-3 h | [2] | |
| ? | <4 h | [4] | ||
| ? | 2-3 h | [12] | ||
| ca. 350 mg | 2-3 h | Kürzeres t1/2 in Kindern | [14] | |
| 10 mg/Kg | 3,2 h + 0,56 SE | Mensch, nach ca. 11 h Fasten (über Nacht) | [38][39] |
Zusammenfassend scheint es mir, das bei DMPS nicht nur die reine Halbwertzeit, sondern auch das tmax relevant ist, weil die Zeit bis zum maximalen Anstieg deutlich kürzer ist als die Zeit des Abfalls bzw. der Metabolisierung. Bei DMSA scheint ist der Abfall im Blut jedoch schneller – bezogen auf die Zeit der Einnahme bis zum tmax. Insofern scheint der von Cutler etablierte Zusammenhang, sowie die in der Praxis erprobten Einnahme-Intervalle für orales DMPS (-> alle 6 h) und DMSA (-> 3 h), gut mit den Daten zu korrelieren – wenn man auf mehr schaut, als die reine Halbwertzeit.
Zur Dosierung und Anwendung von DMPS und DMSA – und etwas zu Infusionen
Da die orale Bioverfügbarkeit von DMSA, je nach Quelle, um Faktor 2-3 unter der von DMPS liegt müsste nach Labor Beyer [2] in verweis auf Hibberd et al. (1998), also um ähnliche Chelatierungs-Erfolge zu erreichen, ca. 3 mal mehr DMSA (Brutto) als DMPS zugeführt werden. Mit Blick auf die (intestinalen) Nebenwirkungen empfiehlt sich in der Regel dann auch DMPS.
Bei den Dosierungen ‚aus der Apotheke‘ gibt es bei DMPS keine große Auswahl:
- 100 mg Kapsel (Dimaval) von Heyl,
- Theoretische Bindungskapazität (bei 40% Resorption): 38 mg Quecksilber oder 120 mg Kupfer oder 116 mg Zink.
- 250 mg Ampullen für die Infusion (Unithol),
- Theoretische Bindungskapazität: 238 mg Quecksilber oder 753 mg Kupfer oder 732 mg Zink. [2]
- (teure) Eigenherstellungen von Apotheken.
Wer meine Artikel zum Cutler-Protokoll und den 3 Phasen der Entgiftung gelesen hat, kann sich sicher Vorstellen, das 250 mg DMPS als Infusion etwas auslösen können, was Niere & Co. nicht mehr über Tubuli, Membrantransporter & anderes bewältigen können -> eine massive Mobilisation von Hg, Kupfer oder auch Blei und Antimon, welche die Niere bewältigen muss. Genau deswegen gehen Infusionen mit DMPS auch öfters schief. So geht das Cutler-Protokoll denn auch einen anderen Weg mittels einer ‚low dose frequent chelation‘, meint: Niedrig dosiert, aber öfters (bzw. regelmäßig). Übliche Dosierungen liegen dann hier auch im Bereich 1-25 mg, maximal jedoch bei 50 mg DMPS oder auch DMSA pro Einzeldosis.
>>>> Ja, richtig gelesen – einige Menschen fangen mit 1-5 mg DMPS oder DMSA (6 bzw. 3 Stunden) an! <<<<<
Deswegen: Ich selber würde nichts übertreiben, was ich nicht ungeschehen machen kann. Ich bleibe „auf dem Teppich“ – fange, wie auch Cutler es schreibt, niedrig an und steigere (sehr) langsam. Kapseln entweder als
- Rezepturherstellung aus der Apotheke (per Arzt-Rezept,
- Hinweis: Die 100 mg ist als Einmaldosis aus meiner und Cutlers Sicht viel zu hoch.
- Eigenbau aus 100 mg Spenderkapseln (brauchen auch ein Arzt-Rezept).
- Tipp: Diese aber wegen der Oxidation schnell verbrauchen bzw. im Schraubglas im Gefrierschrank lagern.
- oder anderweitig, z.B. aus „UK“ bei Mandy M**t
- wobei diese Pakete natürlich auch vom Zoll angeschaut werden könnten, so das man sich sicher sein sollte ob der Import „legal“ ist.
Wer nicht in der EU lebt, der kann es ggf. auch direkt bei Living Supplements in Südafrika versuchen – ohne Garantie natürlich. Die lokale Gesetzgebung beim Import von ggf. verschreibungspflichtigen Dingen ist zu beachten, denn hilfreiches wird leider oft stark reglementiert, wobei jeder im Baumarkt Ultragifte kaufen kann und legal auf seinem Grundstück ausbringen darf!
Nebenwirkungen & Kritiken zu DMPS und DMSA
Wer viel Sucht, der wird auch Kritik zu DMPS & Co. finden – u.a. auf der sehr, sehr alten Webseite ‚DMPS Backfire‘ [23]. Dort wird auch der von mir geschätzte Thomas E. Levy, MD folgend zitiert (übersetzt mit deepl.com):
„Schwermetall-Chelatoren beschleunigen fast immer die Entgiftung des Post-TDR-Patienten (Total Dental Revision). DMSA, DMPS und EDTA können dies alle tun. DMPS ist hier durchweg der größte Übeltäter. Nach nur einer Injektion von DMPS kann es wochen- und manchmal sogar monatelang zu Immundefekten und klinischen Erkrankungen kommen.“
Die gleiche Webseite weist darauf hin, das Nebenwirkungen durch DMPS u.a. auch durch eine vorliegende Kupfer-Vergiftung verursacht werden können (-> Morbus Wilson) [24]. Die Kritiken machen aus meiner Sicht jedoch nur klar, das eine Nutzung von pharmazeutischen Chelatoren erst begonnen werden sollte, wenn auch alle Vorbereitungen in Bezug auf die Organe und die Herstellung der Ausleitungsfähigkeit erledigt sind. Auch Cutler [35, Seite 150] bestätigt Todesfälle in Zusammenhang mit der Anwendung von DMPS – aber nur, wenn dies per Injektion bzw. Infusion (in hohen Dosen) verabreicht wird.
In Bezug auf die Nebenwirkungen findet sich dann u.a. für DMSA [2][13]:
- Metallischer Geschmack (häufiger),
- gastrointestinale Symptome in bis zu 20 % der Patienten: Erbrechen, Durchfall,
- allgemeine Symptome (Kopfschmerzen, Rückenschmerzen, etc.) ca. 15 %,
- GOT- und GPT- Erhöhungen in ca. 10 % der Patienten,
- moderate Neutropenie, 1– 2 %,
- Arrhythmien, ca. 2 %,
- Paraesthesien,
- Hautreaktionen,
- vorübergehend Diarrhö [12],
- Anekdotisch: Knochenschmerzen (ab 5 mg), besonders an den Fußsohlen.
Retzek merkt an, das DMSA wohl eher die Leber belastet und bei Problemen mit der Leber hier auf diesen Chelator verzichtet werden sollte bzw. eine ausreichende Leberfunktion sichergestellt sein muss. Cutler merkt an, das wenn während der Therapie eine Hefe- oder Pilzinfektion auftritt oder fortschreitet, eine Neutropenie zu vermuten ist (da DMSA Neutrophile abtötet, was eine seltene, gefährliche, aber bekannte Nebenwirkung von DMSA ist) und eine Agranulozytose auftreten kann (-> nahezu vollständiger Mangel an Granulozyten im Blut). Dies speziell bei hohen Dosen an DMSA (>= 200 mg), wenn diese nur gelegentlich eingenommen werden. Allerdings kann dies auch bei DMPS auftreten. [35, Seite 150].
Bei DMPS heißt es u.a. [13] (deepl.com): „Es wurden keine schwerwiegenden unerwünschten Wirkungen nach Verabreichung von DMPS bei Menschen oder Tieren berichtet“. Als leichte Nebenwirkungen werden u.a. beschrieben [13]:
- Magen-Darm-Beschwerden,
- erhöhte Leberenzyme (u.a. GOT, GPT),
- leichte Neutropenie,
- Hautreaktionen.
Zudem können wohl einige Patienten, insbesondere solche mit allergischen Asthma Symptomen, eine Überempfindlichkeit gegen DMPS entwickeln [13]. Cutler schreibt zu DMPS noch, das Probleme mit Hefepilzen bei DMPS geringer sind als bei DMSA (deepl.com):
„Oftmals wird die Verwendung von DMPS subjektiv als angenehmer und komfortabler empfunden. Auch scheint DMPS weniger Hefeprobleme aufzurühren.“
Wie auch immer: Wird auf die dosisbezogene Effektivität der oralen Chelatoren geschaut, auf die LD50-Werte, die Nebenwirkungen – dann kann ich nur folgern, u.a. aus eigener Erfahrung, das DMPS der sichere und bei Hg-Belastungen auch effektivere der beiden hier vorgestellten Chelatoren ist [3][13]. Gerade die intestinalen Nebenwirkungen auf Darmflora & Co., speziell wohl auch bei Candida, sind ein Problem von dem ich bei dem Einsatz von DMSA höre.
Mein Fazit
DMPS und DMSA sind keine idealen Chelatoren und keine Allheilmittel bei Belastungen mit Schwermetallen und Quecksilber. Beide Chelatoren sind nicht Fettlöslich, überwinden nicht die Blut-Hirn-Schranke und ‚gehen‘ nicht Intrazellulär – zumindest nicht relevant. Klar ist jedoch, das beide das Hg im Blut und in vielen Organen direkt, und im Gehirn auch (sehr langsam) indirekt, senken können [4].
Bei DMPS, eingenommen nach dem Cutler–Protokoll Schema [35], zusammen mit Bindemitteln, nach Abklärung und ggf. Behandlung einer HPU, einem Blut- und Haar-Test und dem Auffüllen der Mikronährstoff-Depots sowie der Unterstützung von Leber (u.a. Mariendistel, Sylibin, Silmarin) und Niere (u.a. Solidago), sind mir persönlich keine Probleme in der bekannt – zumindest nicht, wenn mit oralen Dosierungen ab 1-5 mg gestartet und langsam bis ggf. 25 mg, pro Einzeldosis gesteigert wird. Dieses reflektieren dann auch verschiedene Studien [3][13]. Auch Cutler schreibt [35, Seite 150] (übersetzt mit deepl.com):
„Oral verabreichtes DMPS lindert die Symptome rascher und vollständiger als DMSA für die Dauer der Therapie“ und „Es wird oft von Menschen vertragen, die DMSA nicht vertragen„
DMSA würde ich selber nur bei hohen Co-Belastungen mit Blei, und dann auch nur intervallweise nutzen. Dies, da hohe Belastungen mit Blei meist mit einer erhöhten Mobilisation aus den Knochen in Zusammenhang stehen und das Blei dort nur langsam mobilisiert wird. Weiterhin vergrößert eine chronische Zufuhr von DMSA den Ausbruch einer Pilz- oder Candida-Belastung im Darm und belastet die Niere im Falle das diese nicht 1a funktioniert. Eine erhöhte Ca-Mobilisation mit gesteigerter Blei-Freisetzung aus den Knochen, welche eher nicht wünschenswert ist, hat ihre Ursache oft bei Problemen mit der Nebenniere und dem Calcium-Stoffwechsel – u.a. viel Calcium und/oder Vitamin D3, aber kein oder wenig K2. Natürlich gibt es auch hohe ‚akute‘ Blei-Belastungen, z.B. bei Sportschützen oder Polizisten mit vielen Aufenthalten auf dem Schießstand.
In jedem Fall sind bei einer Ausleitung per DMPS und DMSA konstant die Leber und Nierenwerte (Blut) zu überprüfen. Falls sich diese zu stark verschlechtern, sollte ggf. die Dosis gesenkt und auf mehr Unterstützung von Leber & Niere und der Phase III der Entgiftung (-> Membrantransporter), z.B. über Bitterstoffe und spezifische Nrf2-Aktivatoren, geachtet werden. Nach Retzek geht DMPS über die Niere und DMSA über die Leber – was in Bezug auf die individuellen Probleme beachtet werden sollte.
Zu den Limitationen von DMPS & DMSA – aber auch Vorsicht bei ALA und NAC
Letztendlich braucht es für die intrazelluläre Mobilisierung von Hg, insbesondere im Gehirn, fettlösliche Chelatoren wie ggf. Irminix (NMBI) [30][31][33], alternativ Mobilisatoren mit Chelatoren-Eigenschaften, wie u.a. wohl die Alpha-Liponsäure (ALA) bzw. ihre reduzierte Form DHLA. Interessant ist an ALA, das diese gleichzeitig noch Glutathion ‚recycelt‘ (-> reduziert), die antioxidativen Systeme und die Entgiftungs-Systeme der Phase II & III hochreguliert (-> u.a. über Nrf2-Induktion). Genau deswegen nutzt das Cutler-Protokoll [35] auch RS-ALA als primären Chelator – wobei DMPS bzw. DMSA vorbereitend und später begleitend eingesetzt werden.
Auch Sears [37] merkt so treffend an, das Alpha-Liponsäure (ALA) nicht nur andere Antioxidantien (z. B. die Vitamine E und C sowie oxidiertes Glutathion) regeneriert – sondern auch eine metall-chelatbildende Wirkung hat- welche aufgrund der fett- und wasserlöslich von ALA vorsichtig eingesetzt werden muss, da es besondere Risiken der Umverteilung von Metallen birgt. So sein DMSA oder DMPS sind die oralen Medikamente der Wahl, wobei die gleichzeitige Anwendung von N-Acetyl-Cystein und ALA so lange vermieden bzw. vorbehalten bleiben sollte, bis der Patient die volle Dosis des Chelatbildner (an DMPS bzw. DMSA) verträgt und die ausgeschiedenen Metallmengen deutlich gesunken sind. [37]
Die Ansicht von Sears [37] passt sehr gut zu Cutlers Aussagen [35] und spiegelt auch meine eigene Ansicht, basierend auf eigenen Erfahrungen und Rückmeldungen von anderen Menschen, wieder: ALA ist nicht nur aus meiner Sicht erst der zweite Schritt beim Hg-Detox und hat vorher strikt vermieden zu werden. Denn wenn DMPS oder DMSA in kleinen Dosen nicht vertragen werden, dann deutet das darauf hin, das etwas mit den Ausscheidungsorganen, der Detox-Genetik oder der Phase II und / oder III der Entgiftung nicht stimmt. Und wenn dort etwas nicht stimmt – sollte nicht auf den ‚Turbo-Knopf‘ der Entgiftung gedrückt werden.
Quellen/Links
- [1] Handbuch der Amalgamvergiftung: Diagnostik – Therapie – Recht., Max Daunderer, 1995
- [2] Durchführung, Referenzbereiche und Interpretation des DMPS-Testes – Eine kritische Datenanalyse, Dr. Wolfgang Bayer, Laboratorium für spektralanalytische und biologische Untersuchungen Dr. Bayer Gmbh
- [3] Comparison of chelating agents DMPS, DMSA and EDTA for the diagnosis and treatment of chronic metal exposure. Blaurock-Busch, E.. (2014)., British Journal of Medicine and Medical Research. Doi: 10.9734/BJMMR/2014/6875.
- [4] A Review on Coordination Properties of Thiol-Containing Chelating Agents Towards Mercury, Cadmium, and Lead, Geir Bjørklund et al., Molekules, Molecules. 2019 Sep; 24(18): 3247., Published online 2019 Sep 6. doi: 10.3390/molecules24183247
- [5] Chronische Metallintoxikationen – Diagnosestellung und Therapie mit und ohne Chelatoren, Dr. Patrick Assheuer, Berlin, 18.11.2017
- [6] Metall-Detox in der Krebstherapie, Von Dr.med. Helmut B Retzek, August 17, 2018
- [7] Entgiftungscheckliste von Daunderer, Toxcenter
- [8] Risikoreduktion bei onkologischen Patienten durch Metallausleitung als Intervalltherapie., Fr. Professor Eleonore Blaurock-Bush, AZN 1/10
- [9] Fachinformationen DMPS (Dimaval) 100 mg Oral, Heyl
- [10] DMSA – die sanfte und effektive orale Entgiftung, Dr. rer. nat. Eleonore Blaurock-Busch, OM & Ernährung, 2011, Nr. 134
- [11] Medical Countermeasures—Chelation Therapy, Govinder Flora et al, Handbook of Arsenic Toxicology, 2015, Pages 589-626, doi: 10.1016/B978-0-12-418688-0.00026-5
- [12] Clinical Environmental Medicine – Identification and Natural Treatment of Diseases Caused by Common Pollutants, Walter J. Crinnion und Joseph E. Pizzorno, Elsevier; Auflage: 1 (26. April 2018)
- [13] Chelation in Metal Intoxication, Swaran J.S. Flora* and Vidhu Pachauri, Int J Environ Res Public Health. 2010 Jul; 7(7): 2745–2788., Published online 2010 Jun 28. doi: 10.3390/ijerph7072745
- [14] Pharmacokinetics of meso-2,3-dimercaptosuccinic acid in patients with lead poisoning and in healthy adults., Dart RC1, Hurlbut KM, Maiorino RM, Mayersohn M, Aposhian HV, Hassen LV., J Pediatr. 1994 Aug;125(2):309-16., doi: 10.1016/s0022-3476(94)70217-9
- [15] Impact of Organic Anion Transporter 3 (OAT3) on renal transport of the metal chelator 2,3-Dimercapto-1-propane-sulfonate (DMPS), Matthias Rödiger et al., Can J Physiol Pharmacol. 2010 Feb; 88(2): 141–146., doi: 10.1139/Y09-123
- [16] Interaction of 2,3-Dimercapto-1-propane Sulfonate with the Human Organic Anion Transporter hOAT1, Florian Islinger, and
- [17] Chelation: Harnessing and Enhancing Heavy Metal Detoxification—A Review, Margaret E. Sears, ScientificWorldJournal. 2013; 2013: 219840., Published online 2013 Apr 18. doi: 10.1155/2013/219840
- [18] Mercury binding to the chelation therapy agents DMSA and DMPS and the rational design of custom chelators for mercury, G.N. George, R.C. Prince, J. Gailer, G.A. Buttigieg, M. Bonner Denton, H.H. Harris, I.J. Pickering, Chem Res Toxicol, 2004 Aug;17(8):999-1006. doi: 10.1021/tx049904e.
- [19] Insights on alpha lipoic and dihydrolipoic acids as promising scavengers of oxidative stress and possible chelators in mercury toxicology, Geir Bjørklunda et al., Volume 195, June 2019, Pages 111-119, Journal of Inorganic Biochemistry, doi: 10.1016/j.jinorgbio.2019.03.019
- [20] MRP2 and the DMPS- and DMSA-Mediated Elimination of Mercury in TR− and Control Rats Exposed to Thiol S-Conjugates of Inorganic Mercury, Christy C. Bridges et al., Toxicol Sci. 2008 Sep; 105(1): 211–220., Published online 2008 May 28. doi: 10.1093/toxsci/kfn107
- [21] Entgiftung: Effektiv bei vielen Krankheiten, Joachim Mutter, OM – Zs. f. Orthomol. Med. 2016; 4: 5–15
- [22] MRP2 involvement in renal proximal tubular elimination of methylmercury mediated by DMPS or DMSA, Rudolfs K Zalups, Christy C Bridges, Toxicol Appl Pharmacol, 2009 Feb 15;235(1):10-7.,doi: 10.1016/j.taap.2008.11.003. Epub 2008 Nov 19.
- [23] The Truth about DMPS, DMPS Backfire.com
- [24] The Interaction of copper (Cu++) with the erythrocyte membrane and 2,3-dimercaptopropane-sulfonate in vitro: a source of activated oxygen species., Aaseth, J, Ribarov, S, Bacher,P Pharmacol Toxicol 1987 Oct.; 61(4): 250-3., doi: 10.1111/j.1600-0773.1987.tb01813.x
- [25] DMPS can reverse the features of severe mercury vapor-induced neurological damage, Sally M Bradberry, Case Reports, Clin Toxicol (Phila), . 2009 Nov;47(9):894-8., doi: 10.3109/15563650903333812.
- [26] The Mt. Diwata study on the Philippines 2000-treatment of mercury intoxicated inhabitants of a gold mining area with DMPS (2,3-dimercapto-1-propane-sulfonic acid, Dimaval), S Böse-O’Reilly et al., Sci Total Environ, 2003 May 20;307(1-3):71-82., doi: 10.1016/s0048-9697(02)00547-8.
- [27] Quecksilber-Entgiftung – mein Standpunkt – und Pubmed, Dr.med. Helmut B Retzek, Februar 8, 2015
- [28] The therapeutic use of 2,3-dimercaptopropane-1-sulfonate in two cases of inorganic mercury poisoning, J R Campbell et al., JAMA, 1986 Dec 12;256(22):3127-30.
- [29] DMPS (2,3-dimercaptopropane-1-sulfonate, dimaval) decreases the body burden of mercury in humans exposed to mercurous chloride, D Gonzalez-Ramirez et al., J Pharmacol Exp Ther, 1998 Oct;287(1):8-12.
- [30] Amelioration of Acute Mercury Toxicity by a Novel, Non-Toxic Lipid Soluble Chelator N,N′bis-(2-mercaptoethyl)isophthalamide: Effect on Animal Survival, Health, Mercury Excretion and Organ Accumulation, David Clarke, Roger Buchanan, Niladri Gupta and Boyd Haley, Toxicol Environ Chem. 2012; 94(3): 616–640., doi: 10.1080/02772248.2012.657199
- [31] Treating Mercury Toxicity With Emeramide – Interview With Boyd Haley, Dr. Mercola, 10.03.2019
- [32] Handbook of Arsenic Toxicology Chapter 26 – Medical Countermeasures—Chelation Therapy, Govinder Flora et al., Handbook of Arsenic Toxicology, 2015, Pages 589-626, DOI: 10.1016/B978-0-12-418688-0.00026-5
- [33] Boyd Haley PhD explains the limitations of chelators DMPS, DMSA and EDTA, Mercury Exposure, 20.04.2011
- [34] Vitamin C, Glutathione, Or Lipoic Acid Did Not Decrease Brain Or Kidney Mercury In Rats Exposed To Mercury Vapor, H. Vasken Aposhian, Daniel L. Morgan, H. L. Sam Queen, Richard M. Maiorino & Mary M. Aposhianm, Journal Journal of Toxicology: Clinical Toxicology Volume 41, 2003 – Issue 4, Pages 339-347, Published online: 06 Feb 2003, doi: 10.1081/CLT-120022000 (Anm.: Diese Studie hat brutale Schwächen im Design… die Aussagen im Titel und Abstract sind irreführend.)
- [35] Amalgam Illness: Diagnosis & Treatment: What You Can Do to Get Better, How Your Doctor Can Help You, Andrew Hall, Ph.D. Cutler , 1. Juni 1999
- [36] Mercury toxicity and antioxidants: Part 1: role of glutathione and alpha-lipoic acid in the treatment of mercury toxicity., Patrick L., Altern Med Rev. 2002 Dec;7(6):456-71.
- [37] Chelation: Harnessing and Enhancing Heavy Metal Detoxification—A Review, Margaret E. Sears, ScientificWorldJournal. 2013; 2013: 219840., Published online 2013 Apr 18. doi: 10.1155/2013/219840
- [38] The role of thiols, dithiols, nutritional factors and interacting ligands in the toxicology of mercury, James P K Rooney, Toxicology, 2007 May 20;234(3):145-56., doi: 10.1016/j.tox.2007.02.016. Epub 2007 Mar 1.
- [39] Human studies with the chelating agents, DMPS and DMSA, H V Aposhian et al., J Toxicol Clin Toxicol, 1992;30(4):505-28., doi: 10.3109/15563659209017938.
- [40] Re: Natural Products for mercury removal, And Cutler, Date: Fri, 23 Jun 2000
- [41] Influence of 2,3-dimercaptopropane-1-sulfonate and dimercaptosuccinic acid on the mobilization of mercury from tissues of rats pretreated with mercuric chloride, phenylmercury acetate or mercury vapors, J P Buchet, Comparative Study Toxicology, 1989 Mar;54(3):323-33. doi: 10.1016/0300-483x(89)90067-x.
- [42] Mechanisms involved in the transport of mercuric ions in target tissues, Christy C. Bridges et al., Arch Toxicol. 2017 Jan; 91(1): 63–81., Published online 2016 Jul 15. doi: 10.1007/s00204-016-1803-y
- [43] Untersuchungen zur Mono-DMPS Mobilisationstherapie im Vergleich zur DMPS-ZnDTPA Kombinationstherapie bei der Schwermetallentgiftung, E. Blaurock-Busch, Micro Trace Minerals Laboratory, umwelt·medizin·gesellschaft, Ausgabe 25, April 2012
Der Rest dieses Beitrages ist nur für eingeloggte Freunde des Blogs einsehbar. Bitte logge Dich ein, oder schaue unter dem Menüpunkt 'Freunde des Blogs' für weitere Informationen wenn ein ernsthaftes Interesse besteht hier weiter zu lesen.








Neuste Kommentare