Eisen-Update Teil 4: Blutwerte im Detail: Hb, Hk, Ery, MC(H/V/CH), Serum-Ferritin, Transferrin (TfS), sTfR, Ferritin-Index, ZnPP, Vitamin A, Kupfer, Coeruloplasmin, CRP & Co.
Blutwerte – was gibt es zu messen? Quelle: Pixabay
Eine (Funktions-) Eisenmangelanämie zeigt sich u.a. durch einem Abfall des Hämoglobingehaltes (Hb < 12 bzw. 13 g/dl) in den roten Blutkörperchen (↓MCH) sowie einer Verkleinerung der Erythrozyten (↓MCV). Dies ist allerdings bereit die 2te „akute“ Stufe einer Mangelsymptomatik.
Um einen Speicher- bzw. Funktions-Eisenmangel vor einsetzten der Anämie bzw. schlechten Blutwerte bei Hb & Co. zu erkennen, bedarf es dem Einsatz von spezifischen Blut- bzw. Laborwerten. Zudem gilt es die verschiedenen Ursachen zu unterscheiden, denn nicht immer fehlt Eisen! Das ist ganz wichtig, denn mit Eisen als Ergänzung spaßt man nicht. Eisen wird niemals „einfach mal so“ oder ohne genauen Grund ergänzt. Nie! Deswegen sollte man auch keine K***** Cornflakes & Co. essen, wo Eisen in sehr ungünstiger Form zugesetzt wird.
In diesem 4ten Teil der Eisen-Update Serie möchte ich deswegen alle mir bekannten eisenrelevanten Blutwerte betrachten und schauen welche Aussagen sich von diesen „wirklich“ ableiten lassen. Ich „will richtige Studien haben“, welche optimalerweise eine Biopsie des Knochenmarks anstellten, also da, wo die roten Blutkörperchen gebildet werden, und schauten wie viel Eisen wirklich „in den Speichern“ ist. Nur so ist (halbwegs) klar „was Sache“ ist und die ermittelten Blutwerte können in einem ungefähren Zusammenhang betrachtet werden. Also keine komplette „Spekulatius“-Wissenschaft, von der es genug gibt.
Das Problem: Es gibt so viele „Eisen“-Blutwerte, das ich und viele Therapeuten „den Wald vor lauter Bäumen nicht mehr sehen“ und deswegen das Risiko von Fehldiagnosen hoch ist. Dies ist bei Eisen komplexer, da es verschiedene Ursachen gibt und viele Eisen-Werte stark entzündungsabhängig sind. Folgendes gilt es in der Regel zu unterscheiden:
- Alles Super!
- Sehr niedriges Speichereisen ohne Anämie (EoA), aber ggf. schon Auswirkungen auf einige eisenabhängige Prozesse.
- Anm.: Noch genug Funktionseisen für Häm/Hb > 12/13 g/dl. Ggf. Mangel von 500-1000 mg Eisen [21]. Ursachen finden, Ernährung optimieren, ggf. Eisen ergänzen (eher Oral).
- den realen Eisen-Mangel (-> Iron Deficiency Anemia, IDA),
- den funktionellen Eisen–Mangel (-> Anemia of chronic Diseases, ACD) wo das Eisen da „aber eingesperrt“ ist,
- Mangel an Co-Faktoren für den Eisen-Metabolismus (u.a. fehlendes Retinol oder Kupfer) und
- den Eisen-Überschuss.
Als Blutwerte herangezogen werden können: Hämoglobin (Hb), MCH, MCV, MCHC, Hämatokrit (Hk), Erythrozyten (Ery), Serum-Ferritin, Serum-Eisen, Transferrin, Transferrin-Sättigung (TfS), Löslicher Transferrin Rezeptor (sTfR), sTfR-Index, Zinkprotoporphyrin, hsCRP, IL-6, Vitamin A (Retinol) Kupfer (Serum), Ceruloplasmin und auch Hepcidin.
Die Liste ist natürlich nicht komplett, weil es auch Gen-Polymorphismen, also genetische Varianten und Erbkrankheiten gibt, die sich auf den Eisen-Metabolismus auswirken und oft zu einer Eisen-Akkumulation führen. Die genetischen Aspekte sind jedoch nicht Umfang dieses Artikels.
Um zu der Deutung der Blutwerte bzw. einem Diagnose-Schema zu kommen (-> in Teil 5 dieser Serie), sollte erst einmal die Wissenschaft hinter den Blutwerten in Bezug auf Eisen, Kupfer und Retinol verstanden werden, soweit dies für den ambitionierten Hobbyforscher möglich ist. Wie bereits in Teil 1 des Eisen-Updates vorgestellt, ist die Eisen-Regulation etwas komplexer, was einer etwas breiteren Schau auf die Blutwerte bedarf. In Eisen-Update Teil 3 bin ich bereits auf Serum-Ferritin eingegangen, und die unterliegenden Krankheiten welche einen realen Eisenmangel bedingen können. Teil 3 offenbarte jedoch auch, das Serum-Ferritin ein etwas „unscharfer“ Laborwert mit einem potentiell großen Graubereich ist.
In diesem Artikel möchte ich deswegen die zu Grunde liegenden Studien zum Serum-Ferritin mit etwas mehr Details vorstellen sowie die restlichen eisenrelevanten Blutwerte beleuchten, wozu ich mich durch dutzende von Original-Studien „gefräst“ habe. Vertiefen möchte ich jedoch „nur“ 6 Stück davon:
- Eisen, Kupfer im Kontext des großen Blutbildes, TIBC und der Transferrin-Sättigung – Wintrobe et al., 1954
- Serum-Ferritin in Männern und Frauen – Jacobs et al. 1972
- Serum-Ferritin Werte in Relation mit denen aus einer Knochenmark-Aspiration – J. Mazza et al. 1978
- Die Hepcidin-Ferritin-CRP Studie bei entzündlichen Darmerkrankungen – Mecklenburg et al. 2014
- Die sTfR-log-Ferritin-Index (FI) Studie von Punnonen et al. 1997
- Unterschiedliche Test-Kits für sTfR, Thomas et al. 2002
Bevor ich mit den Studien beginne, werde ich jedoch kurz die gängigen Blutwerte für die Bewertung des Eisen-Kupfer-Metabolismus aufführen:
- Übersicht über die Eisenrelevanten Messwerte und Parameter im Blutbild
- Löslicher Transferrin-Rezeptor (sTfR): Einblick in den aktuellen Eisenbedarf
- Zinkprotoporphyrin (ZnPP) Beurteilung des Eisenstatus an der Häm-Synthese
- Transferrin und Transferrin-Sättigung
- Retinol-Status und Eisen (bzw. Serum-Ferritin)
Am Ende des Artikels folgt dann mein übliches Fazit.
Hinweis: Hier geht es zum Eisen-Übersichtsartikel
Inhaltsverzeichnis für den Schnellzugriff
Übersicht über die Eisenrelevanten Messwerte und Parameter im Blutbild
Vorab: Dieser Artikel ist ein Schwergewicht, denn ich möchte hier „etwas“ tiefer graben, schauen wie Referenzwerte teils zu Stande kamen, was Ihre die Limitationen sind, welche etwas taugen und unter welchen Bedingungen Sie ggf. sinnvoll einzusetzen sind.
Die Referenzwerte der nachfolgenden Übersichts-Tabelle haben ich, soweit möglich, meinen Blutanalysen bei GanzImmun entnommen [u.a. 20]. Dabei ist zu beachten, das diese je nach Alter, Geschlecht, eingesetztem analytischem Verfahren bei „Spezialwerten“, Labor, Region und Land leicht unterschiedlich sein können. Dies, da sich viele Referenzwerte aus der Kohorte der Menschen berechnen, die sich testen lassen.
Den Anfang der kurzen Übersicht machen die Werte des kleinen (und teils des großen) Blutbildes. Zum Ende des Artikels gehe ich dann noch im Detail auf die Werte ein. [19][20]
| Parameter | Beschreibung | Normwerte |
|---|---|---|
| Hämoglobin (Hb) | Ein Protein in den roten Blutkörperchen, das für den Sauerstofftransport im Körper verantwortlich ist. Ca. 70% des Eisens im Körper in an Hb gebunden. Bei Werten < 12 g/dl (Frauen) bzw. < 13 g/dl (Männer) liegt eine leichte, bei < 10 g/dl eine schwere Anämie vor. Hb reagiert jedoch erst Spät auf eine Anämie. | Männer: 13,5-17,8 g/dL Frauen: 11,5-16 g/dL |
| Hämatokrit (Hk) | Der prozentuale Anteil der roten Blutkörperchen im Blut, der Informationen über das Blutvolumen liefert. ↓ Anämie o. zu wenig Flüssigkeit | Männer: 40%-53% Frauen: 35%-46% |
| MCH | Der durchschnittliche Gehalt an Hämoglobin pro rotem Blutkörperchen, der die Sauerstofftragfähigkeit der Zellen anzeigt. ↓↑ Siehe Anm. | 28-33 pg |
| MCV | Das durchschnittliche Volumen eines einzelnen roten Blutkörperchens, das Aufschluss über die Größe der Erythrozyten gibt. ↓↑ Siehe Anm. | 80-96 fL |
| MCHC | Die durchschnittliche Konzentration von Hämoglobin in einem gegebenen Volumen roter Blutkörperchen, die die Sättigung der Zellen mit Hämoglobin misst. ↓↑ Siehe Anm. | 33-36 g/dL |
| Erythrozyten (Ery) | Die roten Blutkörperchen, die für den Transport von Sauerstoff und Kohlendioxid zwischen den Lungen und dem Rest des Körpers zuständig sind. ↓ Blutarmut/Anämie. | Männer: 4,4 bis 5,9 Mil. Zellen/µL Frauen: 4,1-5,4 Mil. Zellen/µL |
| Ery-Verteilungsbreite (EVB, engl. RDW) | Maßeinheit für die Größenverteilung der roten Blutkörperchen (Erythrozyten), berechnet aus der Standardabweichung des Volumens und MCV. Wenn MCH, MCV ↓ sind kann eine ↑ EVB auf Anämie (ggf. Eisenmangel) und eine ↓ auf ggf. Thalassämie hinweisen. | 11,5% bis 14,5% |
| Leukozyten | Die weißen Blutkörperchen, die eine zentrale Rolle im Immunsystem des Körpers spielen und vor Infektionen und Krankheiten schützen. ↓ ggf. Folat, Vitamin B12-Mangel, Kupfer-Mangel [1] ↑ = Akute und chronische Infekte durch Bakterien und Pilze. | 3,9-10,9 Zellen/pl |
| Monozyten (Abs.) | Untergruppe der Leukozyten, die eine wichtige Rolle im Immunsystem spielen. ↓ seltener, u.a. ach schweren Infektionen, ggf. Kupfer-Mangel [1] ↑ = Akute und chronische Infekte (u.a. Parasiten, „Viren“, Bakterien). | 0,2-0,8 Monozyten /pl |
| Retikulozyten | Junge rote Blutkörperchen, deren Anzahl und Reife Aufschluss über die Produktion neuer Erythrozyten im Knochenmark geben. Normal erniedrigt bei Kupfer- und Eisenmangel, wobei es bei verminderter Produktion von roten Blutkörperchen (Ery, Hk) zur relativen Erhöhung kommen kann [1]. ↓↑ ggf. Folat, Vitamin B12-Mangel, Erythropoteinmangel (Niere) ↑ auch hämolytische Anämie, Behandlung Eisenmangel | 0,5%-2,5% der Ery |
Anm.: Niedriges MCH, MCV, MCHC wird auch mit einem möglichen Vitamin B6-Mangel (-> HPU) verbunden und jeweils hohe Werte mit einem Mangel an B12 und Folat. Sind Hb, MCH, MCHC und Ret niedrig, ggf. später auch MCV, dann wird von einem (funktionellen) Eisenmangel ausgegangen. Aber:
- Es kann ein realer Mangel an Funktions-Eisen (IDA) vorliegen oder
- ein funktionaler Mangel (ACD), bei dem das (ausreichend Vorhandene) Eisen aus den Speicher nicht entsprechend mobilisiert werden kann, z.B. wegen chronischen Entzündungen oder der Eisen-Transport eigeschränkt ist (z.B. wegen akutem Retinol-Mangel).
Nun die Eisen-Diagnostik spezifischen Werte, wobei ich „Extravaganzen“ wie Eisen im Vollblut nicht aufführe, da dieses in Studien faktisch nicht verwendet wird und sich so keine Rückschlüsse über Referenzwerte, Dynamik und Tauglichkeit ziehen lassen. Zudem ist Eisen im Blut stark reguliert und gibt keinen Aufschluss über die Speicher.
| Parameter | Beschreibung | Normwerte |
|---|---|---|
| Eisen (Serum) | Ein Maß für die Menge an (momentanen) Eisen im Blut, das für die Bildung von Hämoglobin und den Sauerstofftransport essentiell ist. Ist im Falle von Entzündungen/Infekten (Akut-Phase) oft erniedrigt weil der Körper die Eisenfreisetzung reduziert. 65 µg/dl sollten es aus meiner Sicht jedoch schon sein. | 22-158 µg/dl im Serum |
| Ferritin (Serum) | Ein (indirekter) Indikator für die ungefähr gespeicherte Eisenmenge im Körper. Akut-Phase Protein und abhängig von Entzündungsprozessen und dann tendenziell erhöht, weil der Körper Eisen in den Speichern zurückhält. ↑ bei Tumor-/Infektanämie, Eisenüberladung, Leberkrankheiten, ↓ bei prälatentem (Speicher-) Eisenmangel. Niedrige Werte (z.B. ~ 18 ng/ml) müssen keinen Mangel an Funktionseisen bedeuten. Werte > 100 ng/ml finde ich nicht mehr optimal, > 150 ng/ml ungut. | Männer: 22-322 ng/ml; Frauen: 10-291 ng/ml |
| Löslicher Transferrin-Rezeptor (sTfR) | Ein Marker, der die Menge an (löslichen) Transferrin-Rezeptoren im Blut misst, die bei „andocken“ von Transferrin an eine Zelle freigesetzt werden, was auf den Eisenbedarf der Zellen hinweist. Je größer der Eisenmangel ist, desto mehr Rezeptoren werden ausgebildet. Eine Abspaltung kann auch ohne Bindung von (mit Eisen geladenem) Transferrin erfolgen, denn auch „leeres“ (Apo-) Transferrin kann an den Rezeptor binden und den löslichen Teil freisetzten. sTfR ist zudem weitgehend frei von Störeinflüssen wie Entzündungen, Tumore, Schwangerschaft etc. Werte ab 3, ggf. auch 2, können in Einzelfällen schon Eisemangelanämie haben [12]. | 1,9-4,4 mg/l |
| sTfR-Index | Eine Berechnung, die den sTfR-Wert (mg/l) durch das Serum-Ferritin (µg/L bzw. ng/ml) teilt, um den Eisenstatus genauer zu beurteilen. Nach Purronen et al. [12] dem sTfR-log-Ferritin-Index deutlich unterlegen. Referenzwerte sind zudem Test- bzw. Laborspezifisch. | < 1,0: Eisen Normal 1,0-2,0: Grenzbereich >2.0: Eisen Erhöht |
| sTfR-Log-Ferritin-Index (FI) | Eine Berechnung, die den sTfR-Wert durch log(Serum-Ferritin) teilt, um den Eisenstatus genauer zu beurteilen. Anm.: Logarithmus zur Basis e des Ferritinwerts. Dieser Wert gilt Serum-Ferritin als Einzelwert, sowie allen anderen Markern, als überlegen um einen wirklichen Mangel an Funktionseisen (als „momentan-Eisen“) zu beweisen [12]. Referenzwerte sind Test- bzw. Laborspezifisch! | < 3,2: Eisen Normal >3.2: Eisen Unzureichend. >2 bei CRP>5 mg/l |
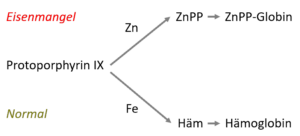
| Zinkprotoporphyrin (ZnPP) | Zinkprotoporphyrin (ZnPP) wird vermehrt bei Eisenmangel gebildet, wenn Zink anstatt statt Eisen als Zentralatom genutzt wird um Hämoglobin zu bilden. ↑: bei Eisenmangel, Bleivergiftung. Dieser Wert ist (Entzündungs-) Akut-Phase unabhängig, kann jedoch nicht zwischen IDA und ACD unterscheiden. | < 40 µmol/mol Hb: Normalbereich 40-80 µmol/mol Hb: Graubereich > 80 µmol/mol Hb: Eisenmangel |
| Transferrin (Serum) | Ein Protein, das Fe3+ Eisen im Blut transportiert und dessen Niveaus Aufschluss über den Eisenmetabolismus geben. ↑ bei Eisenmangel, Schwangerschaft, Frühphase der Hepatitis; ↓ bei Entzündungen (Akut-Phase), Eiweißverlusten, Leberzirrhose, Störungen der Hb-Synthese (z.B. ß-Thalassämie). Nutze ich nur noch als zusätzliche Kontrolle, weil Spezifizität geringer [5][12] | 215-365 mg/dl |
| Transferrin-Sättigung (TfS in %) | Der Prozentsatz des Transferrins, der mit Eisen gesättigt ist. Berechnet wird der Wert aus Eisen (Serum) und TIBC oder Transferrin (TfS [%] = Eisen (Serum) [µg/dl] / Transferrin [mg/dl] x 70,9). ↑ bei Hämolyse, Eisenverwertungsstörung, Störung der Hb-Synthese oder Eisenüberladung (Hämochromatose); ↓ bei Eisenmangel und Eisenverteilungsstörungen (Infekte, Tumoren, Leberschäden), Hereditäre Hypotransferrinämie. Entzündungsbeeinflusst. Werte unter <10% sind kritisch (Anämie, ggf. Mangelernährung, Zöliakie oder Darmerkrankungen wie Morbus Crohn). Ein hoher Wert >45% kann ein Indiz auf eine Eisenüberladung sein, u.a. auch die Erbkrankheit Hereditäre Hämochromatose[26]. Nutze ich nur noch als zusätzliche Kontrolle, weil Spezifizität geringer [5][12] | 16-45 %
Masterjohn [26] :30-40% |
| Retikulozyten-Hämoglobin (Ret-Hb, CHr, MRH) | Hämoglobingehalt der Retikulozyten. Geringe Werte legen Probleme mit der Hämoglobinbildung nahe. Da die Reifungszeit der Retikulozyten nur wenige Tage beträgt sind Veränderungen schnell ersichtlich. Bei Entzündungen und Akut-Phase Reaktionen erniedrigt. | Normal: 28-35 pg Hämoglobin (Hb) je Retikulozyt |
| TIBC / TEBK | Totale Eisenbindungs-Kapazität (TEBK bzw. Total Iron Binding Capacity). Wird als Einzelwert nicht mehr benutzt, geht in die Berechnung der Transferrin-Sättigung ein und wurde selber durch Transferrin ersetzt. Findet sich jedoch oft in älteren Studien zu Eisen. | |
| Hepcidin | Reduziert wenn erhöht, die Expression von Ferroportin und damit die Eisenfreisetzung aus Speichern (Ferritin, RES) sowie die Aufnahme aus den Darmzellen. Wird u.a. über IL-6 erhöht, durch realen Eisenmangel gesenkt. Zwar existieren verschiedene Tests, jedoch hat sich noch kein Standard-Verfahren durchgesetzt [18]. |
Serum-Ferritin (günstig) und der auf sTfR basierende (log) Ferritin-Index erscheinen mir als „beste“ Werte zur Bestimmung eines potentiellen realen Eisenmangels sowie einer Eisen-Mangelanämie (IDA), wenn weitere Blutwerte korrelieren (u.a. Hb, MCH, MCHC, Ret).
Dann gibt es noch die „Kupfer-Relevanten Werte“, welche geprüft werden können, wenn das mit den Eisenwerten irgendwie keinen Sinn ergibt, wie z.B. Anämie und gleichzeitig gute Eisenspeicher:
| Parameter | Beschreibung | Normwerte |
|---|---|---|
| Kupfer (Serum) | Die (aktuelle) Menge an Kupfer im Blut (Serum). Während einer Akut-Phasenreaktion kann der Kupferspiegel (im Serum) ansteigen. Bei Werten < 700 µg/l unbedingt Ceruloplasmin und Prüfen, Kupfermangel ausschließen. | 700-1400 µg/l |
| Vitamin A (Retinol) | Ein Maß für den Retinol Spiegel in der Leber, wobei niedrige oder hohe Werte nur bei bereits sehr leeren bzw. sehr (oder kritisch) vollen Speichern gemessen werden. Meint: Der Zahlenwert verhält sich nicht linear zur Menge des Retinol in der Leber. Werte unter 300, insb. 200, µg/l sind eindeutig mit niedrigen Ferritin-Werten assoziiert [23][24] und einer Ergänzung kann CP normalisieren [27], wenn genug Kupfer vorhanden ist. | 300-700 µg/l |
| Ceruloplasmin (CP) | Ein Protein, das Kupfer im Blut bindet, transportfähig macht (-> Umwandlung von Fe2+ -> Fe3+) und transportiert. Es ist extrem wichtig für den Eisen-Metabolismus. Abhängig von genug Kupfer und Retinol. Akut-Phase Protein, der Spiegel kann während einer Entzündung/Infektion deutlich ansteigen. Werte < 15-16 mg/dl weisen ggf. auch zu wenig bioverfügbares Kupfer oder andere Mängel hin. | 15,0-30,0 mg/dl |
Hinweis: Ist Retinol stark erniedrigt und/oder Kupfer unterhalb de Referenz, dann kann die Eisenverfügbarkeit durch einen Mangel an bioverfügbarem Kupfer ausgelöst sein. Dies ist aus meiner Sicht insbesondere der Fall, wenn (in Folge) auch Ceruloplasmin erniedrigt ist (< 16 mg/dl).
Zu guter Letzt sind noch die Entzündungsmarker und die Leberwerte wichtig, da einige Blutwerte abhängig vom Entzündungen anders ausfallen bzw. erhöht bzw. erniedrigt sind. Ich nutze dafür primär die folgenden und IL-6 nur nachrangig, wenn ggf. eine ACD abgeklärt werden muss und der sTfR-Log-Ferritin-Index (FI) dafür nicht ausreichen sollte.
| Parameter | Beschreibung | Normwerte |
|---|---|---|
| (wr/hs)CRP | (Wide Range / High Sensitive) C-reaktives Protein gehört zu den Akute-Phase-Proteinen. ↑ (> 5 mg/l) bei akuten Entzündungsprozessen, Immunreaktivität, Infektionen, Tumoren. In diesem Fall, ggf. schon ab 1-2mg/l, ist sind im Normbereich liegende Eisen-, Ferritin-, CP-, Kupfer-, Transferrin-, Ret-Werte nicht aussagekräftig oder mit Vorsicht zu interpretieren. | < 5 mg/l (optimal < 0,5 mg/l) |
| GOT, GPT, Gamma-GT (GGT) | Sollten die(se) Leberwerte stark erhöht sein, sind dieses zusammen mit hsCRP Hinweise auf eine Entzündung bzw. Leberstörung. In diesem Fall ist sind im Normbereich liegende Ferritinwerte (aber ggf. auch andere) mit Vorsicht zu interpretieren. | Sollten klar unterhalb des oberen Normbereiches sein. |
| Interleukin 6 (IL-6) | Ist ein proinflammatorisches Zytokin, das eine Schlüsselrolle in der Immunantwort und (chronischen) Entzündungsprozessen spielt. IL-6 korreliert auch stark mit Hepcidin, soweit kein eklatanter Eisenmangel vorliegt, was für die Regulation von Ferrorportin zentral ist. Ein ↑ Hepcidin sperrt das Eisen ein, macht es also weniger Bioverfügbar. | < 5 pg/mL (Laborabhängig) |
Alternativ könnte man auch noch TNF-alpha und andere Interleukine testen lassen. Für meine Geschmack reichen IL-6, als Marker chronischer Entzündungen, sowie hsCRP, was u.a. Akut-Phase-Anstiege bei den Entzündungs-Reaktionen gut reflektiert.
Eisen, Kupfer im Kontext des großen Blutbildes, TIBC und der Transferrin-Sättigung – Wintrobe et al., 1954
„Irre“ ist für mich immer noch die Studie von Wintrobe et al. von 1954 [1], welche damals schon herausgefunden hatten, das ein Mangel an bioverfügbarem Kupfer faktisch die gleichen Auswirkungen auf das Blutbild hat, wie ein Eisenmangel, bis auf Serum-Ferritin. Leider gab es damals das Serum-Ferritin noch nicht, sondern nur TIBC (Sättigung), was der Transferrin-Sättigung entspricht. Am Ende habe ich jedoch auch dazu eine Auflösung 😉
Wintrobe selber ist quasi der Erfinder und Begründer des kleinen Blutbildes und ich denke er (und sein Team) wussten bei ihrer Kupfer & Eisen-Studie an Schweinen, die dem Menschen sehr ähnlich sind, was sie machten. Bei dem Versuch gab es 4 Gruppen:
- Die gesunden Kontrollen,
- Schweine mit starkem Kupfermangel (Hb= 6,4 g/dl),
- Schweine mit starkem Eisenmangel (Hb= 5,9 g/dl),
- und Schweine mit Eisen + Kupfermangel (Hg=3,4 g/dl).
Zudem wurden 30 mg Eisen/Kg Körpergewicht an die kupferarmen Schweine und 0,5 mg Kupfer/Kg Körpergewicht an die eisenarmen Schweine von Beginn des Versuchs an gegeben um die jeweilig anderen Mängel auszuschließen.
Allgemein gilt ein Hb <12 g/dl als ein Indiz für einen mögliche Anämie und ein Wert < 10 g/dl für eine klare Anämie. Ein realer Eisenmangel wird gefolgert, wenn Serum-Eisen, Serum Ferritin, MCH, MCV und MCHC (sehr) niedrig sind. Interessanter Weise gibt es noch weitere Auffälligkeiten:
- Die prozentualen Retikulozyten (RETR) sind bei Kupfermangel normal-erniedrigt, bei Eisenmangel erhöht.
- Info: Dies sind „junge“, frisch im Knochenmark gebildete Erythrozyten (rote Blutkörperchen).
- bei Eisen+Kupfermangel sind faktisch alle Werte bis auf RETR dramatisch niedrig.
Wichtig ist hier, das es in einigen Fällen eine relative Erhöhung der Retikulozyten geben kann, wobei die Gesamtzahl der roten Blutkörperchen stark reduziert ist. Dies bedeutet jedoch nicht, dass die tatsächliche Produktion von Retikulozyten erhöht ist. Normalerweise sind die absoluten Retikulozyten bei Eisenmangel erniedrigt! Nachfolgend noch die Messwerte der Studie aus Tabelle 1:
Hinweis: Der nächste (und weitere) kurze Abschnitt ist aus rechtlichen Gründen für die Freunde des Blogs sichtbar.
In weiteren Untersuchungen (Tabelle 3, nachfolgend) ist zu sehen, das
- Leukozyten (weiße Blutkörperchen, ohne Häm) nur bei Kupfermangel deutlich vermindert waren.
- Mononukleäre Zellen (Monozyten Absolut, einkernige Leukozyten, z.B. Lymphozyten und Monozyten) sind ebenfalls nur bei Kupfermangel vermindert.
- Thrombozyten sind bei starkem Eisenmangel deutlich erhöht, bei Kupfer jedoch nicht.
Hinweis: Der nächste kurze Abschnitt ist nur für die Freunde des Blogs sichtbar.
In den Untersuchungen zu Eisen und Kupfer (Tabelle 4) ist zu sehen, das
- Kupfer im Vollblut, Erythrozyten und Plasma bei Mangel von Kupfer deutlich niedrig ist
- Wichtig: Trotz der Eisengabe bei Kupfermangel-Schweinen ist das Eisen im Plasma niedrig! Das lässt für mich auf mangelnde Eisen-Mobilisierung schliessen.
- Eisen (im Plasma), TIBC und die TIBC- (Transferrin-) Sättigung können einen Eisen bzw. Kupfermangel nicht unterscheiden.
Hinweis: Der nächste kurze Abschnitt ist nur für die Freunde des Blogs sichtbar.
Wichtig: Für die jeweiligen Veränderungen muss jedoch darauf geachtet werden, das diese ggf. erst bei bereits sehr geringen Hb-Werten beobachtet werden. Es ist nicht klar, wie die Progression der Werte bei nur leichter Anämie mit Hb-Werte zwischen 10-12 g/dl ist.
Aus der Schlussfolgerung der Studie ergeben sich leider auch keine weiteren Informationen, ausser, das dort gefolgert wird, das die „Unterschiede zwischen den beiden Mangelsituationen gering waren“.
Die wichtige und ausstehende Frage ist für mich jedoch: „Was würden die Serum-Ferritin-Werte sagen?“ Leider gab es anf. 1950 noch keinen Serum-Ferritin als Laborwert, weswegen dieser nicht gemessen wurde. Allerdings gibt es eine Studie von Miyajima et al., über Aceruloplasminämie [2], eine Störung des Eisenstoffwechsels, die durch das vollständige Fehlen der Ceruloplasmin-Ferroxidase-Aktivität verursacht wird. Das ist der Fall, wenn kein bioverfügbares Kupfer im Körper ist, also wegen Kupfer- und/oder Retinol-Mangel. Das alles geht mit sehr niedrigem bis fehlendem Serum-Ceruloplasmin und einer Kombination der folgenden Merkmale einher:
- Niedrige Kupferkonzentration im Serum
- Niedrige Serum-Eisenkonzentration
- Erhöhte hepatische Eisenkonzentration (-> Leber)
Das meint: Wenn (bioverfügbares) Kupfer fehlt, Fe2+ Eisen nicht nach Fe3+ gewandelt werden kann, dann ist zwar genug Eisen da – es ist jedoch nicht bioverfügbar.
Serum-Ferritin in Männern und Frauen – Jacobs et al. 1972
Im Falle von Serum-Ferritin ist es hilfreich auf die Studie zu schauen, die den Ruf von Serum-Ferritin als Marker für die Eisenspeicher begründete: Jacobs et al., aus 1972 [3]. Die Studie erscheint mir hilfreich, nur man sollte Sie auch gelesen haben, denn Sie charakterisierte diesen Blutwert ganz gut.
Hinweis: Der nächste kurze Abschnitt ist nur für die Freunde des Blogs sichtbar.
O.k., was haben die Forscher im Jacobs damals aus Ihren Messungen abgeleitet?
- Die Ferritinkonzentration im Serum ist ein quantitatives Maß für die Menge des gespeicherten Eisens (-> Korrelation)
- Bei keinem normalen Probanden wurde eine Serum-Ferritin-Konzentration von mehr als 200 ng/ml festgestellt.
- Meint: Hohe Serum-Ferritin Werte sind nicht gut!
- Der mittlere Wert bei
- normalen Männern liegt bei 69 ng/ml,
- bei normalen Frauen dagegen bei 35 ng/ml,
- was alle die mein(t)en 70-150 ng/ml wäre ein Optimalbereich der Irreführung überführt.
- Eine Konzentration unter 10 ng/ml wird jedoch mit einer niedrigen Transferrinsättigung (< 16%) und einer eisenarmen Erythropoese (-> Blutbildung) in Verbindung gebracht.
- vermutlich aufgrund einer gestörten Eisenversorgung des Plasmapools.
- Meint: Ein realer Eisenmangel.
Leider wurde hier nicht der Retinol und der Kupfer-Status gemessen. Allerdings gibt es noch ein paar Werte der Probanden, welche die Forscher tabellarisch aufführten:
Hinweis: Der nächste kurze Abschnitt ist nur für die Freunde des Blogs sichtbar.
Was mir in den obenstehenden Tabellendaten insgesamt noch auffällt ist, das
- Gesunde weibliche Probanden haben generell niedrigere Eisenwerte als Männer (warscheinlich durch die Regelblutung)
- Der Großteil aller gesunden Probanden hat Serum-Ferritin-Werte <= 80 ng/ml
- Selbst Serum-Ferritin-Werte < 20 ng/dl sind nicht außergewöhnlich für gesunde Probanden, speziell Frauen.
- Probanden mit Eisenmangel hatten im Schnitt Hb-Werte < 10 g/dl und in jedem Fall
- Serum-Eisen weit unterhalb von 65 µg/dl.
- Transferrin-Sättigung weit unterhalb von 15%
Wie jedoch Kell et al. [4] anmerken hat Serum-Ferritin das Problem, das sein „guter Wertebereich“ breit bzw. weit ist, es als Akut-Phase Protein bei Entzündungen erhöht ist und es wohl auch ein Produkt zellulärer Zerstörung zu sein scheint. Dies macht seine alleinige Verwendung schwierig. Deswegen schaute ich noch mal etwas tiefer in der Studienlage.
Serum-Ferritin Werte in Relation mit denen aus einer Knochenmark-Aspiration – J. Mazza et al. 1978
Nach dem Jacobs et al Serum-Ferritin in den Fokus gerückt hatten gab es eine reihe weiterer Studien dazu, wobei ich selber J. Mazza et al. aus dem Jahr 1978 [5] interessant finde, weil diee im Knochenmark „nachgeschaut“ haben, was denn nun Sache mit dem Eisen war. Dafür wurden die Date von 100 Patienten herangezogen, bei denen zudem eine Knochenmark-Aspiration über 4 Monaten erfolgte. Gleichzeitig versuchten die Forscher die Nützlichkeit und Korrelation von Serum-Ferritin, der Transferrin-Sättigung und vom Serum-Eisen zu bestimmen. Folgendes haben die Forscher zusammengefasst [5]:
| Variable gemessen | Sensitivität* | Spezifität† | Effizienz‡ |
|---|---|---|---|
| Serum-Eisenkonzentration | 84% | 43% | 52% |
| Transferrin-Sättigung | 84% | 63% | 67% |
| Serum-Ferritin-Konzentration | 79% | 96% | 92% |
| Serum-Eisen und Serum-Ferritin zusammen | 84%§ | 42% | 51% |
| Transferrin-Sättigung und Serum-Ferritin zusammen | 84%§ | 50% | 64% |
*Prozentsatz der Patienten ohne Knochenmark-Hämosiderin und mit einem positiven (niedrigen) Testergebnis.
†Prozentsatz der Patienten mit Knochenmark-Hämosiderin und einem negativen (normalen oder hohen) Testergebnis.
‡Prozentsatz der Patienten mit einem korrekt-negativen oder korrekt-positiven Testergebnis.
§Prozentsatz der Patienten mit positiven (niedrigen) Ergebnissen für einen der Tests oder für beide Tests.
Die Tabelle zeigt, das Serum-Ferritin als Einzelwert zur Bestimmung des Eisen-Status besser war, als jeder der anderen Werte oder Wertekombinationen. Weitere Informationen, welche die Forscher festgestellt hatten:
- Bei 15 der 19 Patienten mit Hämosiderinmangel im Knochenmark lag die Ferritinkonzentration im Serum unter 18 ng/ml. Von diesen 15
- hatten 11 einen unkomplizierten Eisenmangel,
- 3 eine chronische Entzündung und
- 1 einen soliden Tumor.
- Die Ferritinkonzentration im Serum lag nur bei 3 der 67 Patienten mit retikuloendothekalem Hämosiderin unter 18 ng/ml.
- Die Serumeisenkonzentration lag bei 16 der 19 Patienten ohne Knochenmark-Hämosiderin <65 pg/dL
- Die Transferrinsättigung war bei 16 der 19 Patienten ohne Knochenmark-Hämosiderin kleiner als <20%.
Die Studie legte den Punkt an dem das Serum-Ferritin einen potentiellen Eisenmangel indiziert < 18 ng/ml an. Auch Kell et al. [4] merkten, bei aller Kritik an Serum-Ferritin an, das:
„Viele Dutzend Referenzen weisen darauf hin, dass bei normalen Menschen (ohne offenkundige Entzündung) die Ferritinwerte im Serum mehr oder weniger eng mit den Eisenspeichern im Körper (z. B. in der Leber) zusammenhängen, wie sie durch Magnetresonanztomographie, Biopsie oder wiederholte Aderlässe festgestellt werden.“
Meint: Im „Normalfall“ passt das „mit dem Serum-Ferritin“ recht gut, wobei bei Entzündung auch höhere Werte auftreten können, bei den trotzdem ein realer Eisenmangel vorliegt. Das Labor GanzImmun [20] merkt noch an, das die Bestimmung der Ferritinspiegel nur dann aussagekräftig ist, wenn keine anderweitigen Erkrankungen „wie Entzündungen, bakteriellen Infekte, Leberstörungen oder maligne Tumorerkrankungen vorliegen“.
Die Hepcidin-Ferritin-CRP Studie bei entzündlichen Darmerkrankungen – Mecklenburg et al. 2014
Ich weiß, es wird langsam viel. Jedoch fand ich die Studie von Mecklenburg et al. [6] recht interessant, weil Sie einen Einblick in Hepcidin-Werte in Relation zu Serum-Ferritin an einer größeren Patienten-Kohorte gibt. Dies dann noch speziell bei Menschen mit entzündlichen Darmerkrankungen, und dann noch gruppiert in Aktive und nicht aktive Phase. Das ganze erlaubt wirklich gute Einblicke in die Interpretation in die verschiedenen Konstellationen von Blutwerten bei solchen Erkrankungen. Allerdings wurden, wie „üblich“, Kupfer und Retinol, nicht gemessen.
Interessant ist, das die Forscher die Unterscheidung Eisenmangel-Anämie bei Hb < 12 g/dl (Frauen), Hb < 14 g/dl (Männer) und Serum-Ferritin < 30 ng/ml gemacht haben. Hb unter 14 g/dl bei Männer als Parameter für eine eisenmangel-Anämie ist schon eine „Steile“ Nummer, weil hierfür normaler weise 10-12 g/dl als Messlatte gelten. „Interesanter“ passen dann scheinbar alle Patienten in das Raster, so das keiner ein Serum-Ferritin < 30 ng/ml bei einem Hb-Wert >= 12/14 g/dl gehabt hat. Das ist aus meiner Sicht, und in Hinblick auf andere Studien, nicht plausibel. Dennoch, diese Studie verleiht einige relevante Einblicke in die „Spielarten“ von Hepcidin und die Dynamik von Serum-Ferritin.
Nachfolgend erst einmal zwei wichtige Tabellen aus der Studie, welche ich nach Deutsch übersetzt und Transkribiert habe. Zuerst die für die Patienten mit Colits U.:
Hinweis: Der nächste kurze Abschnitt ist nur für die Freunde des Blogs sichtbar.
Folgendes haben die Forscher in der Studie noch explizit bemerkt bzw. angeführt:
- Unabhängig von der Entzündungsaktivität hatten alle Patienten mit vermindertem Ferritin (<30μg/L) einen signifikant niedrigeren Hepcidinspiegel im Vergleich zu Patienten und gesunden Kontrollen mit normalem Ferritin (>30μg/L).
- Anmerkung: Ich habe diese Wertebeziehungen in Blau und Fett markiert. Für mich bedeutet dies, das bei einem klaren realen Eisendefizit auch Hepcidin supprimiert ist, u.a. um die Aufnahme aus dem Darm sowie die Mobilisierung aus den Speichern zu fördern. Interessant wäre gewesen, wen noch IL-6 gemessen worden wäre.
- Es wurde eine signifikante Korrelation zwischen den Serum-Ferritinwerten und dem Serum-Hepcidin festgestellt (Spearman’s Rho=0,491; p<0,001).
- Patienten mit Entzündungen, die durch
- hohe Werte des C-reaktiven Proteins (> 10 mg/L) gekennzeichnet sind, und
- Patienten mit multiplem Myelom (von denen bekannt ist, dass sie überschüssiges IL-6 absondern)
- haben alle einen unangemessen erhöhten Hepcidinspiegel
Allerdings lese ich auch aus dem Daten, das ein chronisch hohes CRP eher wenig Einfluss auf die Serum-Ferritin Werte zu haben scheint, da in der erste Anämie-Gruppe CRP von 7-58 mg/L gemessen wurden, jedoch das höchste Ferritin 29 und das niedrigste 4 µg/L war.
Interessant auch die Schlussfolgerung der Studie:
„Diese retrospektive Analyse legt nahe (unabhängig dem Status der Krankheit), dass Eisenmangel der Hauptauslöser für die Hepcidin-Regulierung bei CED-Patienten mit Anämie ist.“
So bestätigen Xin Guo et al [7] und Lin-Na Guo et al. [10] die Ferritin/Hepcidin-Korrelation in Diabetes Typ 2 Patienten, wie auch Ryan et al. [8] für Patienten mit nicht-alkoholischer Leberentzündung und Gill et al. [9] für Menschen ohne Erkrankung, jedoch nicht für Menschen mit (viraler[8]) Hepatitis (C[9]). Im letzten Fall korrelieren die beiden Werte negativ [8][9]. Nichts ohne Ausnahmen….
Löslicher Transferrin-Rezeptor (sTfR): Einblick in den aktuellen Eisenbedarf
Relativ neu als Blutwert in „normalen“ Laboren ist der lösliche Transferrin-Rezeptor (sTfR). Das Problem bei Ferritin (Serum) und Transferrin ist, das niedrige Werte keinen Mangel an Funktionseisen beweisen, also das „momentan biologisch“ verfügbares Eisen wirklich fehlt und nicht nur, dass das Speichereisen ggf. gering aber dennoch ausreichend ist. Dieser Unterschied ist extrem wichtig!
Zudem werden beide vorgenannten Werte (-> Serum-Ferritin, Transferrin) durch Akut-Phase Entzündungen beeinflusst: Ferritin steigt, Transferrin sinkt und die Transferrin-Sättigung ist dann das Resultat aus falsch und falsch. Die Bestimmung von sTfR ermöglicht nun die wohl weitgehend entzündungsunabhängige Beurteilung der Eisenversorgung eisenabhängiger Zellen.
Der Hintergrund ist folgender: Alle Gewebe bzw. Zellen mit Eisenbedarf regeln ihre Eisenaufnahme durch Expression (-> die Menge) von Transferrinrezeptoren (TfR) auf der Zelloberfläche. An diese kann dann das mit Eisen beladene Transportprotein Transferrin binden, damit das Eisen in das Zellinnere aufgenommen wird. Nach „Andocken“ des Transferrins wird das Eisen abgespalten und das (nun eisenfreie) (Apo)-Transferrin wieder an die Zelloberfläche transportiert. Durch (proteolytische) Ablösung des TfR von den Zellmembranen treten lösliche Transferrinrezeptoren (sTfR) in das Plasma über, welche dann über diesen Bluttest gemessen werden können.
Ggf. ist noch relevant, das ca. 80 bis 95 % der löslichen TfR sich auf den Zellen der Blutbildung (Erythropoesezellen) befinden. Bei Mangel an Eisen steigt die sTfR-Konzentration im Serum recht schnell an, da die Erythropoesezellen mehr TfR auf der Zelloberfläche exprimieren, wobei dies wohl passiert, bevor der Hb-Wert stark absinkt. Man kann also einen potentiellen Mangel an bioverfügbaren Eisen schon früh erkennen. Skikne et al. [11] merken so an, das
- sTfR als Laborwert wertvoll ist, da dieser Wert auch einen leichten Eisenmangel, der erst kürzlich aufgetreten ist, anzeigen kann.
- Serum-Ferritin sei hingegen ein Maß für die Eisenspeicher und
- der (niedrige) Hb-Wert eher ein Maß für einen fortgeschrittenen Eisenmangel.
Das ganze soll auch bei erniedrigter Transferrin-Sättigung funktionieren, sowie auch beim Andocken von „leerem“ (Apo-) Transferrin an die TfR, weil der lösliche Anteil dennoch freigesetzt wird. Im Normalfall bindet jedoch „geladenes“ (Holo-) Transferrin an die TfR, weil hier die Affinität (-> Anziehung) größer ist. Zudem kann wohl der lösliche Anteil auch „abdocken“, ohne das Transferrin andockt, so das ein höherer sTfR-Wert den Anstieg der erhöhten TfR-Exprimierung anscheinend gut wiedergibt.
Ein erhöhter sTfR-Wert ist also ein Indikator für einen ungedeckten Bedarf an Eisen in den Zellen, der auch hoch ist, wenn die Gesamteisenspeicher ausreichend gefüllt sind, aber durch ein hohes Hepcidin das Eisen dort zurückgehalten wird.
Auch Kell et al., welche viele Fragen zur Rolle des Serum-Ferritin haben, [4] äußern sich positiv zum sTfR und schreiben, das Serum-Ferritin als alleiniger Marker für den Eisenstatus in Verruf geraten ist und sTfR als wesentlich nützlicher angesehen wird, da sTfR zur Unterscheidung der Anämie bei chronischen Krankheiten von der Eisenmangelanämie verwendet werden kann. Das dem so ist haben aus meiner Sicht Purronen et al. [12] plausibel nachgewiesen.
Die sTfR-log-Ferritin-Index Studie von Punnonen et al. 1997
Interessant wird es in der Studie von Punnonen et al. [12], die für Ihre Untersuchungen an anämischen Patienten neben Hb und MCV auch Eisen (Serum), Ferritin (Serum), Transferrin (plus Sättigung) sowie sTfR gemessen haben. Zudem haben Sie den sTfR-Index und den sTfR-Log-Ferritin-Index (FI) in Ihrer Prognose-Kapazität überprüft und mit Ferritin und anderen Einzelwerten verglichen.
Die Patientenpopulation bestand dabei aus 129 konsekutiven anämischen Patienten des Universitätskrankenhauses von Turku, bei denen eine Knochenmarkuntersuchung durchgeführt wurde um zu schauen, ob die Patienten wirklich einen realen Eisenmangel hatten. Von diesen Patienten hatten
- 48 eine Eisenmangelanämie (IDA),
- 64 eine Anämie aufgrund einer chronischen Erkrankung (ACD) und
- 17 Patienten wiesen verbrauchte Eisenspeicher und eine infektiöse oder (chronisch) entzündliche Erkrankung bzw. ein nicht-hämatologisches Malignom auf (COMBI).
Allerdings wurden keine Kupfer und Retinol gemessen und die beiden Worte tauchen auch nicht in der Volltext-Studie auf. Zudem gab es keine gesunden Kontrollen und es wurden keine Akut-Phase und /oder Entzündungswerte bestimmt, so das die ermittelten Blutwerte mit Vorsicht verglichen werden müssen, da sich zudem aktuelle analytischen Verfahren teils unterscheiden. Dennoch liefert diese Studie sehr wertvolle Hinweise.
Bei der Interpretation der (nachfolgenden) Tabellenwerte bzw. 3 Patienten-Kohorten ist wichtig zu beachten, das bei ACD (Anemia of chronic Disease) die Hb-Werte auch erniedrigt sind. Dies u.a., weil durch die (chronisch) hohen Entzündungswerte die Eisenfreisetzung aus dem Speichern reduziert ist (-> Hepcidin vermutlich hoch) , was sich auch beim niedrigen Serum-Eisen zeigt.
Die erste Tabelle zeigt die Übersicht über die drei Patienten-Kohorten sowie die gemittelten Blutwerte für die Eisen-Relevanten Parameter. Mit fällt auf, das Ferritin bei ACD in der Regel extrem hoch ist. sTfr ist jedoch nur bei den ACD-Patienten (normal-) niedrig.
Hinweis: Der nächste kurze Abschnitt ist nur für die Freunde des Blogs sichtbar.
Für eine bessere Übersicht haben die Autoren der Studie die einzelnen Messwerte für sTfR, Ferritin und TfR-F-Index noch in einem Scatter-Plot abgebildet. Wo es bei Ferritin und sTfR Überschneidungen bei den Kohorten gab, kann der sTfR-Log-Ferritin-Index (FI) scharf und faktisch ohne Überschneidung auch bei den „Ausreißern“ der Kohorten, zwischen ACD sowie IDA+KOMBI trennen. Werte unter 2,0 bei sTfR-Log-Ferritin-Index sind nach den Scatter-Plots immer ADC zuzuordnen!
Hinweis: Der nächste kurze Abschnitt ist nur für die Freunde des Blogs sichtbar.
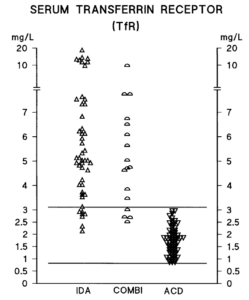
TfR-Konzentrationen im Serum bei anämischen Patienten. Das zentrale 95. Perzentil der Referenzverteilung für den TfR-Assay ist mit horizontalen Balken dargestellt. Quelle: [12]
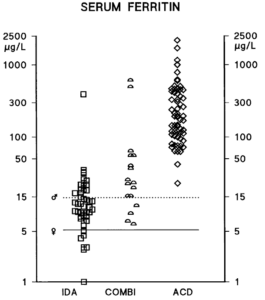
Serum-Ferritin-Konzentrationen bei anämischen Patienten. Die unteren Referenzgrenzen der Serum-Ferritin-Bestimmung sind für männliche (♂) und weibliche (♀) Probanden getrennt durch horizontale Balken angegeben. Quelle: [12]
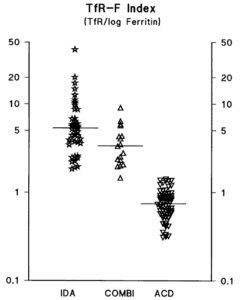
Der TfR-F-Index (Verhältnis TfR/log Ferritin) bei anämischen Patienten. Die Medianwerte für jede Patientengruppe (IDA, 5,4; COMBI, 3,2; ACD, 0,8) sind durch horizontale Balken gekennzeichnet. Quelle: [12]
[/wpmem_logged_in]
Um die einzelnen Blutwert-Marker zu bewerten verglichen die Autoren diese in der nachfolgenden Tabelle (Nr. 3 in der Studie). sTfR-Log-Ferritin-Index (FI) war bei seiner Aussagekraft (-> falsch Negativ, falsch positiv, richtig positiv, richtig negativ, Sensitivität und Spezifizität) der herausragende Marker mit fast 100% Trefferrate – im Guten wie auch im Ausschluss. Sicherlich ist dies in dieser Studie nur deswegen so gut, weil es keine gesunden Kontrollen gibt – aber immerhin! Die Tabelle 3 aus der Studie findet sich im Anhang, unter den Referenzen.
Zusammenfassend folgern die Autoren der Studie:
- Das Ergebnis deutet darauf hin, dass bei ACD-Patienten die potenziell erhöhte Zytokinproduktion die durch Eisenmangel verursachte sTfR-Antwort nicht wesentlich beeinflusst.
- Ein großer Vorteil der sTfR-Messungen gegenüber dem Serum-Ferritin sei die offensichtliche Spezifität der biologischen Reaktion auf Veränderungen des Eisenstatus und der Erythropoese, wenn eine Hämolyse oder Megaloblastose ausgeschlossen werden kann.
- Die logarithmische Transformation der Ferritinwerte und die Berechnung des sTfR-log-Ferritin-Indexes (FI) lieferte jedoch einen hervorragenden Indikator für die Eisenverarmung, wie es aus dem Scatter-Plot hervorgeht.
- Die vorliegende Studie legt nahe, dass die klinische Interpretation von sTfR-Messungen im Vergleich zu Ferritin einfacher ist.
- Der sTfR-log-Ferritin-Index macht sich die Beziehung zwischen zwei Phänomenen zunutze, d. h. einem Anstieg des TfR und einem Rückgang der Ferritinkonzentration.
- Bei einem beträchtlichen Teil der Patienten mit Eisenmangel lag die Transferrin-Konzentration innerhalb der Referenzgrenzen einer gesunden Bevölkerung (siehe Materialien und Methoden), was die klinische Interpretation der Transferrinkonzentrationen erschwerte.
Was bedeutet dies alles in Kürze?
- Serum-Ferritin (SF) alleine ist ein recht guter Marker zur Diagnose von IDA.
- Die SF-Grenze zwischen IDA & ADA ist ca. 50 ng/ml, so das davon auszugehen ist, das ab 50 ng/ml, (bei normalem CRP) in der Regel kein realer Eisenmangel (IDA) mehr vorliegen kann.
- Erhöhte sTfR-Werte reflektieren einen erhöhten zellulären Eisenbedarf (u.a. Erythropoese) und sind somit ein direkter Indikator für den Eisenstatus.
- sTfR alleine ist nicht besser als Ferritin (Serum) in seiner prädiktiven Qualität
- Der sTfR-Log-Ferritin-Index (FI, TfR-F-Index) kann (in der vorliegenden Studie) klar zwischen Eisenmangelanämie (IDA) von Anämie chronischer Krankheiten (ACD) unterscheiden, auch in entzündlichen Zuständen und besser als Ferritin und sTfR alleine.
Zu beachten ist, das es sich bei diesen Patienten und klinisch einwandfrei diagnostizierte IDA und ACD-Patienten handelte, die nicht nur aufgrund eines Parameters klassifiziert wurden. Wie gut die Marker bei Menschen mit einer beginnenden oder leichten IDA bzw. ACD funktionieren ist von diesen Ergebnissen nicht zwingend abzuleiten. Relevant mag noch sein, das bei IDA-Patienten Serum-Ferritin Werte nur bis ca. 40 ng/ml festgestellt wurden, wobei >50% der Patienten einen Wert < 18 ng/ml hatten.
Unterschiedliche Test-Kits für sTfR, Thomas et. al 2002
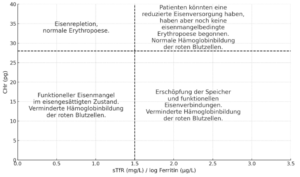
Diagnostisches Diagramm, das die Korrelation zwischen sTfR-log-Ferrtin-Index und CHr (MRH) in Bezug auf den Eisenstatus zeigt. Basierend auf [22]
- Zwei der Assays (Dade Behring und Roche Diagnostics) verwenden die Mikroagglutination von Latexpartikeln, die mit einem monoklonalen Anti-sTfR-Antikörper beschichtet sind.
- Der dritte Test (Nichols Institute) verwendet einen nicht-kompetitiven Sandwich-Typ Assay mit lumineszenzmarkierten monoklonalen Antikörpern gegen sTfR.
Purrunen et al. [12] nutzten hingegen ein Clinigen R&D Systems-Assays auf der Grundlage eines polyklonalen Antikörpers in einem Sandwich-Enzymimmunoassay (EIA), was erklärt warum diese Werte nicht zu denen von Thomas et al. passen.
Die jeweiligen Messwerte waren dann zwar proportional ähnlich, aber Testkit-Spezifisch. Die Werte unterscheiden sich dabei bis zu Faktor 2,5. Insofern müssen in der Praxis immer die Referenzbereiche des jeweiligen Labors beachtet werden, wobei natürlich nicht klar ist, welche genauen „Messlatten“ das Labor anlegt. Interessant ist, das die Forscher noch etwas zu den Referenzbereichen der Tests anmerkten. Die Eisenversorgung ist in den folgenden Fällen erschöpft (IDA), in denen der sTfR-F-Index (u.a. X-Achse im Bild) folgende Werte überschreitet:
- Dade-Assay: >1,5 (bei CRP <= 5 mg/L) und >0,8 (CRP >5 mg/L).
- Nichols-Assay: >3,5 (bei CRP <= 5 mg/L) und >1,9 (CRP >5 mg/L).
- Roche-Assay: >3,8 (bei CRP <= 5 mg/L) und >2,0 (CRP >5 mg/L).
Diese Liste sagt jedoch noch etwas anderes aus: Da der Index unter dem Bruch das Ferritin stehen hat, und dieses bei Akut-Phase Entzündungen erhöht ist (CRP>5), ist der sTfR-log-Ferritin-Index Akut-Phase beeinflusst, wobei dies bei Punnonen et al. nicht so dargestellt wird. GanzImmun [20] schreibt aber gleiches und weist wie Thomas et al. darauf hin, das bei Immunreaktivitäten mit einem CRP > 5 mg/l sich der Entscheidungswert des Ferritinindex von 3,2 nach 2,0 senkt! So scheint GanzImmun wohl das Nichols-Assay, oder Nachfolger davon, zu verwenden.
Die Studie von Thomas et al. liefert jedoch einen weiteren Beitrag: Die Nutzung von Retikulozytenhämoglobin (MRH, CHr, Ret-Hb) um zusammen mit dem sTfR-log-Ferritin Index ebenfalls einen funktionellen von einem realen Eisenmangel zu unterscheiden, wobei beide festgestellt werden (siehe Bild). Allerdings sei angemerkt, das MRH/Ret-Hb von (Akut-Phase) Entzündungen vermindert wird, so das auch diese Diagnosevariante nicht unproblematisch ist.
Zinkprotoporphyrin (ZnPP) Beurteilung des Eisenstatus an der Häm-Synthese
Ein weiterer Parameter zur Beurteilung der Eisenvorsorgung ist Zinkprotoporphyrin (ZnPP). ZnPP wird in Phasen des Eisenmangels während der Häm-Synthese gebildet, wenn Zink anstatt Eisen als Zentralatom in Protoporphyrin eingebaut wird, das eigentlich zu Häm werden sollte. Daher kommt es zu einem Anstieg des ZnPP-Spiegels in der Blut-Zirkulation, wo es leicht gemessen werden kann. Das Verhältnis ZnPP/Häm ist dann ein recht sensitiver und spezifischer Indikator des Eisenstatus im Knochenmark. Da ZnPP kostengünstig zu ermitteln und unabhängig von Akut-Phase Entzündungen ist, ist es als diagnostischer Marker beliebt. Allerding ist ZnPP bei GanzImmun teurer als der sTfR-log-Ferritin-Index.
Im Vergleich zu sTfR kann ZnPP keine IDA von einer ACD unterscheiden. Das ist erst einmal so und muss kein Mangel sein. Ist genug Eisen im System, steht es aber nicht für die Häm-Synthese im Knochenmark zur Verfügung (ACD), dann ist ZnPP auch erhöht [13]. ZnPP unterscheidet also nicht die Art der Anämie und muss deswegen mit anderen diagnostischen Markern, z.B. Serum-Ferritin, kombiniert werden.
ZnPP kann u.a. bei Malaria, anderen Infektionen, chronische Entzündungen und Hämoglobinopathien erhöht sein [14], obwohl kein realer Eisenmangel vorliegt – weil die Eisenfreisetzung „abgedreht“ ist. Auch bei einer Urämie, u.a. in Folge einer terminalen Niereninsuffizienz oder eines akuten Nierenversagens, kann ZnPP falsch hoch sein [15].
Mwangi et al. [16] merken an, dass der Nachweis von Eisenmangel durch die ZnPP zu einer deutlichen Überschätzung der Prävalenz des Eisenmangels führt (mehrere Studien), wobei diese Diskrepanzen zumindest teilweise auf Entzündungen oder Infektionen aber auch auf die geringe Spezifität (-> „Genauigkeit“) bei den konventionell verwendeten Grenzwerten zurückzuführen sein. Zudem zeigten die Ergebnisse von Mwangi et al. dass eine hohe Sensitivität unweigerlich mit einer niedrigen Spezifität und damit einem inakzeptabel niedrigen negativen Vorhersagewert einhergeht (-> zu viele falsch positive).
Weiterhin muss beachtet werden, das ZnPP in im Vollblut und Erythrozyten gemessenen werden kann, wobei sich die Referenzwerte unterscheiden können, wobei ein Störfaktor Bilirubin sei [16]. Allerdings haben wohl beide Varianten die gleichen Probleme. Auch eine andere Studie bestätigte genau dies [17]: Zwar hat ZnPP eine hohe Sensitivität von 91,7%, jedoch eine geringe Spezifität von 60,2% im Vergleich zu 89,1% bei Hb oder 96,4 % bei Serum-Ferritn. In der Praxis bedeutet das viele falsch-positive. Deswegen liesst sich ein Studienergebnis auch recht ernüchternd [16] (deepl.com):
„In dieser Bevölkerungsgruppe haben sowohl die ZPP aus Vollblut als auch die ZPP aus Erythrozyten einen geringen diagnostischen Nutzen als Screening-Marker für die Behandlung von Eisenmangel, unabhängig davon, ob sie als Einzeltests oder in Kombination mit der Hämoglobinkonzentration verwendet werden.„
Was bedeutet dies alles in Kürze?
- ZnPP ist aufgrund der hohen falsch-positiv Rate maximal als hoch sensitiver (Pre-) Screening-Test einzusetzen, bei dem das Ergebnis durch Anamnese und in Zweifel anderen Blutwerte zwingend validiert werden muss.
Allerdings wäre aus meiner Sicht noch einzuwenden, das Serum-Ferritin sowieso bestimmt wird und sTfR günstiger als Vollblut-ZnPP zu bestimmen ist, was an der Praxisrelevanz von ZnPP zweifeln lässt. Insofern merkt eine weitere Studie aus 2018 an, das es noch keine Gold-Standard bei den Test-Kits gäbe und die Harmonisierung (Anm: wahrscheinlich der Wertebereiche) noch im Gange sei [18].
Transferrin und Transferrin-Sättigung (TfS)
Die Bewertung des Transferrin-Werts und seiner Sättigung (%) wurde durch die vorhergehenden Studien abgedeckt und wird von mir nicht weiter vertieft, so das ich hier nur kurz alles relevante noch einmal zusammenfasse.
Aus der Studie mit der monatlichen Blutspende [25] wurde berichtet, das der Serum-Ferritin Wert sank und so die verminderten Eisenspeicher reflektierte. Da kein Teilnehmer anämisch wurde passt dazu, das die Transferrin-Sättigung nicht sank. Ein Serum-Ferritin unter unter 10 ng/ml korreliert mit einer niedrigen Transferrinsättigung (< 16%), Hb-Werte < 10 g/dl mit Transferrin-Sättigung von < 15% [3]. Allerdings sind dies schon starke Eisenmängel. Eine andere Studie bemerkte jedoch, das Bei einem beträchtlichen Teil der Patienten mit Eisenmangel die Transferrin-Konzentration innerhalb der Referenzgrenzen einer gesunden Bevölkerung lag [12].
Das ist auch plausibel, den nach [5] war die Sensitivität (-> Erkennung von Eisenmangel) von TfS zwar gut (84%), jedoch die Spezifizität (-> keine falsch positive): lag nur bei 67%, also deutlich unter Serum-Ferritin (96%) als Einzelwert. Insofern kann der Wert, wenn er bereits vorliegt, sicherlich sinnvoll genutzt werden. Ich würde TfS bis auf Zweifelsfälle jedoch nicht mehr extra bestimmen lassen, wenn damit nicht klar definierte Zwecke verfolgt werden, wie u.a.:
Retinol-Status und Eisen (bzw. Serum-Ferritin)
Retinol und Kupfer, spielen in faktisch keiner von mir gefundenen Studie, bis auf Wintrobe et a., ein Rolle. Allerdings bin ich während meiner Recherche über eine afrikanische [23] und eine arabische [24] Studie gestolpert, welche zumindest Retinol betrachten. Die erste Studie [23] gab u.a. an, das:
- Bei stillenden Müttern, die ansonsten gesund erscheinen, kann ein marginaler (-> grenzwertiger) Vitamin-A-Status die Eisenspeicher beeinträchtigen kann.
- Mütter mit stark dezimierten Eisenspeichern (Serum-Ferritin <12 ng/ml) hatten einen signifikant niedrigeren durchschnittlichen Retinolspiegel im Serum (p < 0,05, Tabelle 2).
- Retinol bei starkem Eisenmangel: 180,46 +/- 53 µg/l.
- Retinol bei marginalem Eisenmangel: 211,97 +/- 86 µg/l
- Dabei gab es dann noch einmal einen signifikanten Unterschied bzw. eine Korrelation (p < 0,05) zwischen Müttern
- mit niedrigem Serum-Retinol (< 300 µg/ml) und niedrigem Serum-Ferritin (<30 ng/ml) und Müttern
- mit normalem Serum-Retinol (>300 µg/L) und normalem Serum-Ferritin (>30 ng/ml).
Die Autoren verweisen auch darauf, das Studien in Bangladesch von Ahmed et al. ebenfalls zeigten ebenfalls, dass heranwachsende Mädchen mit einem höheren Hb-Wert bessere Serum-Retinol-Werte aufwiesen. Die zweite Studie [24] folgerte, das
- auf Basis einer multiplen Regressionsanalyse, der Retinolspiegel im Serum einen signifikanten Zusammenhang mit der Hb-Konzentration aufweist.
Die Autoren schlussfolgerten, dass (wirklich) niedrige Retinolspiegel im Serum, unabhängig von der Eisenhomöostase, zu Anämie beitragen können. Ich denke, ohne das Thema hier noch einmal zu stark vertieft zu haben, das klar ist, dass ohne genug Retinol der Eisen-Transport und auch die Eisen-Aufnahme beeinträchtig ist.
Wichtig: Anmerken mag ich hier, das die Retinol-Spiegel hier < 300 µg/l waren, was wirklich sehr wenig ist. Da kommt dann für mich die Frage auf was a) für diesen Mangel ursächlich war (z.B. „vegane Ernährung“ und genetische Pre-Dispositionen) und b) wie der Gesamtgesundheitszustand dieser Menschen ist. Ggf. reflektiert hier Retinol auch den Grad der schlechten Grundversorgung mit allen mögliche Nährstoffen. Allerdings darf nicht vergessen werden, das genug Retinol z.B. Ceruloplasmin in Ratten erhöht, wenn genügend Kupfer vorhanden ist und vorher ein Mangel an Retinol bestand [27]. Die Relevanz von Vitamin A für den Eisen-Metabolismus ist nicht zu unterschätzen und sehr wichtig.
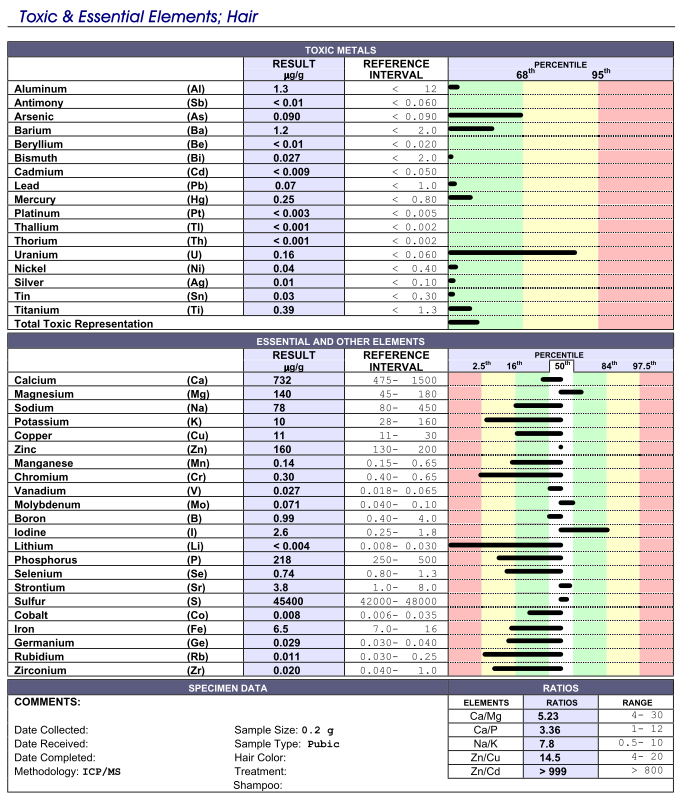
Insofern kann ich aus meiner Realität berichten, das mir ein (weiblicher) Fall bekannt ist in dem das Ferritin immer wieder niedrig war (u.a. 18 ng/ml), Eisen oft unter 65 µg/dl und Kupfer im Vollblut unterhalb der unteren Referenz. Hb lag, je nach Test, bis 12 g/dl, aber nie niedriger, und die TfS auch mal bei 12-14%. Klassischer Eisenmangel, ggf. Kupfermangel mag man meinen. Falsch gedacht! Denn: Kupfer im Haar war im oberen roten Bereich und das Serum Vitamin A lag bei ca. 327 µg/l. Für mich ist hier zu wenig Retinol das Problem, was dann zu einem Folgeproblem beim Kupfer- und Metabolisms führte. Ggf. fehlt das Retinol auch in Kontext Vitamin D (-> RxR) und immunologische Probleme kommen dazu.
Mein Fazit
Dieser Artikel betrachtete die gängigen Marker des Eisenstatus, ihre Sensitivität, Spezifizität, die Limitation und die spezifische Eignung für die Diagnose und Unterscheidung in Bezug auf IDA und ACD, sowie das Zusammenspiel mit anderen Werten. Da entzündliche Prozesse viele Werte „durcheinanderbringen“ können ist eine „>95% richtige“ Diagnose in den Grenzfällen nicht einfach durch Messen von „nur“ Serum-Ferritin möglich.
Letztendlich gibt es mindestens 6,5 Fälle bei einer Diagnose zu unterscheiden, weil das was dann getan oder speziell auch nicht getan werden sollte sich unterscheidet:
- „Alles gut“ –> Hb im gutem Bereich, Funktionseisen o.k., nicht zu wenig, nicht zu viel Speichereisen.
- Anm.: Also „nix“ machen, speziell kein Eisen einnehmen! Auch nicht „präventiv“. Nix, null!
- Wenig Speichereisen, jedoch noch genug Funktionseisen für alle Prozesse, inkl. Häm/Hb -> Hb & Co. o.k.
- Anm.: Hier würde ich nichts machen, ggf. die Ernährung optimieren & auf Risikofaktoren schauen.
- Zu viel Speichereisen, Funktionseisen für alle Prozesse o.k. -> Hb & Co. o.k.
- Anm.: Oft zu viel Häm-Eisen (u.a. rotes Fleisch), teils genetische Defekte. Ggf. Ernährung optimieren, Aderlass bzw. Blutspende erwägen.
- (Speicher-) Eisenmangel ohne Anämie (EoA) , aber ggf. schon Auswirkungen auf einige eisenabhängige Prozesse.
- Anm.: Noch genug Funktionseisen für Häm/Hb > 12/13 g/dl. Ggf. Mangel von 500-1000 mg Eisen [21]. Ursachen finden, Ernährung optimieren, ggf. Eisen ergänzen (eher Oral).
- Eisenmangelanämie (IDA), zu wenig Speichereisen, zu wenig Funktionseisen -> mit niedrigem Hb, MCH, MCHC, (sehr) niedrigem Serum-Ferritin.
- Anm.: Alle Eisen abhängigen Prozesse laufen suboptimal. Ursachen finden, Eisen ergäzen (Oral und/oder Infusion – je nah Ausgeprägtheit)
- Anämie chronischer Krankheiten (ACD), zu wenig Funktionseisen -> wie IDA, zudem oft chronische Entzündungen (u.a. IL-6 hoch) mit Subformen:
- a) Speichereisen (noch) o.k. -> Aber dieses Eisen ist „weggeschlossen“
- b) Zu viel Speichereisen -> zusätzlich zu a) ox-Stress durch viel (ggf. ungebundenes) Eisen.
- Anm.: Kein Eisen Ergänzen!
Ja, es ist „so kompliziert“. Nur befasst sich keine von mir gelesene Studie mit dieser Vielfalt, den oft ist der Fokus entweder der Eisenmangel oder die Unterscheidung von ACD und IDA. Zur Diagnose der unterliegenden Probleme, welche zu ACD oder IDA führen, habe ich bereits in Teil 2 und 3 dieser Serie etwas geschrieben.
Zum Schluss dieses Artikels folgend nun noch einmal eine kurze Zusammenfassung zu den einzelnen Blutwerten. In Teil 5 gibt es dann basierend auf diesem Artikel einen Leitfaden zur „Diagnose“, womit ich i diesem Falle einen Leitfaden zur Deutung der Eisenrelevanten Blutwerte auf basis der hier vorgestellten Studien meine.
Das kleine Blutbild: Hb, Hk, Ery, Ret, MCH, MCV, MCHC
Zur Diagnose einer Anämie sind diese Werte gut geeignet, wobei die Anämie schon sehr ausgeprägt sein kann, bevor diese Marker reagieren. Das Problem hier ist: Diese Marker können nicht zwischen einem Kupfer und Eisen-Mangel unterscheiden und beim Eisenmangeln nicht zwischen IDA und ACD. Man weiß also, das es ein Problem gibt, nur nicht welches so das zwingend andere Blutwerte für eine differenzierte Diagnose benötigt werden.
Serum-Ferritin
Egal wie man es dreht, Serum-Ferritin ist der Marker mit der besten Spezifizität und Sensitivität zur Bewertung der höhe der Eisenspeicher, solange keine Akut-Phase Entzündungen (-> CRP erhöht) oder Leberstörungen (-> GOT, GTP, GGT erhöht) vorliegen. Serum-Ferritin ist aber kein ausreichender Marker um alleine einen Mangel an Funktionseisen zu bestimmen, weil er hierfür zu ungenau und zu vielen Einflüssen unterworfen ist. Bei Werten < 18 ng/ml, wenn auch Hb, MCH und MCV erniedrigt ist, kann jedoch auf eine Eisenmangelanämie (IDA) geschlossen werden.
ZnPP
Würde ich aufgrund der geringen Spezifizität nur als zusätzlichen Marker verwenden, wenn bei einem hohem Speichereisen (u.a. Serum-Ferritin), u.a. bei niedrigen Hb, der Verdacht auf ein potentiellen Funktionseisenmangel vorliegt.
sTfR-Log-Ferritin-Index (FI)
Der sTfR-Log-Ferritin-Index (FI) ist für mich der optimale Wert um einen Mangel an Funktions- und Speichereisen bei einer Eisenmangelanämie festzustellen bzw. zu bestätigen. Dies speziell, da FI bei einer ACD niedrig bleibt, weil hier Eisen-Supplemente oder Infusionen ungut wären. Insofern kann dieser Marker auch in Grenzfällen benützt werden um zwischen IDA und ACD un unterscheiden, z.B. bei entzündungsbedingtem hohem Ferritin, wo dann nicht klar ist ob eine IDA oder ACD vorliegt.
Transferrin und Transferrin-Sättigung (TfS)
TfS kann bei einer Differential-Diagnose bzw. Behandlungskontrolle hilfreich sein, oder wenn sTfR-Log-Ferritin-Index (FI) nicht verfügbar ist. Es ist für mich jedoch, wenn ich die Auswahl habe, kein Wert der ersten Wahl und kein Wert den ich im Bereich eines Screenings bzw. einer regelmäßigen Kontrolle messen lassen würde, da die Spezifizität recht niedrig ist.
Zu Vitamin A und Kupfer
Das für mich auffälligste, außer der sehr alten Studie von Wintrobe et al., war, dass keine andere Studie, welche ein breites Panel an Eisen-Relevanten Blutwerten untersuchte auf den Kupfer-Status schaute. In Bezug auf Retinol scheint es zudem vorwiegend Studien zu geben, welche die Situation in Afrika und Arabien untersuchen. Anscheinend wird nur dort, wo der Vitamin A bzw. Retinol-Mangel wegen Mangelernährung ein großes Problem ist, wird auch danach geschaut. Diese Studien stellten jedoch einen Zusammenhang zwischen niedrigen Retinol-Spiegeln und einer Eisenmangel-Anämie her, wobei der niedrige Retinol-Spiegel als (zumindest) mitverantwortlich für den niedrigen Eisenspiegel gemacht wurde. Allerdings waren die Vitamin A-Spiegel in den von mir betrachteten Studien, bei starkem Eisenmangel, mit < 200 µg/l wirklich sehr, sehr niedrig. Ich habe solche (schlechten) Werte noch nie auf Labor-Ergebnissen gesehen.
Bedeutet: Die Relevanz von Retinol und Kupfer, bzw. die Werte ab denen es kritisch wird, sind für mich nicht einschätzbar. Wer hier gute Studien kennt, her damit! Zu Abklärung einer IDA bzw. eines Funktionseisenmangels würde ich beide Werte jedoch immer messen lassen.
Ceruloplasmin
Hier bin ich nicht in die Tiefe gegangen. Auf jeden Fall kann Aceruloplasminämie [2], eine Störung des Eisenstoffwechsels bei der die Aktivität der Ceruloplasmin-Ferroxidase-Aktivität vollständig fehlt, sehr gefährlich sein, was dann auch mit niedrigen CP und wenig Kupfer im Serum einhergeht. In meinem Kupfer Artikel Teil 2 schrieb ich vor einigen Jahren:
„Produziert wird CP in der Leber, stimuliert durch Schilddrüsen-Hormone. Eine zweite Form von CP wird wohl im Gehirn, der Niere und den Lungen produziert, und spielt wohl eine entscheidende Rolle beim (Ab-)Transport von Eisen aus den Organen. Ist zu wenig Kupfer vorhanden, dann sinkt der CP-Spiegel, u.a. da dieses Protein schnell abgebaut wird wenn es nicht an Kupfer gebunden ist“
Wenig Kupfer macht weniger CP. Dies ist der Grund, warum ich gerne Kupfer im Serum und CP bestimmen lasse, insbesondere wenn regelmäßig viel Zink, Molybdän und / oder auch Schwermetall-Chelatoren eingenommen werden, welche Kupfer im Körper verringern. Zwar ist Kupfer bei Schwermetall-Belasteten oft hoch, aber über einige Jahre der Behandlung sinkt der Spiegel, bzw. die Kupfer-Anreicherungen in den Geweben, deutlich.
Wenn es darum geht einen Funktionseisenmangel Abzuklären (auch IDA und ACD), würde ich diesen Wert, speziell bei niedrigen Vitamin A oder Kupfer immer messen lassen.
CRP, IL-6, GOT, GPT, GGT
Diese Werte sind in der Regel gut bekannt, oft erwähnt und im Kontext IL-6 und Hepcidin in Teil 2 dieser Serie im Detail besprochen worden. Deswegen vertiefe ich Ihre Betrachtung hier nicht weiter. In jedem Fall müssen diese Werte mit in die Bewertung der eisenrelevanten Werte mit einbezogen werden, da faktisch kein Eisenmarker außer ZnPP sowie sTfR (jedoch nicht der Ferritin-Index!) unabhängig vom Entzündungsgeschehen ist.
Was das alles bedeutet….
… ist, das eine richtige Diagnose nur dann einfach ist, „wenn das Kind schon in den Brunnen gefallen ist“. Dann beginnt jedoch erst die Suche nach den wirklichen Ursachen, weil eine Dauereinsen-Supplementation bei IDA keine langfristige Lösung und bei ACD generell unangebracht ist [21]. Die Diagnose der „Graubereiche“ ist schon deutlich schwieriger, wobei ich hier den sTfR-log-Ferritin-Index als ein hilfreiches Mittel ansehe und Klarheit zu schaffen, wenn Serum-Ferritin Werte niedrig (u.a. < 30 ng/ml) aber noch nicht katastrophal (.a. =< 10 ng/ml) sind.
Anhang – Tabellen aus den Studien
Hinweis: Der nächste kurze Abschnitt ist nur für die Freunde des Blogs sichtbar.
Table 3. Ability of Ferritin, TfR, TfR/Ferritin Ratio and TfR-F Index to Identify Patients With Iron Deficiency
| Empty Cell | IDA v ACD | IDA + COMBI v ACD | COMBI v ACD | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ferritin | TfR | TfR × 100/Ferritin | TfR-F Index | Ferritin | TfR | TfR × 100/Ferritin | TfR-F Index | Ferritin | TfR | TfR × 100/Ferritin | TfR-F Index | |
| False negative | 1 | 3 | 1 | 0 | 6 | 4 | 3 | 1 | 5 | 1 | 2 | 1 |
| False positive | 1 | 4 | 1 | 0 | 1 | 4 | 1 | 0 | 1 | 4 | 1 | 0 |
| True negative | 63 | 60 | 63 | 64 | 63 | 60 | 63 | 64 | 63 | 60 | 63 | 64 |
| True positive | 47 | 45 | 47 | 48 | 59 | 61 | 62 | 64 | 12 | 16 | 15 | 16 |
| Sensitivity | 0.98 | 0.94 | 0.98 | 1.00 | 0.91 | 0.94 | 0.95 | 0.98 | 0.71 | 0.94 | 0.88 | 0.94 |
| Specificity | 0.98 | 0.94 | 0.98 | 1.00 | 0.98 | 0.94 | 0.98 | 1.00 | 0.98 | 0.94 | 0.98 | 1.00 |
| Positive PV | 0.98 | 0.92 | 0.98 | 1.00 | 0.98 | 0.94 | 0.98 | 1.00 | 0.92 | 0.80 | 0.94 | 1.00 |
| Negative PV | 0.98 | 0.95 | 0.98 | 1.00 | 0.91 | 0.94 | 0.95 | 0.98 | 0.93 | 0.98 | 0.97 | 0.98 |
| Efficiency | 0.98 | 0.94 | 0.98 | 1.00 | 0.95 | 0.94 | 0.97 | 0.99 | 0.93 | 0.94 | 0.96 | 0.99 |
* Für jeden Parameter wurde eine Effizienzkurve zur Unterscheidung zwischen ACD- und IDA-Patienten erstellt, und der maximale Punkt der Kurve wurde als Grenzwert für alle Patientenpopulationen verwendet. Die auf den Effizienzkurven basierenden Grenzwerte waren 41 μg/L für Ferritin, 2,7 mg/L für TfR, 4,5 für TfR × 100/Ferritin und 1,5 für den TfR-F Index. PV = prädiktiver Wert.
[/wpmem_logged_in]
Links / Quellen
- [1] Studies on Copper Metabolisn: II. Hematologic Manifestations of Copper Deficiency in Swine, M.E. Lahey, C.J. Gubler, M.S. Chase, G.E. Cartwright, M.M. Wintrobe, Blood, Volume 7, Issue 11, 1952, Pages 1053-1074, DOI: 10.1182/blood.V7.11.1053.1053.
- [2] Aceruloplasminemia, Hiroaki Miyajima et al., GeneReviews, Seattle (WA): University of Washington, Seattle; 1993.
- [3] Ferritin in the Serum of Normal Subjects and Patients with Iron Deficiency and Iron Overload, et al., A. Jacobs, Br Med J 1972; 4 doi: 10.1136/bmj.4.5834.206
- [4] Serum ferritin is an important inflammatory disease marker, as it is mainly a leakage product from damaged cells, Douglas B Kell 1, Etheresia Pretorius, Metallomics, 2014 Apr;6(4):748-73. doi: 10.1039/c3mt00347g.
- [5] Usefulness of the serum ferritin concentration in the detection of iron deficiency in a general hospital., J. Mazza et al., Can Med Assoc J. 1978 Oct 21; 119(8): 884–886., PMCID: PMC1819106
- [6] Serum hepcidin concentrations correlate with ferritin in patients with inflammatory bowel disease, Ingo Mecklenburg et al., Observational Study J Crohns Colitis, 2014 Nov;8(11):1392-7. doi: 10.1016/j.crohns.2014.04.008. Epub 2014 May 11.
- [7] Associations between serum hepcidin, ferritin and Hb concentrations and type 2 diabetes risks in a Han Chinese population, Xin Guo et al., Br J Nutr, 2013 Dec;110(12):2180-5. doi: 10.1017/S0007114513001827. Epub 2013 Jun 7.
- [8] Hepatic iron is the major determinant of serum ferritin in NAFLD patients, John D Ryan et al., Liver Int, 2018 Jan;38(1):164-173. doi: 10.1111/liv.13513. Epub 2017 Jul 29.
- [9] Correlation Between Serum Ferritin and Hepcidin Levels in Chronic Hepatitis C Patients, Maria Gill, Cureus. 2021 Aug; 13(8): e17484., Published online 2021 Aug 27. doi: 10.7759/cureus.17484
- [10] Serum and salivary ferritin and Hepcidin levels in patients with chronic periodontitis and type 2 diabetes mellitus, Lin-Na Guo et al., BMC Oral Health. 2018; 18: 63., Published online 2018 Apr 10. doi: 10.1186/s12903-018-0524-4
- [11] Serum transferrin receptor: a quantitative measure of tissue iron deficiency, B S Skikne et al., Blood, 1990 May 1;75(9):1870-6.
- [12] Serum transferrin receptor and its ratio to serum ferritin in the diagnosis of iron deficiency, K Punnonen et al., Blood, 1997 Feb 1;89(3):1052-7.
- [13] Iron assessment tests: transferrin receptor vis-à-vis zinc protoporphyrin, Robert F Labbé et al., Review Clin Biochem, 2004 Mar;37(3):165-74. doi: 10.1016/j.clinbiochem.2003.10.006.
- [14] Serum transferrin receptor and zinc protoporphyrin as indicators of iron status in African children, Michael B Zimmermann et al., Comparative Study Am J Clin Nutr, 2005 Mar;81(3):615-23. doi: 10.1093/ajcn/81.3.615.
- [15] Limited value of zinc protoporphyrin as a marker of iron status in chronic hemodialysis patients, C Canavese et al., Clin Nephrol, 2000 Jan;53(1):42-7.
- [16] Diagnostic utility of zinc protoporphyrin to detect iron deficiency in Kenyan pregnant women., Mwangi, M.N., Maskey, S., Andang’o, P.E. et al., BMC Med 12, 229 (2014). https://doi.org/10.1186/s12916-014-0229-8
- [17] Effectiveness of zinc protoporphyrin/heme ratio for screening iron deficiency in preschool-aged children, Kyeong Hee Yucorresponding, Nutr Res Pract. 2011 Feb; 5(1): 40–45., Published online 2011 Feb 28. doi: 10.4162/nrp.2011.5.1.40
- [18] Assessment of iron deficiency, Chaim Hershko, Haematologica. 2018 Dec; 103(12): 1939–1942., doi: 10.3324/haematol.2018.205575
- [19] Das kleine und das große Blutbild, mük, München Klinik
- [20] Labordiagnostik bei Störungen des Eisenstoff wechsels, Fachinformation 0109, GanzImmun AG
- [21] Eisenmangel ohne Anämie – ein heißes Eisen? Nicht hämatologische Auswirkungen des Eisenmangels: Welche sind belegt, wann kommen sie zum Tragen?, Ferdinand Martius, Medizinische Universitätsklinik, Kantonsspital Bruderholz, Schweiz Med Forum 2009;9(15–16):294–299
- [22] Biochemical markers and hematologic indices in the diagnosis of functional iron deficiency, Christian Thomas et. al, Clin Chem, 2002 Jul;48(7):1066-76.
- [23] Serum retinol, iron status and body composition of lactating women in Nandi, Kenya, G A Ettyang et al., Ann Nutr Metab, 2003;47(6):276-83. doi: 10.1159/000072400.
- [24] Serum retinol levels are positively correlated with hemoglobin concentrations, independent of iron homeostasis: a population-based study, Seyed Mojtaba Jafari et al., Nutr Res, 2013 Apr;33(4):279-85. doi: 10.1016/j.nutres.2013.02.004. Epub 2013 Mar 11.
- [25] Utility of serum ferritin as a measure of iron deficiency in normal males undergoing repetitive phlebotomy, R A Jacob et al., Blood, 1980 Nov;56(5):786-91., PMID: 7426747
- [26] 025: Why You Need to Manage Your Iron Status and How to Do It, Mastering Nutrition Episode 25, Chris Masterjohn, PhD, Jan 27, 2017
- [27] Induction of ceruloplasmin synthesis by retinoic acid in rats: influence of dietary copper and vitamin A status, E F Barber 1 , R J Cousins, J Nutr, 1987 Sep;117(9):1615-22., doi: 10.1093/jn/117.9.1615.
Der Rest dieses Beitrages ist nur für eingeloggte Freunde des Blogs einsehbar. Bitte logge Dich ein, oder schaue unter dem Menüpunkt 'Freunde des Blogs' für weitere Informationen wenn ein ernsthaftes Interesse besteht hier weiter zu lesen.







Neuste Kommentare