Dr. Douglas Wallace – Von Mitochondrien, Haplotypen & maternal Heteroplasmy
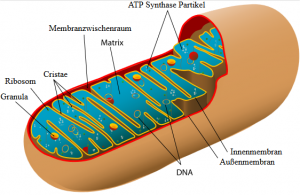
Mitochondrium. Quelle: Wikipedia. Lizenz: Gemeinfrei
Heute geht es um Mitochondrien – einen Begriff den ich schon häufig hier erwähnt habe – sowie den wohl weltbesten Mitochondrien-Forscher: Dr. Douglas Wallace, dem gerade erst der Franklin-Award verliehen wurde.
Was sind Mitochondrien? Es sind ‚vereinfacht geschrieben‘ die Energiekraftwerke in unseren (eukaryontischen) Zellen, welche ATP (unseren universellen und unmittelbar verfügbaren Energieträger) produzieren. Mitochondrien sind dabei Organellen in unseren Zellen.
Spannend war für mich zu verstehen, dass die Mitochondrien eine eigene DNA haben (-> Mitochondrial DNA -> mtDNA), welche sich von der Zell-DNA (-> Nuclear DNA -> nDNA) deutlich unterscheidet. Wird über DNA, Gentherapie, genetische Faktoren & Vererbung gesprochen und berichtet dann ist in der Regel auch die nDNA gemeint, also die DNA des Zellkerns. Die mtDNA ist in der Regel nicht im Fokus, wobei Sie eine extrem wichtige Rolle spielt.
Inhaltsverzeichnis für den Schnellzugriff
Dr. Douglas Wallace & die Wichtigkeit der mtDNA
Nach Dr. Douglas Wallace sind ca. 80% der genetisch bedingten Krankheiten mtDNA und nicht nDNA verursacht (-> Mitochondriopathie) u.a. wenn Mitochondrien mit verschiedener DNA (-> meist mutiert) in unseren Zellen gibt (-> ‚mitochondrial heteroplasmy‚). Je nach Zellart gibt es eine verschiedene Anzahl von Mitochondrien pro Zelle – von ca. 100 bis hin zu vielen Tausend (-> Retina, Stammzellen, etc.). Alleine durch diese Vielzahl (aber auch andere Faktoren) ist die Mutationsrate von Mitochondrien im Vergleich zur nDNA recht hoch. Die Evolutionsrate wird ca. 10-20 mal höher und die Mutationsrate ca. 100-1000 mal höher eingeschätzt als die der nDNA. In der Forschung wird auch immer klarer, das die Fehlfunktionen von Mitochondrien (und damit unserer Energieproduktion) weitreichende Auswirkungen auf viele Krankheitsbilder hat (u.a. degenerative Krankheiten, Herzkrankheiten, Demenz, Alterung und Krebs) [1].
Hoch spannend: Die mtDNA wird rein mütterlicherseits vererbt (‚maternal inheritance‘) – also nicht wie die nDNA, welche eine ‚mix‘ aus der nDNA von Mutter und Vater ist. Möchte man viele erbliche Krankheiten verstehen ist es also sehr wichtig über Erkrankungen bei den mütterlichen Vorfahren bescheid zu wissen. Der Anteil an der Schädigung der mitochondrialen DNA gegenüber einer intakten Referenz-mtDNA wird dann auch als ‚percent Heteroplasmy‚ benannt [1] und folgend berechnet:
„Aligned all mtDNA genomes against the reference sequence. Any deviance at a specific position from the reference was a „mutation“. The % heteroplasmy was calculated by dividing the total number of mutations at a certain nucleotide position by the total number of genomes represented at the position multiplied 100.“ [2]
So können nach Wallace subtile mitochondriale Fehlfunktionen (bzw. Defizite) Organ-Spezifische Auswirkungen haben. Das ganze kreiert dann auch ein Dilemma für Mütter, welche Ihre eigene mtDNA an den Nachwuchs vererben. Ist diese Homoplasmisch (wenn eine Mutation bereits alle Mitochondrien-Kopien einer Zelle gleichermaßen betrifft) dann hilft auch eine Pränataldiagnostik nicht:
„Obviously, all forms of prenatal diagnosis are useless for a woman harboring a homoplasmic mtDNA mutation because all of her fetuses will inherit her mutation.“ [3]
Weil – so wie ich Wallace verstehe – klar ist, das die Mutation mütterlicherseits vererbt wird. Was mir jedoch noch unklar ist, wie dann die im Leben erworbenen mtDNA-Defekte bzw. Mutationen über die Eizelle in den Nachwuchs vererbt werden. Da ich aktuell nichts in Planung habe, habe ich davon abgesehen das auch noch zu recherchieren 😉
‚Historische‘ adaptive Polymorphismen -> Haplotypen
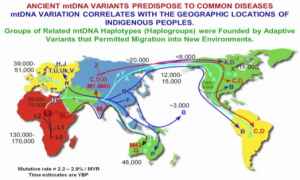
Haplotypeen & Ausbreitung Quelle
Als ‚Haplotypen‚ werden die verschiedenen ‚historischen‘ mtDNA Mutationen bezeichnet, welche sich in den letzten ca. 200.000 Jahren bei der Migration der ersten neuzeitlichen Menschen aus Afrika gebildet haben und die weitervererbt wurden. Meist hat sich dabei eine mtDNA Variante durchgesetzt (vererbt) die auf die neuen regionalen Anforderungen optimal (bzw. besser) adaptiert war.
Nach Dr. Doug Wallace (Video, min. 15:57) haben die verschiedenen Haplotypen eine unterschiedliche Kopplungseffizienz (‚coupling efficiency‘) bei der Energieproduktion. Menschen mit nordeuropäischen Haplotypen erzeugen weniger ATP pro Kalorie (jedoch mehr Wärme -> Lose gekoppelte, min 44:09 im Video) im Vergleich zu den afrikanischen Ur-Typen (Eng-gekoppelt -> Mehr ATP). Der Hintergrund: Im kaltem Nordeuropa war die körpereigene Wärmeproduktion ein Überlebensvorteil – in Afrika war es besser schnell vor einem Löwen weg rennen zu können (nach Dr. Wallace – mit seinem sehr pointiertem trockenem Humor). So lässt sich über die mtDNA auch die Migration der Menschen über den Globus recht gut nachvollziehen, wie es Nebenstehendes Bild aufzeigt.
Vortrag von Dr. Wallace
Ein gutes Video zum Einstieg bei Wallace ist das folgende – in den Links am Ende dieses Blogpost finden sich dann auch noch einige andere Videos von ihm. Meine Einführung in die grobe Thematik sollte dann auch das folgende Video etwas verständlicher machen – denn ich hatte anfangs einige Probleme das Video ohne diese Grundlagen beim ersten anschauen sofort zu verstehen.
Hinweis: Durch aktivieren der Wiedergabe (Play-Button) werden Daten von Youtube nachgeladen. Bitte beachten Sie dazu unsere Datenschutzerklärung
Auswirkungen der mtDNA Mutationen
Dr. Wallace und auch Dr. Kruse geben in Ihren Vorträgen dann u.a. die sich stark veränderten Umweltfaktoren in Bezug auf nnEMF (Mensch gemachte Mikrowellen, Mobilfunk & Co.), Ernährung (Pestizide, hohe Verarbeitung der Nahrung, geänderte Nahrungsgewohnheiten), etc. pp. als Verstärker für die mtDNA Mutationen mit wohl zunehmend negativen Auswirkungen an. Schädigungen bzw. Mutationen der mtDNA können schwerwiegende Folgen haben, wenn dieses zur Regel wird. U.a. [4]:
- Verlust der Instandhaltung des elektrischen und chemischen Transmembranpotentials der inneren Mitochondrien-Membran,
- Veränderungen in der Funktion der Elektronentransportkette,
- eine Reduktion im Transport wichtiger Metaboliten in die Mitochondrien.
All diese Veränderungen haben dann eine reduzierte Effizienz in der oxidativen Phosphorylierung und so eine Reduktion in der ATP-Produktion (-> zelluläre Energie) und oft auch mehr oxidativen Stress zur Folge. Weniger Energie bedeutet dann mehr Krankheiten, mehr metabolische Entgleisungen und irgendwann den (vorzeitigen) Tod.
Interessant fand ich noch, dass wohl mit der Ergänzung bzw. Zufuhr von ausreichend Coenzym Q10, NAD(H), L-Carnitin, α-Liponsäure und Phospholipiden wohl Verbesserungen in der mitochondrialen Funktion erreicht werden können [4][5]. Auch die Gabe von Kreatin soll sich positiv auswirken können [6].
Gedanken zur mütterlichen Vererbung der mtDNA
Ich denke der Allgemeinheit ist noch gar nicht klar wie wichtig die Gesundheit & Lebensführung, insbesondere der Mütter, für den späteren Nachwuchs ist.
Gerade die neuen Risiken: Mensch gemachte (non-native) EMF, künstliches Blaulicht, energiearme und hoch verarbeitete Ernährung, Zusatz- und Giftstoffe, eine weitere Verdichtung des Arbeitslebens (->Stress) und zu wenig ‚Auslauf‘ unter der Sonne sind nach meiner Ansicht (neben anderen) Treiber dieser Entwicklung. Anders kann ich mir die epidemieartige Ausbreitung der Zivilisationskrankheiten kaum noch erklären. Zwar bin ich der Meinung das die Ernährung eine wichtige Rolle spielt, alles ist mit dieser jedoch nicht richtbar. Die Umweltfaktoren wiegen ggf. schwerer als ich bisher angenommen hatte – und eine gute (bzw. weniger schlechte) Ernährung verlangsamt dann nur den Verfall.
Mein Fazit
Klassische Genetik war gestern – mitochondriale Genetik ist heute – mag man meinen. Das ganze spielt dann auch noch zusammen mit der Epi-Genetik, also Veränderungen der nDNA aufgrund von Umweltfaktoren und in Interaktion mit der mtDNA (‚bidirectional crosstalk‘) [7].
Für mich zeigt das Ganze auf, wie schnell sich unsere Genetik aufgrund von Umweltfaktoren auch negativ, also zu unseren Ungunsten, ändern kann – inkl. Vererbung dieser (mitochondrialen) Krankheiten. Angesichts der sich in den letzten Jahrzehnten krass verändernden Umwelt (-> EMF & Co.) schwant mir hier nichts gutes.
Positiv sehe ich hingegen, dass alles was wir täglich machen, wo wir leben, mit was wir uns umgeben, was und wie wir denken und was wir essen – einen Einfluss auf unsere mtDNA und die Epi-Genetik hat. Das gibt mir zumindest zum Teil die (illusorische?) Vorstellung einer gewissen Kontrolle über mein Leben, meine Vitalität und meine Zukunft. Und das stimmt mich positiv in dem was ich tue und hier zum Teil dokumentiere 🙂
Videos
- Dr. Doug Wallace – Talk from 8th Annual Oliver Smithies Symposium, The eighth annual Oliver Smithies Symposium was held on Wednesday, May 20th 2015 at the University of Wisconsin – Madison
- KCU – University Lecture Series – Dr. Douglas Wallace, University Lecture Series delivered by Dr. Douglas Wallace Tuesday, May 3rd, 2016 At Kansas City University of Medicine and Biosciences
- Genetic & Metabolic Basis of LHON – Doug Wallace, PhD, United Mitochondrial Disease Foundation, 2013 Symposium, Newport Beach, CA
Quellen
- [1] Measuring Rates of mtDNA Heteroplasmy Using a NextGen Sequencing Approach – Mitchell M. Holland, Ph.D., Former Director, Forensic Science Program, Associate Professor, Biochem & MolBio, Penn State University, University Park, PA, 2015
- [2] How to calculate the percent of mitochondrial heteroplasmy, StackExchange
- [3] Mitochondrial DNA Genetics and the Heteroplasmy Conundrum in Evolution and Disease, Douglas C. Wallace and Dimitra Chalkia, Cold Spring Harb Perspect Biol. 2013 Nov; 5(11): a021220.
- [4] Mitochondrial Dysfunction and Chronic Disease: Treatment With Natural Supplements, Garth L. Nicolson, PhD, Integr Med (Encinitas). 2014 Aug; 13(4): 35–43.
- [5] Rejuvenate Your Cells by Growing New Mitochondria, By Kirk Stokel, LifeExtension Magazine, 2010
- [6] Creatine Supplementation Normalizes Mutagenesis of Mitochondrial DNA as Well as Functional Consequences, Mark Berneburg et al., Journal of Investigative Dermatology, Volume 125, Issue 2, August 2005, Pages 213-220
- [7] The mitochondrial side of epigenetics., Castegna A, Iacobazzi V., Infantino V., Physiol Genomics. 2015 Aug;47(8):299-307. doi: 10.1152/physiolgenomics.00096.2014. Epub 2015 Jun 2.


![Zusammenfassung der NTP-Studie in Bezug auf die beobachteten Auswirkungen & Krankheiten. Quelle: [13]](https://hcfricke.com/wp-content/uploads//2018/08/ntp-summary.png)





Neuste Kommentare