Nrf2 Teil 1: Der zentrale Schalter für die ‚Hoch-Regulation‘ der antioxidativen Systeme und der biochemischen Entgiftung (Detox Phase II & III, Glutathion-Systeme & Membran-Transporter)
Nrf2 (Abkürzung für Nuclear Factor E2-related Factor) ist ein zellulärer Schalter, der antioxidative Systeme, die Entgiftung und zelluläre Abwehrkräfte orchestriert [2]. Es ist für die Gesunderhaltung des Körpers von entscheidender Bedeutung, da es ein Hauptregulator dafür ist, wie wir mit unserer alltäglichen Umgebung und deren Giften umgehen – um nicht sofort von allem (‚bösen‘) krank zu werden.
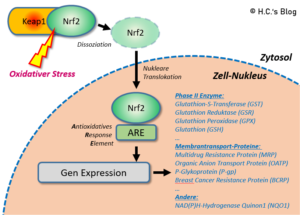
Im ‚Normalfall‘ ist Nrf2 ist im Zytosol der Zelle vorhanden und dort an Keap1 (Kelch-like ECH-associated protein 1) gebunden (siehe Abbildung oben). Das an Cystein reiche Keap1 fungiert in dem paar mit Nrf 2 als Sensor für oxidativen Stress, z.B. Gifte (Arsen, Dioxin, Schwermetalle, …), verschiedene pflanzliche Stoffe, intensiver Sport, und setzt bei bedarf Nrf2 frei [2][3][5]. Danach
- wandert (->transloziert) Nrf2 in den Zellkern und
- bindet sich dort an das antioxidative Response-Element (ARE),
- eine spezielle Promotorregion von Genen welche für die Transkription kritischer Komponenten der Entgiftung kodieren.
Damit wird in Folge das Ablesen von bestimmten Genen gefördert, was letztendlich dazu führt, das vermehrt bestimmte Enzym-Komplexe ‚gebaut‘ werden. Der Nrf2/ARE-Signalweg kann über 500 Gene einschalten, die der Zelle helfen, Schutzmoleküle zu erzeugen. Dazu gehören antioxidative Elemente, Entgiftungsenzyme und Proteine, die für die Glutathion-Synthese und das Recycling benötigt werden, wie die Glutathion-S-Transferase (GST), die Glutathion-Reduktase (GSR) und die Glutathion-Peroxidase (GPX). Nrf2 reguliert auch Proteine hoch, die für die Entgiftung in Phase III und den Transfer von toxischen Substanzen aus der Zelle und dem Zentralnervensystem verantwortlich sind (u.a. die Membrantransporter P-gp, BCRP und MRP2). [2][3][5].
Obwohl Nrf2 auf einem basalen Niveau gehalten wird, hat es eine Halbwertszeit von etwa 15-20 Minuten [13][34] und wird in Zellen, die keinen Stress erfahren, ständig abgebaut [2]. Aus diesem Grund, zumindest folgere ich das, muss nach Dr. Shade Nrf2 am besten auch über einen ‚Punch‘ aktiviert werden [34]: Eine gezielte (hoch dosierte) Stress-Indizierung die eine bestimmte Schwelle überschreiten muss, optimal wohl Liposomal – oder, so sehe ich es, zumindest auf nüchternen Magen (z.B. mit Haritaki, EGCG).
M. Pall [15] führt noch aus, das es jedoch noch viele andere Mechanismen gib, die ins Spiel kommen, was das Nrf2-Steuerungssystem sehr komplex macht. So gibt mehrere Proteinkinasen, die bei der Regulierung von Nrf2 eine Rolle spielen, darunter der ERK/JNK-Signalweg, der PI3K/Akt/GSK-3β-Signalweg, die Proteinkinase C, AMPK und die Proteinkinase G. Wenn das für euch böhmische Dörfer sind – willkommen im Club. Auch Isothiocyanate, H2O2 (Wasserstoff-Peroxid), langkettige Omega-3-Fettsäuren und Carotinoide wirken durch Reaktion mit Keap1-reaktiven Thiolen, wobei die letzten drei durch ihre Oxidationsprodukte wirken. So wirken dann Allium-Schwefelverbindungen (u.a. aus Zwiebeln), Isothiocyanate und Carotinoide über die ERK-Stimulation. Doch dazu in den nächsten Abschnitten mehr – wenn es um Nahrungsergänzungsmittel geht, mit denen eine Nrf2-Aktivierung gezielt gefördert werden kann.
Allerdings – und das behandeln die folgenden Abschnitte – kann Keap1/Nrf2 auch (epigenetisch) blockieren, von uns moduliert aber auch überaktiviert werden. Dies ist der Stoff der nächsten Abschnitte.
Nrf2: Wirkung auf Krankheiten, Entzündungen (NF-κB), oxidativen & nitrosativen Stress, Glutamat & GABA, etc.
Ist der Nrf2-Signalweg beeinträchtigt (-> Suppremiert) dann sind damit in Folge eine Unmenge an Krankheiten bzw. ‚Symptomen‘ assoziiert. M. Pall [15] nennt dann auch nur einige chronische Entzündungskrankheiten, welche sich beim Menschen (oder in Tiermodellen) verbessern, wenn Nrf2, und damit die antioxidativen Systeme hochreguliert werden:
- Verschiedene Herz-Kreislauf-Erkrankungen,
- Nierenerkrankungen,
- Lungenerkrankungen,
- Krankheiten mit toxischen Leberschäden,
- einer mit Cholesterase verbundenen Bilirubinerhöhung [2],
- Krebs (Prävention),
- Diabetes, metabolisches Syndrom, Adipositas,
- Autoimmunkrankheiten, Multiple Sklerose
- entzündliche Darmerkrankungen,
- HIV/AIDS,
- Sepsis und Epilepsie.
Pall gibt an, das für 16 weitere Krankheiten auch noch Evidenz bestehe – jedoch weniger stark mit Studien belegt. All dies wird für regelmäßige Leser dieses Blogs keine Neuigkeit sein, denn oxidativer (und nitrosativer) Stress ist faktisch mit jeder Art von Krankheit verbunden, ja faktisch die wahrscheinliche Ursache für alle Krankheiten [8][14][24] bzw. ‚Krankheit an sich‘ (Levy). Wer den oxidativen Stress mindert, reduziert denn auch in der Regel die Schwere bzw. den Ausbruch von Symptomkrankheiten. Die Nrf2-Aktivierung bewirkt neben der antioxidativen [35] auch eine Vielzahl von entzündungshemmender Wirkungen. Nach M. Pall [15]:
- eine verminderte NF-κB Expression und
- eine verminderte Aktivität einer Reihe von Entzündungsmediatoren, darunter Zytokine, Chemokine, Adhäsionsmoleküle, TNF-alpha, COX-2, MMP-9 und iNOS,
- eine Erhöhung von IL-10, ein Zytokin, was begrenzend und hemmend im Rahmen von Entzündungsprozessen wirkt (u.a. Vermeidung septischer Schock),
- eine Erhöhung entzündungshemmender Prostaglandine und Enzyme [3],
- eine Senkung eines übermäßigen intrazellulären Calciumspiegels,
- u.a. wohl durch eine Senkung einer übermäßigen NMDA-Aktivität (u.a. durch zu viel Glutamat-Bildung -> Quecksilber, Endotoxine und zu wenig Magnesium).
- Meint: Weniger Ca-Einstrom in die Zelle fürder die NMDA2 & Co. Rezeptoren die Calcium-Kanäle ähnlich den VGCC darstellen.
Kern in diesem Prozess ist wohl die Senkung von NF-κB, was ja, wenn erhöht, wiederum Nrf2 senkt [15]. So erklärt sich auch langsam C. Shades Ausspruch ‚Inflamation blocks detoxification‘, was sich auch in meinem Schaubild (oben) widerspiegelt. Dr. Retzek [31] merkt noch an, das:
- NRF2 500 Gene inaktiviert die mit NF-κB Stoffwechsel zu tun haben.
- NRF2 500 Gene aktiviert die für Produktion und den Stoffwechsel von GSH & Co. zuständig sind.
So haben die ‚Supergene‘ bzw. Transkriptionsfaktoren nach Retzek folgende Grundaufgabe, wobei ich bemerken möchte, das NF-κB für eine ausreichende Immunantwort schon sehr wichtig ist – aber eben nicht chronisch erhöht sein sollte [31]:
- NF-κB: Oxidation => Abwehr => Entzündung => Kampf
- Nrf2: Antioxidation => Detox => Ausleitung => Regeneration
NF-κB über überwiegt dann auch bei wiederholtem Stress, parasitären, bakteriellen und viralen Infektionen (u.a. EBV, CMV, Herpes, Borreliose), Elektrosmog (EMF), UV-Strahlung, Radioaktivität, mangelnder Mikronährstoffversorgung, chronischer Vergiftung (u.a. Quecksilber), etc. Die natürlichen Inhibitoren von NF-κB sind dann auch Substanzen, welche Nrf2 fördern (-> Haritaki, Allicin, Quercetin, Curcumin, Ginkgo, EGCG, liposomales DIM, etc.).
Ein weiterer wichtiger Punkt kann noch sein, das wenn durch die Nrf2-Suppression die Glutathion-Systeme heruntergefahren werden, die NO/ONOO-Werte ansteigen (-> Peroxinitrid, NO/iNOS), was dann, neben der VGCC- und NMDA-Aktivierung (-> Calcium-Kanäle), dazu führt das die Glutamat-Achse überwiegt (-> Sympathikus, Erregung) und GABA gesenkt wird. Hier kann dann teils GABA helfen bzw. Substanzen die Glutamat unterdrücken bzw. das GABA-System bzw. dessen Synthese fördern (-> Para-Sympathikus, Entspannung). [28] Ich schreibe dies, weilzu viel Glutamat auch dazu führt, die Entgiftungsfunktionen im Körper zu bremsen.
- Allgemein:
- Catalase (CAT) – Entschärft Wasserstoff-Peroxid [35]
- Superoxid-Dismutase (SOD1&2) – Entschärft Superoxid [15]
- 70 kilodalton Heat-Shock-Protein (Hsp70) [34]
- Phase I
- Cytochrome P450 Monooxygenasen System (FMOs) [34]
- Phase II
- Glutathion-Reduktase (GR) – das Enzym, das oxidiertes Glutathion (GSSG) in GSH umwandelt.
- Glutathion Synthetase (GSS) [34] – wichtig für die de-novo Synthese von GSH
- Glutamat-Cystein-Ligase (GCL) – wichtig für die de-novo Synthese von GSH
- γ-glutamat-Cystein-Ligase-Katalysator-Untereinheit (GCLC) – wichtig für die de-novo Synthese von GSH
- Glutathion-S-Transferase (GST) – Katalysiert die Konjugation von GSH an xenobiotische Substrate, u.a. Hg-Ionen an GSH
- NAD(P)H:Quinon-Oxidoreduktase-1 (NQO1) – die Elektronen spendet und eine Vielzahl von Chemikalien und Medikamenten entgiftet.
- Häm Oxygenase (HO-1) – ist ein Enzym, das den Abbau von Häm in das Antioxidans Biliverdin, den entzündungshemmenden Wirkstoff Kohlenmonoxid, und Eisen katalysiert.
- UDP-Glucuronyltransferasen (UGTs) – katalysiert die Konjugation von Glucuronsäure mit Medikamenten, Chemikalien und Toxinen, wodurch diese wasserlöslicher werden und leichter ausgeschieden werden können.
- Peroxiredoxin-Sulfotransferase (SULTs) – die Peroxide einschließlich Peroxynitrit zerstören (1&6)
- Glutaredoxin (Grx) – Oxidationsreparatur-Enzym, u.a. wichtig für den Glukose-Stoffwechsel
- Thioredoxin (Trx) – wirken als Antioxidantien, indem sie die Reduktion anderer Proteine durch Cystein-Thiol-Disulfid-Austausch erleichtern
- Thioredoxin-Reduktase (TrxR) – Kalatysiert die Reduktion von Thioredoxin
- Sulfiredoxin (SrxN/1) – Ist am antioxidativen Metabolismus durch Reaktivierung von Peroxiredoxinen beteiligt
- Phase III
- Multidrug resistance proteins (MRPs), speziell wohl MRP2 aber wohl auch 3 & 4 [9][22] als wichtige Membrantransporter, die u.a. konjugierte Toxine aus Zellen bzw. Organen in das Blutplasma bzw. die Gallenkanäle befördern, um Sie anschließend mit dem Kot bzw. Urin auszuscheiden.
- Ggf. auch BCRP und P-gp als weitere Membrantransporter [2].
- Allerdings kann dies wohl auch organspezifisch bzw. unterschiedlich und abhängig von jeweiligen Nrf2-Aktivator sein [7].
- Multidrug resistance proteins (MRPs), speziell wohl MRP2 aber wohl auch 3 & 4 [9][22] als wichtige Membrantransporter, die u.a. konjugierte Toxine aus Zellen bzw. Organen in das Blutplasma bzw. die Gallenkanäle befördern, um Sie anschließend mit dem Kot bzw. Urin auszuscheiden.
Darüber hinaus wird über Nrf2 die Expression von über 500 Genen durch den Nrf2/ARE-Signalweg moduliert, u.a. Proteasom-Untereinheiten, Chaperone, Wachstumsfaktoren und ihre Rezeptoren sowie einige andere Transkriptionsfaktoren.
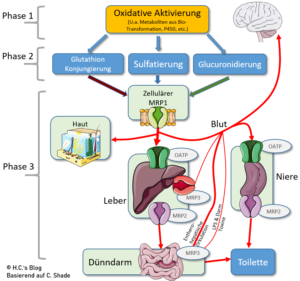
Wie in meinem Grundlagenartikel zu den 3 Phasen der Entgiftung schon angedeutet ist es nicht gut, wenn die niedrigeren Phasen auf Hochtouren laufen – es aber in Phase 3 oder 2 „stockt“. Nach Shade [2] ist denn auch die Ergänzung von N-Acetylcystein (NAC), das die Produktion von Glutathion unterstützt, indem es die Vorstufe L-Cystein bereitstellt, nur begrenzt in der Lage, die intrazellulären Glutathionspiegel zu unterstützen, da die Umwandlung von L-Cystein in Glutathion oft schlecht ist – speziell wenn es an Induktion von Nrf2 mangelt.
Mein Fazit
In meinem Artikel über den EMF-Film ‚Resonance‘ bin ich das erste mal mit Nrf2 in Kontakt gekommen – indirekt, über Melatonin. Melatonin ist unser Schlaf-Hormon, dessen Ausschüttung durch Blaulicht und EMF reduziert wird. Melatonin ist jedoch auch ein Nrf2-Aktivator. Fehlt Melatonin (im Gehirn), dann gibt es dort auch weniger (sekundäre) Antioxidantien – ungut.
Es ist für mich nicht überraschend, dass eine große Anzahl chronischer Krankheiten, die durch oxidativen Stress, Entzündungen und sogenannte mitochondriale Dysfunktion gekennzeichnet sind, zumindest „im Tiermodell“, also in der Regel bei Mäusen und Ratten, durch die Erhöhung von Nrf2 behandelt werden können.
Aus meiner Sicht sind die direkten Auswirkungen einer Aktivierung von Nrf2 auf die antioxidativen System, sowie die Phase II & III der biochemischen Entgiftung fundamental. Pall [15] weist in diesem Kontext auch noch mal auf die Vorteile einer vorwiegend pflanzenbasierten Ernährung mit ihren viele Polyphenolen, Terpenen, Carotinoiden, und anderen hin (u.a. Mediterran und Okinawa). Ernährung ist eben mehr als Kohlenhydrate, Protein, Fett, Mineralien und Vitamine. Hier beginnt aus meiner Ansicht auch die (regelrechte) Panik vor den Lektinen, welche u.a. Gundry schürt, in das Negative zu kippen. Denn all die Nrf2-aktivierenden Substanzen aus den Pflanzen dürften letztendlich Lektine sein -> so genannte „Antinährstoffe“.
Im nächsten Teil gehe ich dann auf potentielle Nrf2-Blockaden ein, die u.a. Shade beschreibt. Dieses könnte ein Hinweis darauf bzw. Aspekt der Thematik sein, warum einige Menschen „besser Entgiften“ als andere.
Links / Quellen
- [1] The Role of the Nrf2/ARE Antioxidant System in Preventing Cardiovascular Diseases, Robert E. Smith, et al., Diseases. 2016 Dec; 4(4): 34., doi: 10.3390/diseases4040034
- [2] A Push-Catch System That Enables Effective Detoxification, Christopher Shade, PhD, and Carrie Decker, ND, Townsend Newsletter, February / March 2018 (Referenzen, Grafiken, Auf einer Seite)
- [3] 5 Ways to Activate the Anti-oxidant Benefits of Nrf2, Dr. Jockers
- [4] Ep 145 – Advanced Detoxification Protocols for Heavy Metals, Leaky Gut, Lyme Disease, and Chronic EBV with Dr. Chris Shade, Biohacking Sectrets Show,
- [5] Lipoic Acid, Linus Pauling Institute (LPI)
- [6] Alpha-lipoic acid as a dietary supplement: Molecular mechanisms and therapeutic potential, Kate Petersen Shay et al., Biochim Biophys Acta. 2009 Oct; 1790(10): 1149–1160., Published online 2009 Aug 4. doi: 10.1016/j.bbagen.2009.07.026
- [7] St. John’s Wort (Hypericum perforatum) induces overexpression of multidrug resistance protein 2 (MRP2) in rats: a 30-day ingestion study, Y Shibayama et al., Food Chem Toxicol, 2004 Jun;42(6):995-1002., doi: 10.1016/j.fct.2004.02.012.
- [8] Death by Calcium, Dr. T. Levy, MedFox Publishing, 2013
- [9] Oxidative and electrophilic stress induces multidrug resistance-associated protein transporters via the nuclear factor-E2-related factor-2 transcriptional pathway, Jonathan M Maher et al., Hepatology, 2007 Nov;46(5):1597-610. doi: 10.1002/hep.21831.
- [10] Innovative drinking water treatment techniques reduce the disinfection-induced oxidative stress and genotoxic activity, Johan Lundqvist et al., Water Res, 2019 May 15;155:182-192. doi: 10.1016/j.watres.2019.02.052. Epub 2019 Feb 28.
- [11] Nicotinamide mononucleotide attenuates brain injury after intracerebral hemorrhage by activating Nrf2/HO-1 signaling pathway, Chun-Chun Wei et al.,Sci Rep. 2017; 7: 717., Published online 2017 Apr 6. doi: 10.1038/s41598-017-00851-z
- [12] Fasting Induces Nuclear Factor E2-Related Factor 2 and ATP-Binding Cassette Transporters via Protein Kinase A and Sirtuin-1 in Mouse and Human, Supriya R. Kulkarni et al., Antioxid Redox Signal. 2014 Jan 1; 20(1): 15–30., doi: 10.1089/ars.2012.5082
- [13] Oxidative stress sensor Keap1 functions as an adaptor for Cul3-based E3 ligase to regulate proteasomal degradation of Nrf2, Akira Kobayashi et al., Mol Cell Biol, 2004 Aug;24(16):7130-9. doi: 10.1128/MCB.24.16.7130-7139.2004.
Der Rest dieses Beitrages ist nur für eingeloggte Freunde des Blogs einsehbar. Bitte logge Dich ein, oder schaue unter dem Menüpunkt 'Freunde des Blogs' für weitere Informationen wenn ein ernsthaftes Interesse besteht hier weiter zu lesen.









Neuste Kommentare